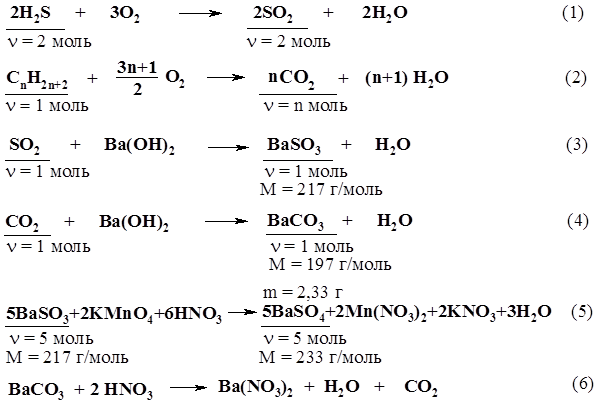- 5-6 литров газообразного бромоводорода было абсорбировано водой
- Исходные данные
- Приготовление раствора
- Процесс поглощения
- Результат и вычисления
- Выпаривание раствора
- Разбавление раствора
- Запишите данные
- Задачи на приготовление растворов
- Решение
- Видео:
- 10 класс(база).Решение задач на нахождение формулы по продуктам сгорания и массовой доли элемента.
5-6 литров газообразного бромоводорода было абсорбировано водой
Бромоводород (HBr) – газообразное вещество с желтоватым цветом. В данной статье будет рассказано о химической реакции, произошедшей при поглощении 5 6 литров газообразного бромоводорода водой.
Исходные данные
- Количество бромоводорода (HBr): 5 6 литров
- Количество воды (H2O) для поглощения бромоводорода
Приготовление раствора
Для поглощения бромоводорода было рассчитано, сколько воды следует использовать. Исходя из химической реакции:
HBr + H2O → H3O+ + Br—
Молярная масса бромоводорода (HBr) составляет около 81 г/моль. Поэтому масса бромоводорода, найденная в 5 6 литрах, равна:
Масса HBr = V × M = 5 6 л × 81 г/л = 4 536 г
Чтобы рассчитать, сколько воды нужно для полного поглощения бромоводорода, необходимо знать стехиометрическое соотношение между HBr и H2O. В данном случае, соотношение 1:1. То есть, каждую молекулу HBr можно превратить в одну молекулу H3O+ и одну молекулу Br—. Следовательно, масса воды, необходимая для поглощения бромоводорода, может быть рассчитана следующим образом:
Масса H2O = Масса HBr = 4 536 г
Процесс поглощения
Исходный 5 6 литров бромоводорода смешали с необходимым количеством воды. Бромоводород, имеющий желтоватый цвет, выделился при этом процессе. Концентрация полученного раствора будет зависеть от количества воды, добавленного в реакцию:
- Если весь бромоводород был полностью поглощен водой, полученный раствор будет иметь массовую концентрацию HBr равную 100%.
- Если вода была добавлена меньше, чем требуется для полного поглощения бромоводорода, концентрация раствора будет меньше 100%.
Результат и вычисления
В результате поглощения 5 6 литров бромоводорода водой, получено растворов с различной концентрацией. Расчет будет представлен для двух случаев:
- Выпаривание полученного раствора до конечного объема.
- Разбавление полученного раствора водой до заданного объема.
Выпаривание раствора
Для этого примера предположим, что весь полученный раствор был выпарен до конечного объема. Если его конечный объем составил 1 0 литров (по условию), рассчитаем массовую концентрацию полученного раствора:
Массовая доля = (Масса раствора / Масса раствора + Масса воды) × 100%
Масса раствора равна массе бромоводорода, найденного в исходных 5 6 литрах:
Масса раствора = 4 536 г
Масса воды (поскольку весь раствор был выпарен) равна 0 г:
Масса воды = 0 г
Теперь можем рассчитать массовую долю раствора:
Массовая доля = (4 536 г / 4 536 г) × 100% = 100%
Таким образом, после выпаривания полученного раствора до конечного объема (1 0 литров), его массовая доля будет составлять 100%.
Разбавление раствора
Для данного случая предположим, что полученный раствор разбавили водой до заданного объема. Если заданный объем разбавленного раствора составляет 2 0 литров, рассчитаем его концентрацию:
Массовая доля = (Масса раствора / Масса раствора + Масса воды) × 100%
Масса раствора (поскольку он был разбавлен) равна массе бромоводорода, найденного в исходных 5 6 литрах:
Масса раствора = 4 536 г
Масса воды равна массе разбавленного раствора:
Масса воды = 2 0 л × 1 0 0 0 г/л = 2 0 0 0 г
Теперь можем рассчитать массовую долю раствора:
Массовая доля = (4 536 г / (4 536 г + 2 0 0 0 г)) × 100% ≈ 69.4%
Таким образом, после разбавления полученного раствора водой до заданного объема (2 0 литров), его массовая доля составит около 69.4%.
Запишите данные
Использованное количество бромоводорода: 5 6 литров
Массовая доля полученного раствора при выпаривании: 100%
Массовая доля полученного раствора при разбавлении: около 69.4%
Таким образом, при поглощении 5 6 литров газообразного бромоводорода водой, можно получить раствор с различной массовой концентрацией. Эта концентрация зависит от количества добавленной воды и может быть рассчитана с помощью соотношения масс компонентов в реакции. Успешное выполнение химической реакции и получение нужного раствора требуют точного следования предоставленным данным и правильных вычислений.
Задачи на приготовление растворов
Решение
Давайте рассчитаем массу бромоводорода в исходном растворе:
Масса = объем * плотность = 5 6 * 30 = 168 г
С учетом массовой доли исходного раствора, масса сахара в конечном растворе будет равна:
Масса сахара = масса исходного раствора * массовая доля сахара = 168 * 5 / 30 = 28 г
Для получения 28 г раствора сахара нам понадобится сделать разбавление, т.е. добавить определенное количество воды.
Поскольку массовая доля сахара в конечном растворе должна быть 13-ного десятых, можно рассчитать объем конечного раствора:
Масса сахара = объем * массовая доля сахара
Объем конечного раствора = Масса сахара / массовая доля сахара = 28 г / 13 / 10 = 2.1538461538461537 литров
Чтобы растворить соль калия, смешанную со соляной кислотой, в итоге получить раствор, содержащий сахара, нужно добавить в полученный раствор соль кальция, ацетата и нитрата калия. В результате получим раствор соляной кислоты, цветом черного запишите его массу.
Видео:
10 класс(база).Решение задач на нахождение формулы по продуктам сгорания и массовой доли элемента.
10 класс(база).Решение задач на нахождение формулы по продуктам сгорания и массовой доли элемента. by Уроки химии с Жуковой Еленой 10,834 views 3 years ago 16 minutes