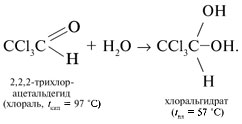- Реакция альдегида с водой: уравнение и особенности
- Химические свойства альдегидов и кетонов
- Химические свойства альдегидов и кетонов
- 11 Гидрирование
- 12 Присоединение воды
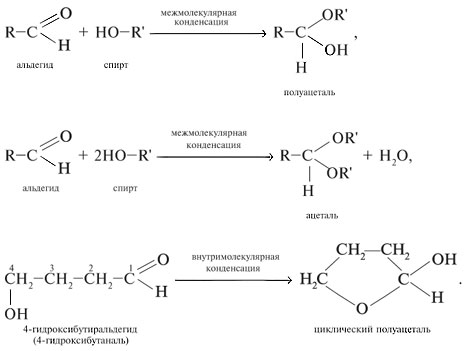
- 13 Присоединение спиртов
- 14 Присоединение циановодородной синильной кислоты
- 2 Окисление альдегидов и кетонов
- 21 Окисление гидроксидом меди II
- 22 Окисление аммиачным раствором оксида серебра
- 23 Жесткое окисление
- Видео:
- #40. Химические свойства альдегидов
Реакция альдегида с водой: уравнение и особенности
Альдегиды – это органические соединения, содержащие в своей структуре карбонильную группу, состоящую из атома углерода, связанного с атомом кислорода двойной связью. Данная группа функциональных групп характерна для альдегидов и кетонов. Она обладает рядом уникальных свойств и способна участвовать в различных химических реакциях.
Одной из наиболее известных реакций, которая может протекать с участием альдегидов, является реакция альдегида с водой. Уравнение этой реакции часто используется для описания процесса образования гидроксидов и солей альдегидов. При реакции альдегида с водой образуется спирт или кетон в зависимости от структуры и свойств исходного альдегида. При этом карбонильная группа альдегида претерпевает присоединение водного молекула, а двойная связь превращается в одинарную.
Процесс реакции альдегида с водой происходит в присутствии кислотного катализатора или щелочного раствора, например, гидроксида натрия. При данной реакции альдегид присоединяет воду через карбонильную группу, образуя гидроксильную группу. Выделяющиеся атомы водорода и гидроксила могут присоединиться к соседнему атому углерода в молекуле альдегида, образуя новую химическую связь и конечный продукт реакции.
Реакция альдегида с водой может протекать без выброса углеродной кислоты или окисления атома углерода, как это происходит в случае полного горения. Таким образом, при реакции альдегида с водой образуются спирты или кетоны, а не угольная кислота. Также возможна реакция альдегида с аммиаком или аммонием в присутствии серебра оксида, в результате которой образуются соли.
Химические свойства альдегидов и кетонов
Одним из основных свойств альдегидов и кетонов является их способность к окислению. Альдегиды могут окисляться до карбоновых кислот, в результате чего образуется группа COOH. Кетоны не могут подвергаться окислению до карбоновых кислот, так как в их структуре отсутствует атом водорода, связанный с атомом углерода, сопряженным с карбонильной группой.
Альдегиды и кетоны также могут быть подвергнуты конденсационной реакции, в которой гидроксильная группа одного соединения реагирует с карбонильной группой другого соединения, образуя новую химическую связь и выделяя молекулу воды. Эта реакция особенно характерна для альдегидов и называется «кетонированием» или «альдегидированием».
Карбонильные соединения, такие как альдегиды и кетоны, также могут образовывать производные с другими функциональными группами. Например, существует возможность образования карбонил-группы с атомами азота в результате реакции с аминосоединениями. Также существует возможность образования карбонил-группы с атомами серы в результате реакции с соединениями, содержащими группу -SH.
Альдегиды и кетоны могут проявлять свои химические свойства на основе их реакций с различными веществами. Например, они могут реагировать с гидридами и восстанавливаться до соответствующих спиртов. Также, альдегиды и кетоны могут реагировать с циановодородом, образуя соответствующие циангидрины. Они могут подвергаться полимеризации в присутствии кислот и гидроксидов меди или железа.
Таким образом, характерные свойства альдегидов и кетонов включают их способность к окислению, конденсации, образованию производных с другими функциональными группами, а также реакции с различными веществами.
Химические свойства альдегидов и кетонов
Присоединение воды к карбонильной группе альдегида или кетона является такой реакцией. В результате образуется гидрат, который имеет формулу вида R-C(OH)2 или R2C(OH)2, где R представляет собой остаток альдегида или кетона.
Альдегиды характеризуются свойством образовывать положительный ион альдолат (альдегид+оль), который может претерпевать конденсацию с молекулами карбонильных соединений. При этом образуется бо́льший молекулярный вес вещества.
Альдегиды и кетоны имеют возможность образовывать полимеры с помощью полимеризации. Например, полимеризация метаналя (формальдегида) приводит к образованию полиформальдегида, который в промышленности применяется как мощный антисептик.
Окисление альдегидов может происходить с помощью кислорода или других окислителей, что приводит к образованию карбоновых кислот. При этом образуется углекислый газ (CO2) и образование кислоты, которой присутствует карбонильная группа на молекуле. Например, метаналь окисляется до образования метановой кислоты (этановой).
Реакция альдегидов с аммиачным раствором описывается в уравнении. В результате такой реакции образуются именно альдегиды и их соединения с атомами водорода. Например, метаналь взаимодействует с аммиаком и образуется метиламино)метанол.
Характерной особенностью кетонов является отсутствие атома водорода в положении α-к углерода с карбонильной группой. Водород цепочки альдегида заменен на карбоновую группу –СН2-. Такая жесткая структура не позволяет карбонильной группе альдегида или кетона образовывать реакции с атомами меди(II) или другими соединениями, только атомами группы синильной(нитрильной).
11 Гидрирование
Например, гидрирование этаналя (формальдегида) приводит к образованию метанола:
- СН2О → СН3ОН
Альдегиды имеют карбонильную группу (связь C=O), которая характерна для нейтральных органических соединений. Группа карбонильного атома углерода может быть окислена до кислоты или снижена до спирта при наличии соответствующих химических реагентов.
Гидрирование альдегидов часто используется в органическом синтезе для получения первичных и вторичных спиртов. Эта реакция особенно важна при присутствии катализаторов, таких как цианид водорода или палладиевая паста.
Гидрирование карбоновых кислот, в противоположность альдегидам, приводит к образованию первичных и вторичных спиртов. При этом карбонильная группа окисляется до спирта, а водород присоединяется к атомам углерода, замещая группу -OH.
Гидрирование альдегидов и карбоновых кислот также имеет важное структурное значение, поскольку реакция образования альдегида путем частичного окисления соединений с активной метиловой группой называется «альдольная» реакция. Карбонильная группа также может быть укорочена до двух атомов с образованием алкана. С другой стороны, альдегиды могут быть окислены до соответствующих кислот.
Гидрирование альдегидов и карбоновых кислот обладает рядом свойств, которые характерны для данной группы органических соединений. Например, они реагируют со спиртами и основаниями, образуя группу гидроксила или карбонильной группы. Они также могут претерпевать замещение атомов в углеродной цепи или окисление до более сложных соединений.
12 Присоединение воды
К примеру, этаналь (ацетальдегид) взаимодействует с молекулами воды, при этом происходит присоединение водорода и окисление атома углерода, что приводит к образованию гидроксильного и гидридного остатка:
CH3-CHO + H2O → CH3-CHOH-CH3
Такая реакция присоединения воды к альдегиду или кетону характерна для нейтральной среды.
Важным классом соединений, образующихся в результате присоединения воды к альдегидам и кетонам, являются альдолы. Альдолом называется соединение, содержащее гидроксильную и карбонильную группы: CHOCHOH; при этом образуется два атома углерода, соединенные между собой. Существуют аддиционные соединения, получающиеся в результате реакции присоединения воды к альдегидам или кетонам в присутствии аммиачного катализатора и солей серебра или меди, и получение синильной кислоты, диметанальной кислоты и 3-гидроксипропанальной кислоты.
Присоединение воды также характерно для образования солей кислот. Это реакция, когда происходит присоединение гидроксильного остатка к атомам металла или металлиду, присутствующих в данной реакции, с образованием соответствующих солей. Например,
CH3-COH + NaOH → CH3-COO-Na+ + H2O
Присоединение воды к альдегидам и кетонам имеет особенность при присутствии окислителей, в частности серебряного оксида или серебряной пудры при взаимодействии с раствором кислорода или уксуснокислым гидролизом. В результате такой реакции образуется серебро восстановленное.
Присоединение воды к альдегидам и кетонам осуществляется на промышленности для получения определенных химических веществ, таких как синильная кислота, гераниловая кислота, ацетон и другие вещества. Эта реакция также может быть использована для получения полимеризационных соединений и формирования полимеров, например, этанального полиэтилена.
13 Присоединение спиртов
Альдегиды и кетоны обладают сходными свойствами, так как оба класса веществ имеют карбонильную группу (CO) в своей структуре. Группа альдегида обозначается формулой R-CHO, где R обозначает угольную группу. Группа кетона обозначается формулой R-CO-R’, где R и R’ представляют собой различные угольные группы. Положительный атом в группе альдегида или кетона связан с кислородом и гидроксидом или водородом.
Присоединение спиртов к альдегидам и кетонам происходит при участии гидроксидов щелочных металлов (NaOH, KOH), гидроксида аммония (NH3OH) или других оснований. В результате этой реакции образуется спирт и образуется карбонильное соединение.
Например, при взаимодействии этаналь (CH3CHO) с метанолом (CH3OH) в присутствии гидроксида натрия (NaOH) происходит образование метанолаат натрия (CH3COONa) и воды.
| Реакция | Продукты |
|---|---|
| CH3CHO + CH3OH | CH3COOCH3 + H2O |
Присоединение спиртов также характерно для альдегидов и кетонов при их окислении. При окислении альдегидов атому углерода карбонильной группы окисляются до группы кислот (COOH), а при окислении кетонов карбонильная группа остается неизменной.
Также присоединение спиртов может происходить в результате замещения положительного атома в карбонильной группе. Например, аммиак (NH3) может замещать водород в карбонильной группе, в результате чего образуется гидразин.
В реакции присоединения спиртов также могут участвовать другие соединения, такие как серебряное зеркало (толуол C7H8, серебро Ag) и циановодород (HCN). Например, при взаимодействии фенола (C6H5OH) с формальдегидом (CH2O) в присутствии гидроксида натрия (NaOH) происходит образование синильной кислоты (C6H5CN) и воды.
| Реакция | Продукты |
|---|---|
| C6H5OH + CH2O | C6H5CN + H2O |
В общем случае, реакция присоединения спиртов к альдегидам и кетонам проходит в похожей манере и является важным процессом в химии органических соединений.
14 Присоединение циановодородной синильной кислоты
Присоединение циановодородной синильной кислоты проводится в присутствии оснований или катализаторов. Один атом водорода от воды заменяется атомом циана (CN). Происходит конденсация циановодородной синильной кислоты с карбонильной группой альдегидов или кетонов. Существует множество химических реакций, которые могут привести к образованию соединения с цианогруппой.
Структурная формула циановодородной синильной кислоты: CHCN.
Окисление этаналь, который является простейшим альдегидом, в присутствии раствора серебра окислителя AgNO3 приводит к образованию цианистого серебра (CHCN-Ag) и аммиачным спиртом-основания.
Одна из важных химических реакций с участием циановодородной синильной кислоты – гидрирование. При этом реагентом выступает гидрированный карбонильный окислитель (например, LiAlH4), который превращает циановодородную синильную кислоту в соответствующий амин.
Присоединение циановодородной синильной кислоты может происходить также в присутствии фенолами или других карбоновых соединений. Окисление этих соединений в присутствии циановодородной синильной кислоты приводит к образованию соединений, содержащих карбонильную группу и группу CN.
Таким образом, присоединение циановодородной синильной кислоты является важной реакцией, позволяющей получать соединения с цианогруппой. Она может применяться в лабораторных условиях для получения различных органических соединений.
2 Окисление альдегидов и кетонов
Для окисления альдегидов и кетонов используется различные катализаторы, такие как серебряные соли или растворы серебряного оксида. Одним из распространенных катализаторов является раствор аммиачной серебряной кислоты.
Процесс окисления аммиачным раствором серебряной кислоты заключается в присоединении атома кислорода из воды к углеродной группе альдегида или кетона. При этом карбонильная группа превращается в группу синильной кислоты.
Формула окисления альдегидов или кетонов выглядит следующим образом:
Альдегид или кетон + 2[H] → карбонильная кислота
Окисление альдегидов или кетонов может протекать как в присутствии кислородных соединений, так и без них. Кислородное окисление альдегидов и кетонов приводит к образованию группы с положительным зарядом на карбонильной группе.
Окисление альдегидов и кетонов является важным процессом в химической промышленности. Он используется, например, для получения полимеризации формальдегида или метилового спирта. Также окисление альдегидов и кетонов может служить одним из этапов реакции окисления спиртов до кислот или конденсации альдегидов с амино-группой, а также фенолом.
Свойства окисления альдегидов и кетонов включают горение и химическую реакцию соединений, содержащих атомы кислорода, а также возможность образования высокомолекулярных соединений.
Альдегиды с двумя атомами углерода называются формальдегидами, а с тремя — уксусными альдегидами. Кетоны — это соединения, в которых два углеводородных фрагмента связаны группой карбонильного кислорода.
21 Окисление гидроксидом меди II
При окислении органических карбонильных соединений гидроксидом меди II происходит замещение карбонильного атома кислорода на атом меди, при этом образуется нейтральная циановодородная и/или соединения с другими карбонильными группами. Этот процесс называется окислением карбонильных соединений гидроксидом меди II.
Например, окисление метаналя (HCHO) гидроксидом меди II приводит к образованию углекислого газа (CO2) и метановой кислоты (HCOOH):
- 2Cu(OH)2 + HCHO → Cu2O + CO2 + 3H2O
- Cu2O + HCHO → HCOOH + Cu
Альдегиды и кетоны могут окисляться и другими окислителями, например, аммиачным хлоридом (NH4Cl). В этом случае, карбонильная группа превращается в карбонильную кислоту (r-COOH). Окисление альдегидов и кетонов может протекать с образованием оксида меди II (CuO) или других окисных продуктов.
Окисление альдегидов гидроксидом меди II может иметь различные примеси, например, гидроксид меди II может соответствовать иону меди II (Cu2+). В лабораторных условиях окисление альдегидов и кетонов можно осуществить с использованием гидроксида меди II (Cu(OH)2).
Таким образом, окисление гидроксидом меди II является одним из способов получения оксида меди II и других окисных соединений, а также может использоваться для получения карбонильных кислот и других окисных продуктов.
22 Окисление аммиачным раствором оксида серебра
Одним из возможных уравнений для этой реакции является:
AgOH + RCHO → RCOOH + Ag
В присутствии оксида серебра могут также происходить реакции замещения карбонильных групп. Например, фенол (C6H5OH) может претерпеть полимеризацию при воздействии гидроксида серебра:
AgOH + C6H5OH → (C6H4OH)n + Ag
Также, в результате окисления карбонильной группы, возможно получение кетонов и карбонильных кислот:
AgOH + R2CO → R2CO2H + Ag
Органические соединения, полученные в результате этих реакций, называются альдегидами и кетонами. Они широко используются в лабораторных и промышленных целях, например, для получения органических солей и других химических соединений.
Окисление аммиачным раствором оксида серебра характерно для кислоты серебра (AgOH) и является одним из методов окисления карбонильных групп. При этом происходит присоединение атома серебра к карбонильной группе, что приводит к образованию гидроксильной группы. Структурная формула гидроксильной группы выглядит так: -OH.
В процессе окисления аммиачным раствором оксида серебра происходит перенос электронов от карбонильной группы на аге или AgOH. При этом карбонильная группа оксидируется, а оксид серебра восстанавливается. Реакция окисления аммиачным раствором оксида серебра может протекать при нормальной температуре и давлении, при этом образуются гидроксильные соединения и группы гидроксильных соединений.
23 Жесткое окисление
Альдегиды и спирты могут быть окислены до кислот и соединений, содержащих группы аммиачного, циановодородного и метаналя. Аммиачное окисление – это процесс присоединения аммония к карбонильной группе альдегидов и кетонов с образованием аммиачной гидроксидной соли. Циановодородное окисление описывает реакцию присоединения циановодорода к алдегидам и кетонам. Эти окисления характерны для альдегидов и кетонов, имеющих положительный замещение на углеродах.
Спирты, подвергаясь окислению, могут превращаться в карбонильные соединения и кислоты. При частичном окислении алканол соединение превращается в альдегид, а при полном окислении – в кислоту. Кислотное окисление алканола может проходить с помощью хромового катализатора или меди. Окисление фенола описывается реакцией с присоединением гидроксильной группы к кольцевому углероду с образованием карбоксильной группы. Образование кислородных солей таких кислородсодержащих органических кислот используется для названия данной группы соединений – фенолы.
Вода в химических реакциях с участием альдегидов и спиртов может привести к их окислению или конденсации. При образовании альдегидов из альканов или присоединении к оним альдегидной группы с помощью меди, серебра или ртути используются вода и аммиак. Окислительные свойства воды применяются также при синтезе карбонильных соединений из соединений, содержащих карбонильную группу.
Видео:
#40. Химические свойства альдегидов
#40. Химические свойства альдегидов by Himikum 365 views 4 years ago 31 minutes