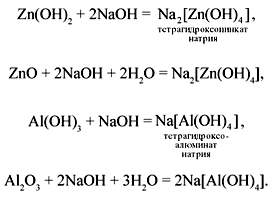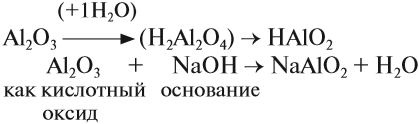Химическая реакция алюминия с щелочью в присутствии воды.
Алюминий — химический элемент, который обладает амфотерными свойствами. Это означает, что он может реагировать как с кислотами, так и с щелочами. При взаимодействии алюминия с водой образуется реакция, в ходе которой возникает гидроксид алюминия (Al(OH)_3).
Вода реагирует с алюминием при нагревании или длительном взаимодействии. При этом алюминий оксидируется на алюминиевый гидроксид с выделением водорода. Реакция представлена следующим образом:
2Al + 6H_2O -> 2Al(OH)_3 + 3H_2
Реакция воды с металлом алюминий происходит достаточно бурно, особенно при нагревании или использовании алюминия в порошкообразном виде. В результате реакции образуется осадок гидроксида алюминия, который обладает важными свойствами в химических процессах.
Гидроксид алюминия имеет высокую растворимость в воде. Это позволяет использовать его в процессе получения алюминия и его соединений. Например, гидроксид алюминия может быть использован в ходе реакции с солью алюминия и при взаимодействии с серной кислотой. Также гидроксид алюминия может быть получен взаимодействием алюминия с щелочью или водным раствором щелочи.
В природе алюминий образуется в виде множества бинарных соединений, включая криолит — минерал, содержащий алюминий и фтор. Взаимодействие алюминия с водой и его растворами также может возникать в виде оксида алюминия (Al_2O_3), который образуется природным путем. Здесь важно отметить, что вода с алюминием образует амфотерную реакцию, в ходе которой алюминий взаимодействует с оксидной кислотой или основанием, образуя растворимые соли или осадок гидроксида.
Видеоопыт с алюминием и водой демонстрирует, как происходит реакция алюминия с водой. При взаимодействии алюминия и воды происходит электронная передача, и алюминий оксидируется, образуя гидроксид алюминия. Реакция возникает со значительным выделением тепла, что может привести к зажиганию газа воздухом. Поэтому такую реакцию необходимо проводить с осторожностью и под контролем.
Алюминий щелочь вода реакция
Щелочь – это общее название для растворов гидроксидов щелочных металлов – натрия (NaOH), калия (КOH) и др., а также аммонийной соли (NH4OH). Щелочь обладает высокой щелочностью и используется в различных областях, включая химическую промышленность, где она применяется для получения многих веществ и соединений.
Реакция алюминия с щелочью, особенно с водным раствором щелочи, происходит достаточно бурно. В ходе реакции алюминий образует соль алюминия и высвобождается водород. Вода, в которой растворена щелочь, является амфотерным раствором, т.е. реагирует и с кислотами, и с основаниями. Соль алюминия (в виде амфотерного гидроксида Al(OH)3, известного под названием алюминий гидроксида) обладает низкой растворимостью в воде и образует осадок.
Алюминий обладает очень высокой химической активностью и способностью к пассивации, т.е. образованию на поверхности оксидной пленки Al2O3, которая защищает его от дальнейшего окисления. Поэтому реакция алюминия с водой происходит только при высоких температурах и в присутствии щелочи или кислоты.
В контексте алюминия и щелочи, вода является катализатором реакции. Реакционная способность щелочи позволяет активировать поверхность алюминия и ускорить реакцию. При этом образуются соли щелочи и газообразный водород. Такая реакция может быть представлена уравнением: 2Al + 6NaOH -> 2Na3AlO3 + 3H2.
Стоит отметить, что реакция алюминия с щелочью может протекать и с образованием бинарных соединений алюминия с галогенами – фтором, хлором, бромом и йодом. При этом образуются соответствующие халогениды алюминия, например, AlCl3 или AlI3.
Таким образом, реакция алюминия с щелочью (в том числе с водным раствором щелочи) является бурной и сопровождается выделением водорода. При нагревании алюминия избытком щелочи его поверхность покрывается оксидной пленкой Al2O3, что приводит к пассивации металла. Этот процесс может быть использован для получения алюминия из его оксидной руды при помощи расплава криолита.
Алюминий
Алюминий взаимодействует с щелочью и образует гидроксид алюминия (Al(OH)3), который называют алюминиевой щелочью. Это амфотерное вещество, которое растворяется в воде и образует раствор средней щелочности.
Алюминий также может реагировать с кислотами, образуя соли. В частности, он может взаимодействовать с серной кислотой и образовывать алюминиевые сульфаты.
Алюминий активно применяется в процессе получения металла путем электролиза расплава оксида алюминия (Al2O3), который называется греческой щелочью.
Азот, аммиак и гидроксид натрия также могут взаимодействовать с алюминием. При этом образуются соединения такие как оксид аммония (NH3), гидроксид алюминия и гидроксид натрия (NaOH).
Водород может образовываться в ходе взаимодействия алюминия и воды при нагревании или в присутствии катализаторов. Эта реакция может быть продемонстрирована в видеоопыте, например, с помощью кусочка алюминия и воды в пробирке.
При нагревании алюминий также может реагировать с галогенами (например, хлором) и образовывать бинарные соединения, такие как хлорид алюминия (AlCl3).
Алюминий обладает способностью к пассивации, то есть образованию пленки оксида на поверхности, которая предотвращает дальнейшую реакцию с водой или другими веществами. Это является причиной высокой коррозионной стойкости алюминия.
Алюминий Химия алюминия и его соединений
При взаимодействии алюминия с раствором щелочи, такой как NaOH, происходит реакция, в результате которой образуется соль и вода:
2Al + 6NaOH → 2Na3AlO3 + 3H2O
Также алюминий может реагировать с кислотами, образуя алюминиевые соли и высвобождая водородный газ:
2Al + 6HCl → 2AlCl3 + 3H2↑
Алюминий вступает в реакцию с водой только при нагревании и образует гидроксид алюминия:
2Al + 6H2O → 2Al(OH)3 + 3H2↑
Алюминий также способен взаимодействовать с оксидной щелочью и образовывать соль, известную как криолит (Na3AlF6). Эта реакция является очень полезной в химической промышленности, так как криолит используется в процессе выплавки алюминия из его руды.
Одной из особенностей химии алюминия является его способность к пассивации. Это означает, что поверхность металла покрывается тонким слоем оксидов или гидроксидов, которые защищают его от дальнейшей реакции с окружающей средой.
Алюминий и его соединения имеют широкое применение в различных отраслях промышленности. Они используются в производстве авиационных и автомобильных деталей, упаковочных материалов, конструкционных материалов и многих других. Химия алюминия и его соединений продолжает развиваться, и поэтому постоянно возникают новые вопросы и исследования в этой области.
Алюминий
У алюминия высокая электроотрицательность и он обладает амфотерными свойствами, что делает его активным при взаимодействии с различными веществами.
Алюминий реагирует с кислотами и образует соли алюминия и водород. При этом образуется тонкая пленка оксида алюминия, которая защищает металл от дальнейшего взаимодействия с кислотой.
Взаимодействие алюминия с щелочью, например, раствором гидроксида натрия (NaOH), также является реакцией, при которой образуется водород и соли гидроксидов алюминия.
Алюминий обладает амфотерными свойствами, поэтому он может взаимодействовать с щелочами и кислотами. В результате таких реакций образуются соли алюминия или гидроксиды алюминия.
Аллюминий также может взаимодействовать с растворами гидроксидов, основаниями, кислотами и солями. В результате образуются амфотерные соли и гидроксиды алюминия.
При взаимодействии алюминия с галогенами, например с хлором (Cl), бромом (Br) или йодом (I), образуются галогениды алюминия – хлорид алюминия (AlCl3), бромид алюминия (AlBr3) или йодид алюминия (AlI3).
Алюминий также может взаимодействовать с водой, в результате чего образуется водород и гидроксид алюминия (Al(OH)3).
Одним из способов получения алюминия является его электролиз с помощью раствора галогенида алюминия в расплаве с галогенами.
Алюминий также может взаимодействовать с аммиаком (NH3) и образовывать гидроксид алюминия и аммиакат алюминия.
В обычных условиях алюминий не растворяется в воде, но при взаимодействии с кислотой натрия (Na3AlF6) или криолитом в определенных условиях образуется растворимый и стабильный комплекс алуминия и фторида — Na3AlF6.
В присутствии избытка щелочи, при взаимодействии алюминия с комнатной температурой водой, может образовываться гидрогенид алюминия (AlH3).
Таким образом, алюминий проявляет активность при взаимодействии с различными химическими соединениями и веществами, образуя различные соли и соединения.
Видео:
Взаимодействие алюминия со щелочью и водой
Взаимодействие алюминия со щелочью и водой by paramitacenter 6,790 views 12 years ago 1 minute, 6 seconds