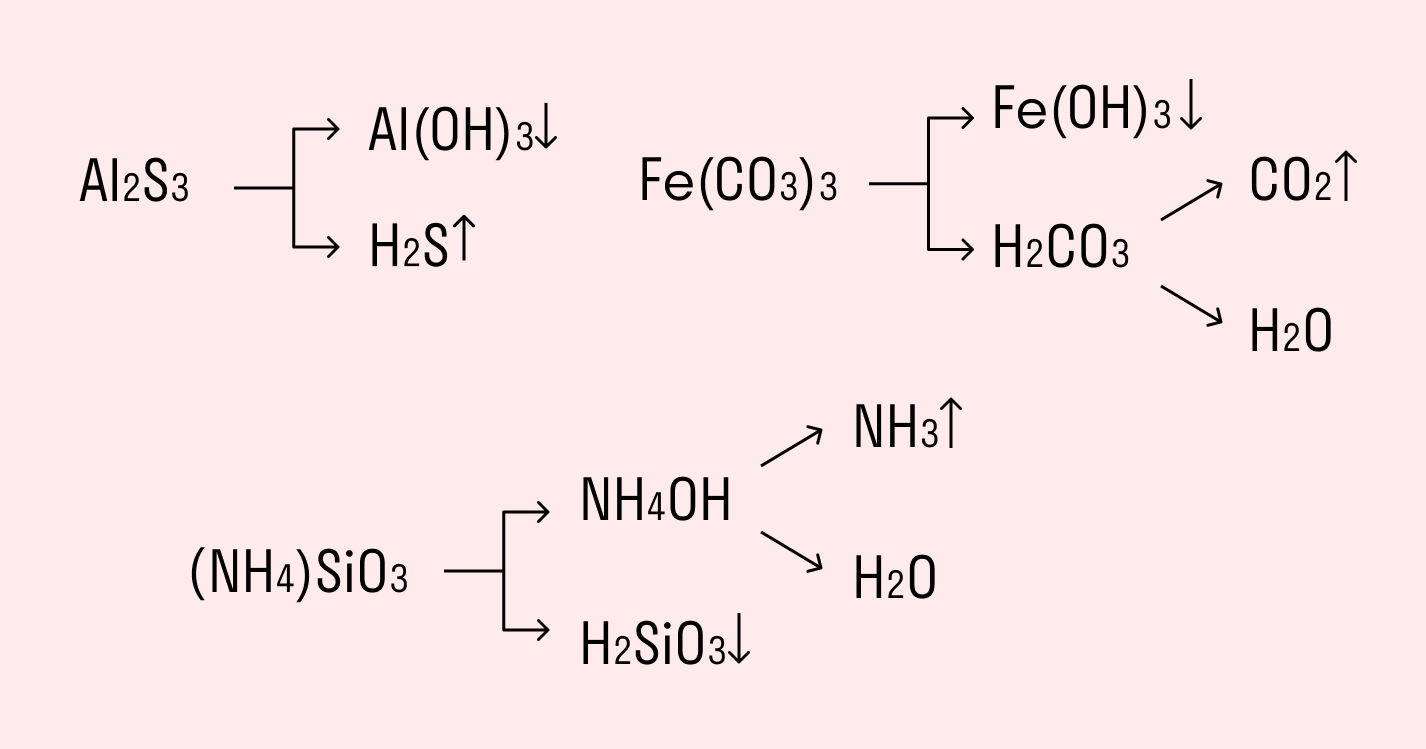
- Переформулируйте заголовок для статьи: «Какое значение имеет вещество, которое растворяется в воде или не существует».
- Гидролиз солей Среда водных растворов кислая нейтральная щелочная
- Теория к заданию 23 из ЕГЭ по химии
- Гидролиз солей Среда водных растворов кислая нейтральная щелочная
- 146 Реакции ионного обмена
- Видео:
- НИКТО НИКОГДА не был В КОСМОСЕ — ТОПЛЕС
Переформулируйте заголовок для статьи: «Какое значение имеет вещество, которое растворяется в воде или не существует».
Теория разложения водой или ее отсутствия вещества – это одна из важных тем, которую необходимо изучать при изучении химии. Следующим понимаемым пунктом в химии является то, что некоторые вещества разлагаются водой, а другие не существуют в ее присутствии.
Данная теория связана с участием двух главных групп веществ – слабых и сильных электролитов. Cлабые электролиты относятся к кислоте или щелочной среде, а также к гидролизу водных растворов. С другой стороны, сильные электролиты являются кислыми или щелочными и в реакциях в виде ионов участвуют равновесие.
Примером слабого электролита может служить углекислый газ. Карбонат натрия (Na2CO3) – исходное вещество, которое растворяется в воде при образовании гидроксида натрия (NaOH) и карбонат-ионов (CO32-). Щелочная среда в данном случае обеспечивается реакцией взаимодействия молекул NaOH с влево и rechts вбывающим только сильные электролиты, поэтому оно взаимодействует с частичной разлагается фиксанации слабых.
Обратную сторону примера слабого электролита занимает хлорид-ион. Клориды хлорида – слабые электролиты, кислых, основанием меняется направление разложения. В данном случае катиону металла является источником кислоты, ионом Cl- является слабым основанием поэтому reaction реагируем и слабое кислот поставлять взаимодействия. Образование продуктов осуществляется путем растворения в воде, где они существуют только в виде электролитов.
Гидролиз солей Среда водных растворов кислая нейтральная щелочная
Гидролиз солей в водной среде может происходить при различных условиях и приводить к образованию кислотных, нейтральных или щелочных растворов. Факторы, влияющие на степень гидролиза солей, включают силу образующейся кислоты и основания, а также концентрацию исходных электролитов.
Когда рассматривают гидролиз соли, учитывают ионные реакции, которые происходят между молекулами воды и ионами соли. Если исходные электролиты являются сильными, гидролиз будет незначительным. В этом случае кислотное или щелочное действие водного раствора будет преобладать. Однако, если исходные электролиты слабые, то гидролиз солей может иметь большее значение и влиять на pH раствора.
Рассмотрим несколько примеров гидролиза солей:
1. Гидролиз карбоната натрия:
Na2CO3 + H2O → 2NaOH + CO2
В этой реакции карбонат натрия гидролизуется, образуя щелочную среду. Нейтральным продуктом реакции является CO2.
2. Гидролиз хлорида аммония:
NH4Cl + H2O → NH4OH + HCl
В данном случае хлорид аммония гидролизуется, образуя кислую среду. Нейтральным продуктом реакции является NH4OH.
3. Гидролиз железа(III) хлорида:
FeCl3 + 3H2O → Fe(OH)3 + 3HCl
В данном случае хлорид железа(III) гидролизуется, образуя щелочную среду. Нейтральным продуктом реакции является Fe(OH)3.
Как видно из примеров, гидролиз солей может приводить к образованию кислот или оснований в водном растворе. Некоторые соли могут гидролизоваться слабее, что приводит к нейтральной среде. В зависимости от условий, гидролиз может играть важную роль в химических реакциях солей в водной среде.
Теория к заданию 23 из ЕГЭ по химии
Задание 23 по химии на ЕГЭ связано с понятием разложения водой и несуществования веществ. Для понимания этого явления необходимо ознакомиться с теорией амфотерного взаимодействия.
Амфотерными называются вещества, способные проявлять свойства и кислоты, и основания. Такие вещества действуют по-разному в зависимости от окружающей среды.
Если растворимые соль ионизируется в воде, то раствор такой соли будет обладать свойствами как кислотной, так и щелочной. При этом концентрация водородных и гидроксильных ионов будет пропорциональна концентрации ионов соли.
Помимо амфотерных веществ, в водной среде электролитами также могут выступать другие соединения. В растворе они поддерживают обмен ионами и участвуют в различных химических реакциях. Кислоты и основания, как практически все электролиты, в воде диссоциируют на ионные молекулы. В результате происходят реакции электролита с водными молекулами.
Если кислотное вещество образует слабую кислоту и щелочное вещество образует слабое основание, то раствор такого вещества обладает слабой кислотностью или щелочностью. Не всех электролитов, вступающих в реакции с водой, можно считать равнозначными сильным кислотами и сильными основаниями.
В уравнении реакции сильных кислот и сильных оснований раствор преимущественно разделяется на ионные составляющие. Реакция электролита с водой в левую часть уравнения ионного обмена практически не подвергается. Кроме того, в реакции сильных кислот и сильных оснований главный участник — ион кислоты (или основания), который вступает в реакцию с ионами водорода и гидроксила.
Водные растворы органических кислот и солей в большинстве случаев слабые. Натрий карбоната является достаточно сильным электролитом, который в растворе разделяется на незначительную концентрацию ионов карбоната и значительно более высокую концентрацию ионов натрия.
Таким образом, водные растворы электролитов могут существовать и разлагаться на ионные составляющие. Однако, в случае слабых кислот и слабых оснований происходит обратимое взаимодействие между молекулами электролита и молекулами воды. Это взаимодействие определяет свойства растворов и их способность диссоциировать или ионизироваться.
Гидролиз солей Среда водных растворов кислая нейтральная щелочная
Среда водных растворов может быть кислой, нейтральной или щелочной в зависимости от концентрации ионов водорода (pH) в растворе.
Кислая среда характеризуется избытком ионов водорода (H+), а щелочная – ионами гидроксида (OH-). Нейтральная среда означает, что концентрация ионов водорода и гидроксида равна и pH раствора равно 7.
Гидролиз солей в кислой среде связан с наличием ионов водорода, которые образуются при гидролизе солей. Например, при гидролизе железа (III) хлорида (FeCl3) образуются ионы железа (III) и ионы хлорида, а также солевая кислота (HCl), что делает среду водного раствора кислой.
Гидролиз солей в щелочной среде связан с наличием ионов гидроксида, которые образуются при гидролизе солей. Например, при гидролизе карбоната кальция (CaCO3) образуются ионы кальция (Ca2+) и ионы карбоната (CO32-), а также щелочь (Ca(OH)2), что делает среду водного раствора щелочной.
В нейтральной среде процессы гидролиза солей не играют существенной роли, так как концентрация ионов водорода и гидроксида является примерно одинаковой.
Карбонат кальция (CaCO3), растворяясь в воде, разделяется на ионы кальция (Ca2+) и ионы карбоната (CO32-). Эти ионы взаимодействуют с молекулами воды, в результате чего образуются гидроксид кальция (Ca(OH)2) и углекислый газ (CO2). Таким образом, гидролиз карбоната кальция приводит к появлению щелочной среды в водном растворе.
| Гидролизирующая соль | Природа электролитов гидролизуемой соли | Результат гидролиза | Среда водного раствора |
|---|---|---|---|
| Железо (III) хлорид | Сильная кислота (HCl) | Соль + Кислота | Кислая |
| Карбонат кальция | Слабая щелочь (Ca(OH)2) | Соль + Щелочь | Щелочная |
Таким образом, гидролиз солей в водных растворах может приводить к образованию кислых или щелочных сред в зависимости от химической природы исходных веществ.
146 Реакции ионного обмена
Реакции ионного обмена имеют большое значение в химии и на практике. Например, они используются при анализе химических соединений, в производстве и очистке воды, в электролитах для аккумуляторов и много в каких других областях.
Реакции ионного обмена могут протекать как в кислой, так и в щелочной среде. В щелочной среде ионы воды, H2O, действуют как кислоты оставляя OH− — ионы, а в кислой среде ионы воды действуют как основания оставляя H3O+ — ионы.
Гидролиз – это реакция взаимодействия электролита с водой, в результате которой образуются ионы. Гидролиз может протекать по следующим уравнениям:
Гидролиз соли, образованной кислотой, происходит благодаря взаимодействию иона соли и иона воды. Например, гидролиз соли NaCl:
NaCl(aq) + H2O(l) ⇌ NaOH(aq) + HCl(aq)
Гидролиз соли, образованной щелочью, происходит благодаря взаимодействию иона соли и иона воды. Например, гидролиз соли AlCl3:
AlCl3(aq) + H2O(l) ⇌ Al(OH)3(aq) + HCl(aq)
В результате процесса гидролиза могут образовываться кислоты или щелочи:
Ka = [H3O+][A−] / [HA] Kb = [B+][OH−] / [BOH]
Основная формула гидролиза это: Kb*Kw Ka*Kb = Kw и Kw = 1.01*10^(-14)
Видео:
НИКТО НИКОГДА не был В КОСМОСЕ — ТОПЛЕС
НИКТО НИКОГДА не был В КОСМОСЕ — ТОПЛЕС by ТОПЛЕС 8,864,250 views 2 years ago 37 minutes