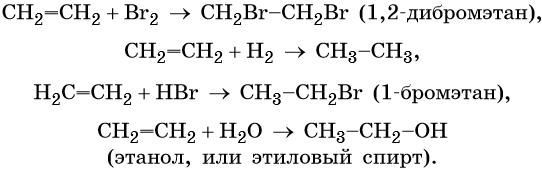Один из методов получения бромэтана — реакция этилена с бромной водой
Реакция замещения в органической химии – это процесс, в результате которого одна группа атомов или ионов замещается другой группой. Одной из наиболее известных реакций замещения в органической химии является взаимодействие этилена (C2H4) с бромной водой (HBrO). Этот процесс хорошо исследован и широко применяется в промышленности для получения различных органических соединений.
Этилен – это простейший представитель алкенов, органических соединений, в молекуле которых имеется одна или более π-связь между углеродными атомами. Именно благодаря этой π-связи алкены обладают своими уникальными свойствами и могут подвергаться различным химическим превращениям.
Реакция этилена с бромной водой представляет собой окисление двойной связи между углеродными атомами этилена при присоединении молекулы воды. В результате этой реакции образуются бромэтанол (C2H3BrO), бромоводородная кислота (HBr) и гидрат брома (HBrO), которые имеют различные применения в химической и фармацевтической промышленности.
Окисление алкенов, включая реакцию этилена с бромной водой, является одним из важных правил химического преобразования органических соединений. Также существуют другие реакции, такие как гидрогалогенирование, полимеризация, изомеризация, разрыв π-связей и замещение связей в цепи. Кроме того, этилен может подвергаться каталитическому окислению и присоединению кислорода, например с помощью перманганата калия, что приводит к образованию углекислого газа и воды.
Химические свойства алкенов
При взаимодействии алкенов с водой происходит гидратация двойной связи. В этом случае атом кислорода присоединяется к одной из связей между атомами углерода, образуя кетон или спирт. Двойная связь алкена предпочтительно подвергается окислению, и поэтому неотступно вступает в реакции с бромной водой. Реакция происходит под воздействием света или перманганата калия, в присутствии сильных кислот. Эти реакции можно условно разделить на жесткое и мягкое окисление.
Одним из свойств алкенов является их способность к горению. При горении алкенов происходит полное окисление атомов углерода и водорода, и образуется углекислый газ и вода. Горение алкенов протекает с ярким пламенем и выделяет значительное количество теплоты.
Алкены также подвергаются полимеризации – реакции присоединения молекул алкена друг к другу. При полимеризации образуются многочисленные молекулы полимеров соединенные друг с другом боковыми связями, образуя длинные цепи. Полимеры, получающиеся в результате полимеризации алкенов, используются широко в производстве пластиков, эластомеров и других полимерных материалов.
Кроме того, алкены подвержены различным реакциям изомеризации, при которых одна из двух связей между атомами углерода перегруппируется, образуя другой изомер. Реакции изомеризации могут происходить как спонтанно, так и под воздействием катализаторов.
| Окисление алкенов | Гидратация алкенов | Горение алкенов |
|---|---|---|
| Происходит под действием света или перманганата калия в присутствии сильных кислот | Происходит под действием воды в присутствии кислоты или катализатора | Происходит с ярким пламенем и выделяет теплоту |
Химические свойства алкенов
Алкены представляют собой класс органических соединений, которые отличаются от алканов наличием двойной связи между атомами углерода. Из-за наличия двойной связи, алкены обладают определенными химическими свойствами, которые отличают их от алканов.
Одним из основных химических свойств алкенов является их активность при различных реакциях. Алкены способны претерпевать реакции замещения, гидратации, галогенирования, окисления, полимеризации и другие.
Реакция замещения основана на замене одной или нескольких атомов в молекуле алкена другими атомами или ионами. Наиболее известной реакцией замещения является гидрохлорирование, при котором к молекуле алкена добавляется молекула HCl и образуется продукт, содержащий замещенную метиловую группу.
Гидратация алкенов происходит при взаимодействии алкена с водой. В результате гидратации в молекуле алкена образуется спирт.
Галогенирование представляет собой реакцию алкена с хлором, бромом или йодом. При этом на двойную связь алкена присоединяется одна или две галогенные группы.
Окисление алкенов происходит при взаимодействии алкена с кислородом. Образуется кетон или альдегид, в зависимости от условий реакции.
Полимеризация алкенов является реакцией, при которой молекулы алкена присоединяются друг к другу, образуя молекулы полимера. Эта реакция широко используется в производстве пластмасс и синтетических материалов.
В результате горения алкенов преимущественно образуется углекислый газ и вода. Например, при полном сгорании пропилена (C3H6) уравнение реакции выглядит следующим образом: C3H6 + 9/2 O2 → 3 CO2 + 3 H2O.
Таким образом, химические свойства алкенов обусловлены наличием двойной связи между атомами углерода. Они проявляют активность при реакциях замещения, гидратации, галогенирования, окисления, полимеризации и других процессах.
1 Реакции присоединения
Одной из наиболее распространенных реакций присоединения является гидратация алкенов. При гидратации двойной связи алкена с молекулой воды образуется одна или несколько новых химических связей между атомами. Например, при гидратации пропилена (C3H6) образуется пропанол (C3H7OH).
Также одной из важных реакций присоединения является галогенирование алкенов. При галогенировании атомы галогенов, такие как хлор или бром, добавляются к двойной связи алкена. Например, при галогенировании этилена (C2H4) с бромом (Br2) образуется 1,2-дибромэтан (C2H4Br2).
Реакции присоединения имеют множество применений, в том числе в синтезе органических соединений, производстве пластмасс, веществ для лекарственных препаратов и других сферах химической промышленности. Знание этих реакций позволяет ученым создавать новые вещества с желаемыми свойствами и разрабатывать новые методы синтеза органических соединений.
Видео:
Задание 12. ЕГЭ 2022 по химии (ЕГЭ 2010 по химии. Демо. А26. Реакции с бромной водой)
Задание 12. ЕГЭ 2022 по химии (ЕГЭ 2010 по химии. Демо. А26. Реакции с бромной водой) by Your system education 167 views 6 years ago 4 minutes, 15 seconds