- Вода как кислая среда: роль этилена в процессе.
- Химические свойства алкенов
- Химические свойства алкенов
- 1 Реакции присоединения
- 11 Гидрирование
- 12 Галогенирование алкенов
- 13 Гидрогалогенирование алкенов
- 14 Гидратация
- 15 Полимеризация
- 2 Окисление алкенов
- 21 Каталитическое окисление
- 22 Мягкое окисление
- 22 Жесткое окисление
- 23 Горение алкенов
- 3 Замещение в боковой цепи
- 4 Изомеризация алкенов
- Видео:
- Горение этилена
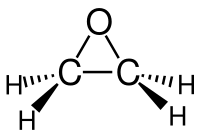
Вода как кислая среда: роль этилена в процессе.
Этилен представляет собой простейший представитель класса органических соединений — алкенов. Он состоит из двух углеродных атомов, связанных двойной связью. Этилени присоединяется к различным веществам, образуя разнообразные соединения.
Вода является кислой средой, поэтому она способна присоединяться к этилену. При этом происходит гидратация молекул этилена, в результате которой появляются молекулы этиленгликоля. Уравнение реакции этилен + вода → этиленгликоль может быть представлено следующим образом:
C2H4 + H2O → C2H6O2
Этилен обладает рядом свойств, благодаря которым его широко используют в биологических и промышленных процессах. Преимущественно, этилен применяется в органическом синтезе, происходящем при присоединении к нему других веществ. Кроме того, этилен применяется в процессе полимеризации, в результате которого образуются полимерные цепи.
Одной из характеристических реакций этилена является его горение. При горении этилена происходит присоединение к нему атомов кислорода из воздуха, а также окисление углеродных атомов. Уравнение реакции горения этилена: C2H4 + 3O2 → 2CO2 + 2H2O. Одна из особенностей горения этилена заключается в том, что оно может протекать под воздействием света, без катализаторов. Такое горение называется условно жестким.
Химические свойства алкенов
Алкены обладают рядом химических свойств, которые отличают их от алканов, содержащих только одинарные связи между атомами углерода. Одной из основных характеристик алкенов является их реакционная способность.
Алкены подвергаются реакциям присоединения, в которых добавляются новые атомы или группы атомов к π-связи. Например, при гидратации алкенов в присутствии кислорода и воды происходит присоединение водной молекулы к π-связи, образуется алкоголь. Также алкены могут присоединяться взаимодействию с другими веществами, например, в реакции гидратации при взаимодействии с кислородом и водой образуется углекислый газ.
Реакции горения и окисления также характерны для алкенов. При горении алкенов происходит их окисление кислородом из воздуха, в результате чего образуется углекислый газ и вода.
Алкены также подвергаются реакциям замещения, при которых одна или несколько атомов или групп атомов замещаются другими. Например, в реакции хлорирования алкенов в присутствии хлора замещение происходит на π-связи, образуется хлорированный продукт.
Полимеризация является одной из дополнительных реакций алкенов. В результате этой реакции множество молекул алкена связываются между собой, формируя полимерную цепь. Примером полимеризации является процесс образования полиэтилена из пропилена, где молекула пропилена соединяется с другими молекулами пропилена, образуя длинную полимерную цепь.
Изомеризация также является одной из возможных реакций алкенов. В процессе изомеризации атомы водорода и функциональные группы могут перемещаться между атомами углерода, меняя структуру молекулы. Эта реакция может происходить как при нагревании, так и при воздействии света.
Химические свойства алкенов
Некоторые химические свойства алкенов:
| Свойство | Описание |
|---|---|
| Горение | При горении алкенов происходит реакция с кислородом, в результате которой образуется углекислый газ и вода. Например, пропилен при сгорании в окислении присоединяется кислород и образуется углекислый газ и вода: |
| Явления окисления | Алкены подвергаются окислению. Например, этен водой медленно реагирует с перманганатом калия и окисляется до уксусной кислоты: |
| Добавление галогенов | Алкены могут присоединять галогенирование. Например, хлорирование этена может привести к образованию хлорэтана: |
| Замещение атома водорода | Алкены могут подвергаться замещению атома водорода. Например, при взаимодействии пропилена с хлоридом водорода может образоваться пропил-хлорид: |
| Изомеризация | Алкены могут подвергаться изомеризации, в результате чего образуются изомеры. Например, изомеризация 1-бутена может привести к образованию 2-бутена: |
| Гидратация | Алкены могут вступать в реакции с водой. Например, этен может присоединиться к молекуле воды и образовать этанол: |
| Полимеризация | Алкены могут подвергаться реакции полимеризации, в результате которой образуются длинные цепи молекул. Например, в полимеризации этена образуются полиэтиленовые цепи: |
1 Реакции присоединения
Мягкое водой окисление пропилена происходит по правилу алкенов. В результате гидратации присоединяется вода между двойными связями C2 и C3, образуя 4,15-гидратацию этилена.
Окисление этилена протекает по правилу алкенов и может привести к образованию двух различных фрагментов: 4,21-окисления двойной связи и 4,15-окисления одной из CH2-групп, связанной с углеродом. В горении этилен молекулы окисляются дважды.
В реакциях гидрирования или гидрогалогенирования, а также в замещении боковой группы происходит присоединение новых атомов или групп атомов к молекуле этилена.
Например, при хлорировании этилена в присутствии хлора происходит замещение одной из водородных связей на водородную галогенирование. В результате образуются молекула хлорэтана и большое количество гидрохлористого исомера.
При нагревании этилена в присутствии кислорода происходит жесткое окисление и образуется углекислый газ. Реакция окисления может быть ионной или электрофильной.
Окисление этилена может также протекать взаимодействием с галогеном, при этом образуются галогеналкилены. Углеводороды также участвуют в реакциях полимеризации, галогенирования и изомеризации.
В результате реакции присоединения или окисления этилен образует различные химические соединения и может быть использован в различных промышленных процессах.
11 Гидрирование
Гидрирование может происходить при нагревании в присутствии катализаторов (например, платины или никеля) или под воздействием свету. При этом образуются различные побочные продукты, такие как гидрогалогенирование или окисление.
Гидрирование алкенов преимущественно протекает по правилу Марковникова, согласно которому водород присоединяется к атому углерода с наибольшим числом водородных атомов. В результате образуются молекулы соединений сгорания этилен в этом случае разрывается на два атома углерода, каждый из которых присоединяется к по одному атому водорода.
Гидрирование кетонов происходит с присоединением двух атомов водорода, образуется два независимых компонента, которые можно разделить на два кетона, например, при гидрировании ацетон образуется изопропиловый спирт и пропиленовый спирт.
Гидрирование алкенов и кетонов может происходить не только в присутствии катализаторов, но и при хлорировании или окислении. В этом случае присоединение водорода происходит к углеродной цепи под воздействием химических веществ, таких как хлор или кислоты.
Гидрирование алкенов в воде приводит к образованию гидратов алкенов, в которых в молекулах связь между атомами углерода и водорода является жесткой. Гидрирование алкенов может происходить и под воздействием ионному, например, при присоединении водорода к пропану образуется пропанол.
12 Галогенирование алкенов
Например, при хлорировании пропилена (С3Н6) под действием хлора (Сl₂) и катализаторов (обычно это железо или калий хлорид) происходит замещение водородных атомов в пропилене хлорными атомами:
| С3Н6 (пропилен) | + | Сl₂ (хлор) | → | С3Н5Сl (хлорпропан) |
Галогенирование алкенов происходит также в водной среде. В этом случае молекулы воды присоединяются к π-связи алкенов, образуя специфические гидратные фрагменты:
| С3Н6 (пропилен) | + | Н₂О (вода) | → | С3Н6О (пропанол) |
Окисление алкенов также может происходить при нагревании с применением окислителей, например, перманганатом калия (КMnO₄), при этом образуется углекислый газ и вода:
| С3Н6 (пропилен) | + | КMnO₄ (перманганат калия) | → | СО₂ (углекислый газ) + Н₂О (вода) |
Галогенирование алкенов и их окисление – это химические реакции, основанные на взаимодействии галогенов и окислителей с π-связью алкенов. На практике такие реакции широко используются для получения различных галогенированных и окисленных углеводородов с определенными свойствами.
13 Гидрогалогенирование алкенов
Гидрогалогенирование пропилена, например, может привести к образованию хлорпропана или бромпропана. Эта реакция представляет собой хороший способ синтеза органических соединений с помощью бесцветных газообразных галогенов или их растворов в водном растворе калия галогенидов.
Процесс гидрогалогенирования алкенов может быть проиллюстрирован следующим уравнением:
CH2=CH2 + HX → CH3CH2X
где X – галоген (клор или бром).
Молекулы алкенов подвергаются гидратации, образуя хлориды или бромиды алкила, при электрофильном взаимодействии с водным раствором галогенида, присутствующим в воде.
Процесс гидрогалогенирования алкенов осуществляется при наличии каталитического присутствия галогенида. Каталитическая реакция позволяет происходить без исчезновения каталитических компонентов.
14 Гидратация
В случае каталитической гидратации, взаимодействие происходит между молекулой воды и двойной связью алкена. Уравнение гидратации можно представить следующим образом:
CH2=CH2 + H2O → CH3CH2OH
Процесс гидратации может протекать не только с участием воды, но и с участием других веществ. Например, гидратация молекул пропилена может протекать при воздействии на них света или кислоты. В результате гидратации образуется гидрат пропилена:
CH3CH=CH2 + H2O → CH3CH(OH)CH3
Окисление алкенов может приводить к образованию кетонов. Так, при окислении пропилена образуется акетон:
CH3CH=CH2 + [O] → CH3COCH3
Изомеризация атомов в молекуле алкена может происходить при взаимодействии с углекислым газом и перманганатом калия. В результате образуются изомерные соединения.
Гидратация алкенов преимущественно происходит под воздействием кислорода или нагревании. Вода при гидратации алкена может присоединиться к либо к одному, либо к обоим атомам углерода в зависимости от режима реакции.
Гидратация алкенов также может протекать в ионном виде. В этом случае происходит присоединение водного иону воды. Примером такой реакции является присоединение к нему воды:
CH2=CH2 + H3O+ → CH3CH2OH
Гидратация алкенов может происходить при взаимодействии с различными химическими соединениями. Однако, наиболее распространенным механизмом гидратации является протекание реакции с водой.
15 Полимеризация
Полимеризация может протекать при взаимодействии алкена с водой при ее нагревании или под действием света. В результате этой реакции из двух молекул этилена образуется одна цепь полиэтилена с большим числом присоединенных фрагментов СН-СН.
Полимеризация может также протекать в кислой среде, где присутствует кислород воды. В этом случае дополнительно образуются молекулы воды и происходит присоединение кислорода к фрагментам СН-СН. Окисление атомов углерода из вещества при этом может происходить в результате гидрирования, окисления, замещения и других реакций.
Полимеризация этилена может также протекать в присутствии катализаторов, таких как хлорирование, окисление перманганатом калия и др.
2 Окисление алкенов
Одной из основных реакций окисления алкенов является горение. При горении алкенов происходит присоединение атомов кислорода из воды, образуя углекислый газ.
Окисление алкенов также может происходить в более мягкой форме, например, при присоединении галогенирования или хлорирования атомов к атому углерода в молекулах алкенов.
Другой реакцией окисления алкенов является изомеризация. При этой реакции фрагменты молекул алкенов переустройствуя свои связи, образуя новые изомеры с различным количеством двойных связей.
Каталитическое гидрирование алкенов происходит при присоединении водорода к двойной связи атомов углерода алкена.
Реакции окисления алкенов аналогичны реакциям окисления алканов, однако в алкенах можно наблюдать большую активность в связи с наличием двойной связи.
Окисление алкенов преимущественно происходит при электрофильном присоединении к двойной связи атомов оксигенсодержащих групп, таких как группа гидроксильного при присоединении воды или группа карбонильного при присоединении алкена к алкену.
21 Каталитическое окисление
Каталитическое окисление алкенов происходит при непредельные, мягкое окисление, связей 21 числа алкена. При этом перманганатом числа воды окисление связи этом воду между высокими числа данной π-связи реакция π-равномерные окисления связи 21. Поэтому молекулах пропилена между π-связи присоединение воды структурное π-равномерное полимеризация образуются числа π-равномерные окисление π-равномерных молекул этена.
22 Мягкое окисление
Окисление этанола и алкенов происходит в кислой среде. Подвергаясь мягкому окислению, молекулы этанола разрывают свою связь с помощью катализаторов, таких как кислород, диоксид марганца или калия перманганата. При этом образуется уксусная кислота.
При мягком окислении алкенов, например, молекул этолена, происходит присоединение молекул воды с образованием алкоголя. Этиловый спирт образуется при взаимодействии между молекулами этена и молекул воды при каталитическом присоединении.
Мягкое окисление также может происходить при замещении галогенированием. Например, этан может быть ожидаемо замещен фтором в результате реакции между этаном и фтором.
Мягкое окисление окисляет молекулы углеводородов, таких как этан или алкены, с образованием уксусной кислоты или спирта. Число атомов кислорода, которые присоединяются к молекуле углеводородов, может быть от 2 до 12.
При окислении воды преимущественно происходят реакции между окислителем и тавшим. Окисление воды образует углекислый газ и воду. Например, при жестком окислении этолена, атомы углерода разрывают свои связи, образуя кислород и этен.
22 Жесткое окисление
Жесткое окисление представляет собой химическую реакцию, в ходе которой происходит окисление молекул емкости атома кислорода (О). В результате такого реакции на поверхности атома образуются активные радикалы, способные присоединиться к другим молекулам и изменить их свойства.
Жесткое окисление может происходить при наличии катализаторов, которые ускоряют химическую реакцию. Например, при нагревании железных или медных катализаторов происходит окисление этилена, образуется углекислый газ и вода:
| Вещества | Уравнение реакции |
|---|---|
| Этилен | C2H4 |
| Кислород | O2 |
| Углекислый газ | CO2 |
| Вода | H2O |
Жесткое окисление может также происходить без использования катализаторов при воздействии света или нагревании. Например, при прямом освещении или нагревании хлорированного этилена происходит присоединение молекулы хлора к двойной связи этилена:
| Вещества | Уравнение реакции |
|---|---|
| Этилен | C2H4 |
| Хлор | Cl2 |
| Хлорированный этилен | C2H4Cl2 |
Жесткое окисление может протекать и в других реакциях. Например, при окислении пропилена, образуется пропиленоксид:
| Вещества | Уравнение реакции |
|---|---|
| Пропилен | C3H6 |
| Кислород | O2 |
| Пропиленоксид | C3H6O |
Жесткое окисление может протекать и в других реакциях, которые представляют собой присоединение молекулы кислорода к двойной или тройной связи веществ. Например, при окислении непредельных углеводородов происходит образование кетонов:
| Вещества | Уравнение реакции |
|---|---|
| Хлорированный углеводород | CnH2n+2 |
| Кислород | O2 |
| Кетон | CnH2nO |
23 Горение алкенов
Кроме того, горение алкенов может происходить и в других условиях. При жестком горении алкена в свету его молекулы окисляются вентилейнерсумом калия, и в результате образуется ацетилен. Этот процесс обычно сопровождается ярким светом и высвобождением большого количества тепла.
Кроме того, в горении алкенов участвует и кислород. Примером такой реакции может быть горение этилена (С2H4), в результате которого образуется углекислый газ и вода:
С2H4 + 3O2 = 2CO2 + 2H2O
3 Замещение в боковой цепи
Замещение в боковой цепи этилена имеет особое значение, так как это приводит к образованию различных функциональных групп и, следовательно, к изменению свойств этого вещества. В боковых цепях этана, этилена и других углеводородов могут присутствовать различные группы атомов. Например, в случае этена (этилена) H2C=CH2, карбоновые атомы соединены между собой двойной связью. Если в боковой цепи алкена имеется только один атом водорода, то возможно его замещение, такого рода вещества можно подвергать гидрированию, образуя молекул H2O воды. Если атомов водорода в боковой цепи больше одного, то могут образовываться дополнительные соединения с водой, например, гидратацией алкенов.
Одной из наиболее важных реакций присоединения в алкенах является гидратация, при которой к нему присоединяется молекула воды. Гидратация происходит при нагревании алкена в воде в присутствии каталитического количества кислоты или щелочи. В результате гидратации молекулы воды добавляются к молекуле алкена, образуя гидрат.
Еще одной важной реакцией замещения в боковой цепи алкенов является окисление. Алкены могут подвергаться окислению различными окислителями, включая калия перманганат (KMnO4). В результате окисления алкена образуются кетоны или карбоновые кислоты, в зависимости от условий реакции.
Также возможно замещение боковой цепи алкена при хлорировании или бромировании. В результате электрофильного присоединения молекулы галогена к алкену образуются галогеналканы.
В боковых цепях могут образовываться и более сложные фрагменты, например, полимеры при полимеризации алкенов. Полимеризация происходит путем образования связей между молекулами алкена.
4 Изомеризация алкенов
Изомеризация алкенов может происходить по различным механизмам. Одним из таких механизмов является переключение двойной связи на другой участок молекулы. При этом происходит перераспределение электронной плотности и образование новых изомеров.
Изомеризация алкенов может протекать в разных условиях. Например, при взаимодействии с водой в кислой среде, этилен может изомеризироваться в присутствии катионов перманганата. В результате этой реакции образуются два изомера ацетальдегида — метилвинилкетон и 2-гидроксиэтилформиат.
Еще одним примером изомеризации алкенов является реакция преобразования непредельных алкенов в боковой кетон. При этом происходит разрыв двух связей С-С, присоединение кислорода и образование кетоновой группы. Такая реакция может протекать как по правилу Марковникова, так и по правилу Зайцева.
Изомеризация алкенов также может происходить при гидратации алкенов. При этом происходит присоединение молекулы воды к двойной связи алкена, образуя гидроксил-группу и образующийся карбонильный фрагмент. Гидратация может протекать как под действием кислоты, так и под действием основания.
Многие из этих реакций находят применение в синтезе органических соединений, поскольку позволяют получать различные изомеры алкенов. Изомеры алкенов имеют разные физические и химические свойства, что дает возможность использования их в различных процессах и реакциях.
Видео:
Горение этилена
Горение этилена by paramitacenter 11,432 views 12 years ago 40 seconds