- Взаимодействие этиленгликоля с бромной водой: особенности и результаты расщепления.
- Этиленгликоль химические свойства и получение
- Строение этиленгликоля
- Водородные связи и физические свойства спиртов
- Химические свойства этиленгликоля
- 11 Взаимодействие с раствором щелочей
- Видео:
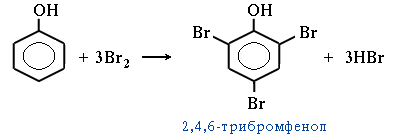
- Взаимодействие фенола с бромной водой
Взаимодействие этиленгликоля с бромной водой: особенности и результаты расщепления.
Этиленгликоль (C2H6O2) – это один из наиболее известных гликолей, широко используемый в промышленности. Его молекулярная структура состоит из двух гидроксильных групп, связанных между собой метиловым мостиком. Этиленгликоль обладает уникальными физическими и химическими свойствами, которые делают его ценным сырьем для многих процессов и реакций.
Одной из таких реакций, в которых этанол взаимодействует с бромной водой, является этерификация. При этой реакции этиленгликоль претерпевает взаимодействие с этерифицирующим агентом, например, с раствором бромной воды (Br2/12Н2О). В результате этого взаимодействия образуются сложные эфиры, содержащие щелочноземельные и водородные связи.
Окисление этиленгликоля присутствует во многих химических реакциях. Например, растворы хрома (Температура 22 — 24 °C) могут образовывать водные и сложные оксиды. При окислении с присутствием катализатора — хрома, этанол окисляется в ацетальдегид, а затем в уксусную кислоту.
Дегидрирование этиленгликоля может происходить при взаимодействии с щелочными и металлическими гидроксидами при повышенных температурах. При этом образуются окислительные соединения, которые после реакции гидролизируются в воду. Важной особенностью этого процесса является необходимость присутствия катализатора — меди.
Этиленгликоль химические свойства и получение
Он обладает рядом химических свойств, которые определяют его реакционную способность. В присутствии катализатора и кислорода он может окислиться до образования многоатомных кислородсодержащих соединений. Например, при окислении этаниленгликоля образуется сложное соединение, содержащее 11 атомов кислорода.
Одной из основных реакций этаниленгликоля является его дегидрирование. Оно может происходить как с помощью щелочных металлов, так и с помощью гидрирования. В результате дегидратации образуется ацетальдегид, а из него затем получают различные продукты.
Этиленгликоль также может взаимодействовать с водой, образуя раствором оксида этаниленгликоля. В этом случае реакция протекает с участием катализатора — водородного фторида. В результате образуется гидроксид этиленгликоля, который может быть дополнительно окислен до ацетальдегида аммиаком в присутствии кислорода и оксирование.
Этиленгликоль реагирует с щелочными гидроксидами (например, натриевым или калиевым) с образованием ацетата этаниленгликоля. Эта реакция протекает в щелочной среде, а реагентами служат соответствующий щелочной гидроксид и этаниленгликоль. Реакция возможна протекать только в присутствии специальных условий, например при высокой температуре и давлении.
Физические свойства этаниленгликоля также определяют его химическую активность. Он хорошо растворяется в воде и спиртах, образуя стабильные растворы. В воде и спирте он образует гидраты, что может использоваться в некоторых процессах.
Таким образом, этаниленгликоль обладает разнообразными химическими свойствами и может применяться в различных реакциях. Его получение осуществляется путем окисления соответствующего алкена или дегидратации соответствующего гликоля. Различные реагенты и условия приводят к образованию различных соединений, что позволяет использовать этаниленгликоль в широком спектре применений.
Строение этиленгликоля
H | H - C - C - H | H |
| Структурная формула этиленгликоля |
Строение этиленгликоля имеет сложные химические свойства. Благодаря присутствию гидроксильных групп, этиленгликоль образует соединения с другими веществами, включая карбонильные соединения, оксиды металлов и щелочные растворы. Он также реагирует с галогеноводородами, образуя замещенные этиленгликоли.
Этиленгликоль является хорошим растворителем для многих органических соединений, так как он способен образовывать водородные связи с молекулами других веществ. Взаимодействие этиленгликоля с водой и щелочными растворами приводит к образованию сложных полиэтиленгликольных соединений.
Этиленгликоль может быть использован в качестве катализатора реакций, таких как дегидрирование, гидрирование и дегидратация. Например, этиленгликоль может быть использован для получения этаниленгликоля путем гидролиза в присутствии меди и щелочных растворов.
Строение этиленгликоля также позволяет ему образовывать комплексные соединения с металлами, например, с медью и хромом. Такие соединения имеют мягкое и жесткое строение, и могут использоваться в различных областях, включая каталитические процессы и производство полимеров.
Водородные связи и физические свойства спиртов
Водородные связи — это слабые химические связи между атомом водорода в гидроксильной группе и электроотрицательным атомом (кислородом, азотом или фтором) в другой молекуле. Вспомогательные водородные связи образуются между атомами водорода и электроотрицательными атомами внутри той же молекулы. Образование водородных связей приводит к повышению кипения и плотности спиртов, так как они препятствуют движению молекул.
Спирты образуют водородные связи как между собой, так и с молекулами других веществ. Например, при взаимодействии этиленгликоля с водой образуются водородные связи между атомами водорода в гидроксильной группе этиленгликоля и атомами кислорода в молекуле воды. Это объясняет его растворимость в воде.
Водородные связи также могут влиять на химические реакции спиртов. Например, этаниленгликоль реагирует с бромной водой, при этом происходит окисление гидроксильной группы и образуется оксид этаниленгликоля. Спирты могут дегидрироваться в присутствии кислорода или щелочей-гидроксидов, образуя алкены.
Физические свойства спиртов определяются их способностью образовывать водородные связи и взаимодействовать с другими соединениями. Спирты обычно имеют более высокие температуры кипения и плотности по сравнению с соответствующими алканами, так как образование водородных связей делает молекулы спиртов более компактными. Например, этанол (CH3CH2OH) имеет температуру кипения 78 °C, в то время как этан (CH3CH3) -38.7 °C.
Также водородные связи влияют на растворимость спиртов в воде и других растворителях. Спирты хорошо растворимы в воде, особенно маломолекулярные спирты, благодаря возможности образования водородных связей с молекулами воды. Растворимость может зависеть от длины углеродной цепи в молекуле спирта и присутствия функциональных групп.
Итак, водородные связи являются важными для понимания физических свойств и реакций спиртов. Они влияют на горение спиртов (реакция с кислородом) и эффективность их окисления — спирты можно окислить до соответствующих карбонильных соединений, например, при взаимодействии с кислородом или хрома(VI) оксидом.
Химические свойства этиленгликоля
Одним из химических свойств этиленгликоля является его способность к образованию эфиров. В реакции с карбоновыми кислотами происходит эстерификация, в результате которой образуются эфиры. Используя оксиды щелочных металлов, можно получить щелочные соли этиленгликоля, обладающие высокой растворимостью в воде.
Этиленгликоль также образует сложные эфиры с металлами — в результате реакции с спиртами. Кислородные атомы этиленгликоля образуют связи с металлом, а водородные атомы замещаются эфирной группой.
Взаимодействие этиленгликоля с галогеноводородами приводит к образованию соответствующих дигалогеналканов. При этом происходит замена одного или двух водородных атомов этиленгликоля на атомы галогена.
Бромная вода реагирует с этиленгликолем, образуя оксид бромистого(III) и воду. При этом происходит дегидрирование этиленгликоля до образования оксида бромистого(III).
Этиленгликоль способен окисляться в присутствии кислорода до образования оксида этадиена(IV), который при гидрировании превращается в этилентанедиол и, в конечном итоге, в этанол.
При гидрировании этиленгликоля получают гликоль, а при горении – углекислый газ и воду. Также этот спирт реагирует с щелочами, образуя соли этиленгликоля, в результате гамования связи этерного атома с оксигруппой.
Хрома реагирует с этиленгликолем, образуя сложное соединение. Этиленгликоль также подвергается гидролизу в щелочной среде, превращаясь в более простые соединения – метанол, гликольевую кислоту и ацетон. Это может быть полезным в некоторых химических процессах и синтезах.
11 Взаимодействие с раствором щелочей
При взаимодействии с растворами щелочей также может происходить гидрирование этиленгликоля с образованием сложных соединений. В этом случае молекула этанола вступает в реакцию с основание, образуя сложную молекулярную структуру.
Кроме того, при взаимодействии с растворами щелочей происходит дегидратация этиленгликоля. В результате этой реакции из молекулы этиленгликоля удаляется водная группа, что приводит к образованию драгоценного эфира.
Также щелочи могут окислить этиленгликоль при наличии катализатора, таких как щелочные металлы. При этом происходит образование органических кислородных соединений, например, карбоновых кислот.
Одним из особых свойств этиленгликоля при взаимодействии с растворами щелочей является его способность образовывать водородные связи с молекулами воды. Такие водородные связи могут быть слабыми, мягкими или же жесткими.
Взаимодействие этиленгликоля с растворами щелочей происходит с образованием сложных структур, связей и соединений, которые обладают различными физическими и химическими свойствами.
Видео:
Взаимодействие фенола с бромной водой
Взаимодействие фенола с бромной водой by Органическая химия 25,651 views 7 years ago 49 seconds