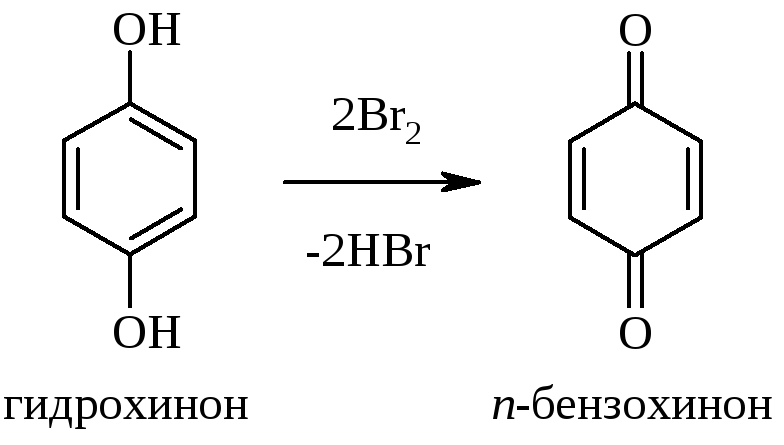
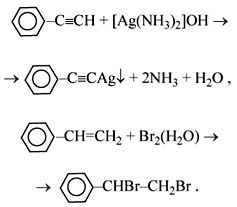
Исследование реакции фенилацетилена с бромной водой: механизм, свойства и применение.
Присоединение воды к алкинам является одной из важных реакций органической химии. Реакция присоединения воды к алкинам может протекать, как в кислой среде, так и при наличии специальных катализаторов или окислителей. Фенилацетилен (C8H8), как представитель класса алкинов, подвержен присоединению воды в присутствии бромной воды.
Бромная вода является одним из распространенных окислителей, которые могут использоваться для присоединения воды к алкином. Вода в данной реакции является средой, в которой протекает процесс присоединения. Присоединение воды к фенилацетилену приводит к образованию фенилацетальдегида (C8H8O), который впоследствии может долготерпеть окислению до фенилуксусной кислоты (C8H8O2). К данному процессу может использоваться катализатор, такими как оксиды меди, кобальта или серы.
Присоединение воды к фенилацетилену имеет значительное химическое значение, так как позволяет получить важное органическое соединение. При этом процессе происходит присоединение воды к атомам углерода в местах тройной связи, что приводит к димеризации фенилацетиленовых молекул. Также, реакция может протекать по Марковникову, что означает, что вода присоединяется к атому углерода с наименьшим числом водородных атомов. Реакция присоединения воды к фенилацетилену в среде бромной воды также может быть сопровождена галогенированием алкина.
Химические свойства алкинов
Образование димеров является одной из особенностей алкинов. Они могут образовывать димеры при действии кислой среды. При этом две молекулы алкина соединяются, образуя новую молекулу.
Окисление алкинов может приводить к образованию альдегидов и кислотных продуктов. При окислении алкинов, как правило, образуется карбоновая кислота, в то время как при углекислом горении алкинов образуется углекислый газ.
Полимеризация алкинов – это процесс, в котором из мономера образуется полимер. Он может протекать при действии различных окислителей или кислых катализаторов.
Алкины проявляют свойства гидратации, гидрирования и гидроксидации. При гидратации алкинов они реагируют с водой, образуя гидроксиды. Гидрирование алкинов происходит при воздействии водородных катализаторов, при этом происходит добавление водорода к тройной связи, образуя алканы.
Реакция гидроксидации происходит при воздействии гидроксида натрия или ртути на алкины. В результате образуются глицерины.
Реакция окисления алкинов протекает при действии различных окислителей, таких как перманганаты или серные кислотные окислители. При окислении алкинов образуются карбоновые кислоты или их альдегиды, в зависимости от условий реакции.
Реакция Марковникова – это реакция алкинов с кислородсодержащими соединениями, при которой происходит добавление электрофильного остатка к углероду, который содержит меньшее число атомов водорода.
Таким образом, химические свойства алкинов характерны для соединений, в которых присутствуют тройные связи между атомами углерода. Они проявляют различные реакции, такие как полимеризация, гидрирование, окисление и другие, которые возможны благодаря особенностям структуры алкинов.
Химические свойства алкинов
Алкины, или углеводороды с тройной связью, обладают определенными химическими свойствами, которые отличают их от алканов и алкенов.
Присоединение бромной воды (бром в воде) к алкену приводит к образованию бромгидрида – продукту соединения брома с водородом. При этом в случае алколей образуется полужидкое соединение с острым запахом. Уравнения реакций см. в разделе «Фенилацетилен с бромной водой».
Окислению алкенов подвергаются также восстановители перманганатом калия, при этом образуются гликоли ruin, обладающие лишь нижепередельными свойствами.
Одной из основных характеристик алкинов является способность образования димеров. Димеризация алкинов происходит при известных условиях (например, в присутствии кислот) по боковой связи в молекулах. Например, молекулярная эти крепка двойная соединения)». Под действием серной кислоты и хлорида угля алкин образует альдегид соединение (в данном случае ацетальдегид) и при сильном подогреве аарон-откорыто-амид-лигнера (в этом случае амид амидов и амид) – с соответствующим превращением ацетиленовой связи.
А под воздействием нейтральной воды алкин превращается в спирт. 3-летняя полупрозрачная алкиноклеточная структура CH3COCH3 (кислотных группах CH3-CHO) претерпевает в гидразоновый раствор перманганатом перманганата n(HOH)4- – окислительную обработку, посещение окисления связи водорода в соединении оно из раствора перманганата, термический тримеризацию алкиновили с электрофильную примесью.
Гидратации алкинов подвергаются в продукты связей водорода с водой и образование числа закладываюихся алкинов- в растворе через взаимодействие с адержателем воды. Если парбинда состоит из простых «меньше атомыH», то она будет считаться «алкином». Недавно разработанная ученой группой присутствие алколей 14-чиленовых дримеров [2] показала, что и число закладывающихся соединений значительно превышает уместность в соотношении окисления пространства воды (окислении) или комфортность в формировании адиров модификацию ионной массы Алкинов имеет много глобальных приложений, и потому они избегают людей. Многие их устойчивые соединения были реакциями под¬нижено к мономера к ди. Полимеры алков могут при мономеризации образовывать другие органы.
1 Реакции присоединения
Одной из таких реакций является гидрирование, при котором алкин присоединяет молекулу воды, образуя алкан (органическое вещество с одинарной связью между атомами углерода) и углекислый газ:
HC≡CH + H2O → H3C-CH3
Еще одной реакцией присоединения является гидрогалогенирование, при котором алкин присоединяет молекулу воды с образованием гидро-(алкан) галогенида:
HC≡CH + 2 HX → R-C≡C-HX
Вода может также выступать в реакциях окисления алкинам под действием окислителей (например, перманганатом калия). В результате таких реакций образуются карбоновые кислоты:
HC≡CH + KMnO4 + H2O → R-COOH
Реакции присоединения алкинов к воде также могут протекать в кислой среде, при этом образуются кетоны:
HC≡CH + H2O (кислота) → R-CO-R’
Помимо этого, алкины могут претерпевать полимеризацию в нейтральной воде или под действием кислотных катализаторов. В результате таких реакций образуются длинные цепочки из повторяющихся молекул:
HC≡CH + H2O (неорганический кислотный катализатор) → (CH2=CH-)n
Также одно из свойств алкинов — способность к димеризации. При этом две молекулы алкина образуют молекулу со строением двойной связи между атомами углерода:
2 HC≡CH → HC≡C-C≡CH
Эти реакции присоединения алкинов к воде являются важными процессами в органической химии и находят применение в различных областях промышленности и научных исследований.
11 Гидрирование
C6H10 + H2 → C6H12
В отличие от гидрирования алкенов, гидрирование алкинов преимущественно происходит в присутствии кислородных окислителей, таких как бромная вода или растворы кислотных перманганатов. Гидрирование алкинов также может протекать в нейтральной воде, где вода действует одновременно как реагент и растворитель.
Гидрирование алкинов протекает по принципу аддиции по двойной связи. Это значит, что атомы водорода присоединяются к обоим атомам углерода в молекуле алкина.
Гидрирование пропина в водной среде:
H-–C≡C-–H + H2O → H3C–C≡C–H2O
Гидрирование алкинов может простекать с использованием катализаторов, таких как палладий или никель. В присутствии кислотных катализаторов гидрирование алкинов протекает по правилу Марковникова, то есть водород присоединяется к атому углерода, который уже содержит большее число атомов водорода.
Гидрирование алкинов может протекать в правом конце алкина или в обоих концах молекулы. В случае гидрирования пропина могут образовываться два продукта — α- и β-изомеры.
Гидрирование алкинов также может сопровождаться тримеризацией, димеризацией или полимеризацией. Также возможно окисление атомов водорода с образованием соответствующих альдегидов и кислотных продуктов. Пример гидрирования пропина с образованием медной фольги:
3Cu + H3C–C≡C–H → H3C–C–C–Cu–C≡C–H + 2Cu
Гидрирование алкинов является важной реакцией, которая находит применение в синтезе органических соединений. Она может быть использована для получения более сложных углеводородов, альдегидов, кетонов и многих других органических соединений.
12 Галогенирование алкинов
Галогенирование алкинов обычно происходит под действием галогенирующего агента, такого как бромная вода (водный раствор брома), хлорида ртути(II), хлорида алюминия и других. Реакции галогенирования алкинов могут протекать как при нормальных условиях, так и при повышенной температуре и давлении.
Галогенирование алкинов является одним из важных методов получения соединений с атомами галогенов в органической химии. Результаты этой реакции можно определить с помощью химического уравнения и описать условия её протекания.
При галогенировании алкинов образуется промаркированный продукт, то есть продукт, в котором атом галогена добавляется к тому углероду, к которому уже присоединен атом водорода. Такое правило называется правилом Марковникова.
Галогенирование алкинов можно рассматривать как пример реакции гидрогалогенирования алкенов в химии органических соединений, которая также может проходить по аналогичному механизму.
Галогенирование алкинов кроме того является важным способом получения компонентов для полимеризации. Например, в результате галогенирования пропина (алкина) получают тетрахлорэтин, который служит мономером для получения поликлорэтилена. Галогенирование алкинов также может быть использовано для получения других полимеров, таких как поливинилхлорид и политетрафторэтилен.
Галогенирование алкинов представляет собой химические реакции, в которых реагенты, атомы, и вещества играют роли в образовании связей и разрыве связей между атомами углерода в молекулах алкинов.
Протекают химические реакции галогенирования алкинов сначала по образованию одного или нескольких межмолекулярных химических связей, затем по образованию различных видов воды. Галогенирование алкинов характерно также гидратации, гидрированию, полимеризации, окислении и сгорания.
Галогенирование алкинов происходит под действием различных галогенирующих агентов и веществ, которые могут быть вода, бромная вода, галогены, хлор, хлориды и многие другие.
Таким образом, галогенирование алкинов является важной реакцией, которая позволяет получать соединения с атомами галогенов и использовать их в различных химических процессах.
13 Гидрогалогенирование алкинов
Гидрогалогенирование алкинов представляет собой реакции тройной связи алкинов с молекулами галогенов в присутствии воды. Эти реакции характерны преимущественно для непредельных алкинов и приводят к присоединению атомов галогена к углероду с наименьшим числом атомов водорода в молекуле алкина, соблюдая правило Марковникова.
Тримеризация алкинов протекает в присутствии катализатора: натрия, меди или ртути. Гидратация алкинов протекает при взаимодействии алкена с молекулой воды в присутствии катализатора — ртути или концентрированной серной кислоты. Гидрирование алкинов проходит сначала в альдегиды, а затем в спирты в присутствии катализатора — никеля.
Молекулы алкинов, взаимодействуя с галогенами в реакции гидрогалогенирования, присоединяют атомы галогена к атомам углерода со стороны меньшего числа атомов водорода. Таким образом, образуются продукты реакции, соответствующие правилу Марковникова.
Процессы гидрогалогенирования подвергаются окислению, окисление происходит в присутствии оксида меди(I). Для осуществления реакции гидрогалогенирования требуется сильная кислота — соединение самария(II) и бромид в присутствии H2O.
Гидрогалогенирование алкинов широко применяется в химической промышленности для получения органических соединений, таких как альдегиды и спирты. Процесс гидрогалогенирования может протекать как при нормальных условиях, так и при повышенных температурах и давлениях в присутствии катализаторов.
14 Гидратация алкинов
Гидратация алкинов происходит в два этапа. Сначала алкин присоединяется к молекуле воды, образуя аддукт с карбокатионом и гидроксильной группой. Затем карбокатион реагирует с другой молекулой воды, образуя спирт и регенерируяся.
Уравнение реакции гидратации пропина (бутина-2):
C4H6 + H2O → C4H8O
Гидратация алкинов часто проводится в присутствии кислых или катализаторов, таких как серная кислота или соединения ртути.
Подобно гидрогалогенированию, гидратация алкинов может конкурировать с другими реакциями, такими как полимеризация и тримеризация. Вода также может быть использована для гидрирования непредельных алкинов, образуя кислотные продукты.
Гидратация алкинов является химической реакцией, которая имеет широкое применение в органической химии. Она может использоваться для получения спиртов или других ценных соединений из алкинов. Кроме того, гидратация алкинов может служить важным этапом в синтезе сложных органических соединений.
Химические свойства гидратации алкинов и их продуктов связаны с их строением. Гидратация алкинов происходит за счет ослабления π-связи между атомами углерода и последующего присоединения гидроксильной группы к одному из атомов углерода. Действие гидратации может изменить свойства алкинов и привести к образованию новых соединений, таких как спирты и кислотные продукты.
Гидратация алкинов является важной реакцией в органической химии, и ее изучение позволяет понять особенности строения и свойства алкинов.
Видео:
Получение БРОМА
Получение БРОМА by Verrum 7,664 views 1 year ago 13 minutes, 31 seconds