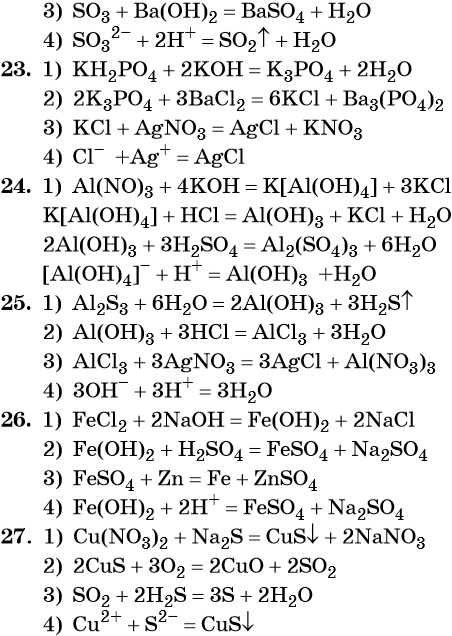- Реакция растворения фосфата кальция в воде: уравнение и особенности
- Фосфат кальция
- Характеристики и физические свойства фосфата кальция
- Получение фосфата кальция
- Химические свойства фосфата кальция
- Применение фосфата кальция
- Медицина
- Пищевая промышленность
- Сельское хозяйство
- Производство
- Видео:
- Реакции ионного обмена.
Реакция растворения фосфата кальция в воде: уравнение и особенности
Фосфат кальция (Ca3(PO4)2) — это важное химическое соединение, которое широко применяется в различных областях, включая медицину, сельское хозяйство и строительство. Получение фосфата кальция осуществляется путем реакции между фосфоритом или апатитом и кислотами в химической лаборатории или промышленности.
Фосфат кальция существует в двух модификациях: α и β. α-модификация является твердым соединением с сингонией элемента, в то время как β-модификация имеет более сложную кристаллическую структуру. Оба вида фосфата кальция обладают различными характеристиками и свойствами.
Описание краткой характеристики фосфата кальция в водных растворах заключается в его низкой растворимости. Это свойство делает его неподходящим для использования во многих химических реакциях и решении задач. Однако, фосфат кальция может быть полезной солью ортофосфорной кислоты в различных областях.
Уравнение реакции между фосфатом кальция и водой выглядит следующим образом: Ca3(PO4)2 + 3H2O = 3Ca(OH)2 + 2H3PO4. В химической лаборатории это уравнение используется для определения концентрации фосфата кальция в растворах с помощью различных методов анализа.
Плотность фосфата кальция составляет около 3 г/см³, а его молярная масса — примерно 310 г/моль. Минералы фосфата кальция, такие как апатит или гидроксиапатит, являются основными составными частями костей и зубов, обеспечивая им прочность и устойчивость.
Фосфат кальция
Формула фосфата кальция представляет собой соединение трех кальциевых и двух ортофосфорных групп. Он является кристаллическим веществом с плотностью, характерной для солей.
Фосфат кальция является главным компонентом апатита, который в свою очередь представляет собой основное минеральное соединение в зубах и костях. Гидроксиапатит, в свою очередь, является основным компонентом костной ткани.
Уравнение реакции фосфата кальция с водой (H₂O) можно представить следующим образом:
Ca₃(PO₄)₂ + 3H₂O → 3Ca²⁺ + 2PO₄³⁻ + 6OH⁻
При этом реакция происходит при высоких температурах.
Фосфат кальция имеет различные химические и физические характеристики. Он обладает высокой устойчивостью к разложению и растворению, что делает его широко используемым в промышленности. В частности, фосфат кальция применяется в производстве лекарственных препаратов, удобрений, косметических средств, а также в пищевой промышленности.
Описанный выше фосфат кальция, также известный как апатит, может находиться в разных α-модификациях, каждая из которых имеет свои характеристики и свойства.
Получение фосфата кальция может осуществляться различными способами. Например, можно использовать реакцию растворения оксида кальция (CaO) в растворе ортофосфорной кислоты (H₃PO₄) или реакцию между растворами кальция и фосфата.
Для рассчета количества фосфата кальция, получаемого в реакции, можно использовать соотношение между массами реагентов и молярной массой соединения.
Примеры характеристик и свойств фосфата кальция:
- Масса фосфата кальция зависит от количества использованных реагентов и метода получения.
- Фосфат кальция обладает высокой плотностью и может иметь различные кристаллические формы.
- Он является химически стабильным веществом и обладает высокой устойчивостью к разложению и растворению.
- Фосфат кальция широко используется в медицине, пищевой и химической промышленности.
Таким образом, фосфат кальция является важным химическим соединением со множеством применений и характеристик.
Характеристики и физические свойства фосфата кальция
Фосфат кальция имеет ряд физических свойств и химических характеристик, которые определяют его применение и взаимодействие с другими соединениями:
| Свойство | Описание |
|---|---|
| Температура плавления | Ортофосфат кальция плавится при температуре около 1670 °C. |
| Плотность | Плотность фосфата кальция составляет примерно 3,14 г/см³. |
| Форма | Фосфат кальция может быть представлен в виде твердой сингонии. |
| Взаимодействие с кислотами | Фосфат кальция может растворяться в кислотах, образуя раствор. |
| Физическое состояние | Фосфат кальция находится в твердом состоянии при комнатной температуре. |
Другими формами фосфата кальция являются оксиды кальция и фосфора, а также соли фосфорной кислоты. Основным источником фосфата кальция является минерал апатит, который содержит его в своем составе. Фосфат кальция также используется в различных промышленных процессах и в качестве добавки в пищевых продуктах.
Для решения задач, связанных с фосфатом кальция, можно использовать молярную массу этого вещества, уравнение реакции и рассчитать концентрацию раствора фосфата кальция в заданном растворителе. Примеры реакций, в которых участвует фосфат кальция, включают реакции с кислотами и хлоридами.
Фосфат кальция обладает широким спектром применения. Он используется в производстве керамики, стекла, удобрений, косметики, фармацевтики и многое другое. Также он находит применение в медицине для лечения костных заболеваний и восстановления костной ткани.
Получение фосфата кальция
Фосфат кальция можно получить различными способами. Одним из основных методов получения является реакция фосфора с водой, при которой образуется ортофосфат кальция:
P + 5H2O → 3H3PO4
Ортофосфат кальция можно превратить в другие формы фосфата кальция, такие как гидроксиапатит (основный компонент костей и зубов) путем добавки внешнего источника кальция, такого как гидроксид кальция:
H3PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 3H2O
Фосфат кальция также может быть получен из природных источников, таких как фосфориты. Например, реакцией фосфорита с кислотами можно получить фосфат кальция:
Ca3(PO4)2 + 2H3PO4 → 3Ca(H2PO4)2
Основными фосфатами кальция являются α-модификация и β-модификация, которые различаются по своим кристаллическим структурам. В химических формулах кальция фосфат присутствует в виде Ca3(PO4)2.
Молярная масса фосфата кальция составляет примерно 310,18 г/моль, а его плотность составляет около 3,14 г/см³. В зависимости от температуры и условий реакции, можно получить различные формы и структуры фосфата кальция. Термическое разложение фосфата кальция приводит к получению кальция и фосфора в виде Павера:
Ca3(PO4)2 + 6Ca → 3Ca2P2 + 5O2
Таким образом, фосфат кальция — это важное химическое соединение, которое может быть получено различными способами, и имеет широкий спектр применения как добавка в пищу, лекарственное средство и вещество, используемое в различных промышленных отраслях.
Химические свойства фосфата кальция
Фосфат кальция обладает следующими химическими свойствами:
| Формула | Ca3(PO4)2 |
| Состояние | Твердое вещество |
| Плотность | 3,14 г/см³ |
| Сингония | α-модификация и β-модификация |
Фосфат кальция является основным компонентом минерала апатита, который является основным источником фосфатов для получения фосфата кальция.
Фосфат кальция растворяется в кислотах, в результате чего можно получить растворимые соли фосфорной кислоты:
Ca3(PO4)2 + 6HCl → 2H3PO4 + 3CaCl2
Фосфат кальция может быть получен путем взаимодействия гидроксиапатита (Ca5(PO4)3(OH)) с хлоридом кальция (CaCl2):
5Ca5(PO4)3(OH) + 8CaCl2 → 12Ca3(PO4)2 + 13H2O + 8HCl
Фосфат кальция также может быть получен путем обработки ортофосфата кальция (Ca(H2PO4)2) оксидом кальция (CaO):
Ca(H2PO4)2 + CaO → Ca3(PO4)2 + H2O
Фосфат кальция обладает примечательными химическими свойствами, такими как низкое растворимость в воде и стабильность при нормальных условиях температуры и давления.
Примеры применения фосфата кальция включают использование его в производстве удобрений, в смывных и жидкостных системах для удаления фосфатов, а также в промышленности для производства фосфорной кислоты и фосфатных солей.
Применение фосфата кальция
Медицина
Наиболее известным применением фосфата кальция является его использование в медицине. В виде β-модификации, фосфат кальция применяется в качестве протезного материала для пополнения дефектов костей при переломах, остеопорозе и других заболеваниях костей. Кроме того, он используется как ингредиент в некоторых стоматологических пастах и зубных пудрах для укрепления и защиты зубной эмали.
Пищевая промышленность
Фосфат кальция используется в пищевой промышленности в качестве стабилизатора и загустителя. Он добавляется в различные продукты, включая молочные продукты, мороженое, кондитерские изделия и соусы, чтобы улучшить текстуру и увеличить срок годности.
Сельское хозяйство
Фосфат кальция является важным удобрением в сельском хозяйстве. Он обеспечивает растения необходимым количеством фосфора для их нормального роста и развития. Фосфат кальция также может использоваться для обработки кормов для животных, чтобы обеспечить их нужды в фосфоре и кальции.
Производство
Фосфат кальция используется в различных производственных процессах. Он может использоваться в качестве катализатора или ингредиента для производства различных химических соединений, таких как фосфорная кислота, фосфаты и хлориды. Также с его помощью можно получить β-модификации фосфата кальция.
В целом, применение фосфата кальция обширно и разнообразно. Это соединение обладает уникальными химическими и физическими свойствами, что делает его полезным в различных отраслях промышленности и науке.
Видео:
Реакции ионного обмена.
Реакции ионного обмена. by Наталья Журавлева 1,108 views 2 years ago 36 minutes