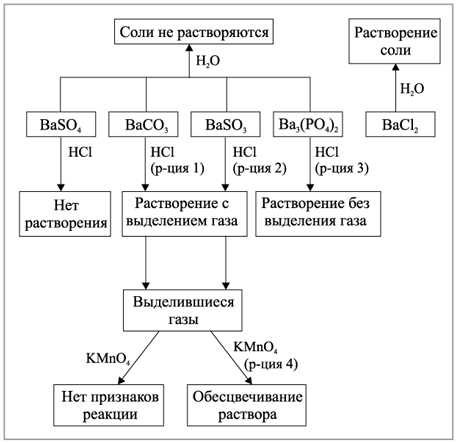
- Возможности газа для избавления от окрашивания бромной воды
- Газ обесцвечивающий бромную воду
- Тренажер задания 31 по химии серы
- Органическая химия
- Качественные реакции в органической химии
- Качественные реакции на алканы
- Качественные реакции на алкены
- Качественные реакции на алкины
- Качественные реакции на альдегиды
- Качественные реакции на спирты
- Видео:
- Пожарных затопило водой!
Возможности газа для избавления от окрашивания бромной воды
Одной из интересных реакций, изучаемой в химии, является взаимодействие газа с раствором бромной воды. Бромная вода, в свою очередь, представляет собой продукты взаимодействия брома с водой. Бром — один из химических элементов, а бромная вода — одна из его соединительных форм.
Взаимодействие газа с бромной водой происходит в виде химической реакции, в результате которой образуется продукт, обесцвечивающий бромную воду. В начальном состоянии раствор бромной воды имеет ярко-желтый или желто-коричневый цвет вследствие присутствия брома. При взаимодействии газа с раствором бромной воды происходит образование серной кислоты и сульфида серы.
Полученную в результате реакции бромную воду можно записать следующим образом: 2HBr + SO2 -> H2SO4 + H2S.
Задание заключается в определении состава исходного раствора при выполнении качественных химических реакций на образующееся взаимодействие с образовавшимся обесцвечивающим продуктом.
Газ обесцвечивающий бромную воду
Бромная вода, имеющая формулу HBrO, обычно имеет зеленоватую расцветку. Но при взаимодействии с определенными газами, оно обесцвечивается. Данная реакция основана на окислении газов кислородом, который присутствует в составе бромной воды.
Обесцвечивание бромной воды может быть вызвано алканами, аммиаком, серной кислотой и многими другими органическими соединениями. Для проверки наличия газа, способного обесцвечивать бромную воду, помещают ее в тренажер и поочередно вводят небольшие порции газов в присутствии бромной воды.
При реакции образуется газовая пузырьковая разновидность. В зависимости от газа, образующегося при взаимодействии с бромной водой, может быть полученный осадок и изменение цвета реакционной смеси. При обесцвечивании бромной воды газы поглощают в ней необходимые для них кислородные ионы, что приводит к обесцвечиванию их самих.
| Газ | Реагенты | Реакция |
|---|---|---|
| Аммиак | Бромная вода + аммиак | Образуется белый осадок амидных солей |
| Серная кислота | Бромная вода + серная кислота | Образуется серный газ и обесцвечивание реакционной смеси |
| Алканы | Бромная вода + алкан | Образование эфира и обесцвечивание реакционной смеси |
Таким образом, газ, обесцвечивающий бромную воду, может быть определен качественными реакциями, позволяющими выявить его наличие в органических соединениях. Это важный метод анализа в химии органических соединений.
Тренажер задания 31 по химии серы
В задании номер 31 по химии серы требуется исследовать реакцию, при которой образуется белый осадок. Для этого необходимо добавить воду к веществу, полученному в результате обжига серебряного сульфида, а затем поглотить выделившийся газ с помощью раствора бромной воды.
Сначала необходимо решить задание по составлению формулы. В результате обжига серебряного сульфида образуется сера и продукты горения органического вещества. Эти продукты обесцвечивают раствор бромной воды, содержащий органическую вещество. Формулы органических веществ, вступающих в реакцию, можно записать следующим образом: алкины, алкены или альдегиды.
В данном задании предлагается получить аммиачный раствор бромной воды. Для этого в раствор натрия цинка добавляется избыток аммиака. Полученный раствор образует осадок белого цвета, который обесцвечивает бромную воду.
После этого поглотите выделившийся газ с помощью раствора бромной воды и нагрейте полученную смесь. При этом цвет раствора изменится из желтого на белый.
В результате реакции будет образовано необходимое вещество, которое может быть использовано для получения качественных солей, эфира или других органических соединений.
Для написания уравнения необходимо знать следующие данные: цвет бромной воды до и после реакции, цвет раствора серы в воде, цвет органических соединений до и после обжига, а также вид и цвет осадка, образующегося в результате реакций с медным перманганатом.
В данном тренажере у вас есть возможность проверить свои знания и найти правильное решение задания номер 31 по химии серы.
Органическая химия
Органическая химия изучает свойства и реакции органических соединений, то есть соединений, содержащих углерод. В одном из заданий органической химии требуется изучить реакцию газа с бромной водой.
Бромная вода — это раствор брома в воде, который обладает характерным оранжево-красным цветом. Согласно реакции, описанной в задании, газ обесцвечивает бромную воду: пропускают через воду газ, полученный в результате реакции.
Для проведения реакции необходимы спирты. Взаимодействие бромной воды с спиртами приводит к образованию обесцвечивающего газа (активного хлора).
В процессе проведения эксперимента, газ сплавили с добавлением серебра. Сплавление газа с серебром потребовало взаимодействие раствора газа с серной кислотой. В результате взаимодействия образуются осадок и серная кислота.
Полученное вещество вычисляют по формуле, заданной в задании.
После вычисления, полученное вещество отделяют от раствора, просушивают соляной кислотой и проводят необходимые качественные реакции. Выпавший осадок в растворе будет фуксинсернистой кислотой.
Требуется также составить уравнение реакций в заданном порядке. Для этого избыток газа взаимодействует с гидроксидом серы, после чего выпавший осадок растворяется в воде и реагирует с серной кислотой.
Качественные реакции в органической химии
Органическая химия изучает взаимодействие молекул органических соединений. Важную роль в этом процессе играют качественные реакции, которые позволяют идентифицировать и дифференцировать органические соединения.
Один из интересных примеров таких реакций — обесцвечивание бромной воды. Газ, обладающий способностью обесцвечить бромную воду, получает название «газ обесцвечивающий бромную воду».
Для получения этого газа, обработали органическую фуксинсернистой кислотой, содержащей серу и серную кислоту. Раствор фуксинсернистой кислоты нагрели с избытком цинка в эфире и пропускали через него газы, полученные в результате горения алкинов.
Сущность данной реакции заключается во взаимодействии серной кислоты с кислородом воздуха, полученного в результате горения алкинов. В результате этой реакции образуется серный газ, который растворяется в воде и образует серную кислоту вместе с газовыми выделившимися веществами.
Таким образом, газ обесцвечивающий бромную воду представляет собой смесь газов, в которой присутствуют серный газ и другие газы, имеющие характерный запах. Пропуская эту смесь через бромную воду, происходит образование некоторых необходимых в данной задаче соединений.
Результатом пропускания газов через раствор бромной воды является обесцвечивание воды. Бромная вода, исходно имеющая красный цвет, становится белой.
| Вещество | Формула |
| Фуксинсернистая кислота | алкины |
| Бромная вода | Br2 |
| Сплавленный порошок цинка | Zn |
| Серная кислота | H2SO4 |
Качественные реакции на алканы
Качественные реакции на алканы записаны в химической литературе вследствие их важности в органической химии. При взаимодействии алканов с бромной водой (раствор брома в воде) происходит образование сложного серы, который приводит к обесцвечиванию раствора.
Когда алкан добавляется в бромную воду, происходит окислительное взаимодействие, в результате которого образуется оозонидная соль. Оозонидная соль обнаруживается по появлению бледно-желтого цвета раствора.
Другой качественной реакцией на алканы является взаимодействие с аммиачным серебром. При взаимодействии алканов с аммиачным серебром образуется осадок серебряного сульфида, который имеет темно-серый цвет. Это обесцвечивающая реакция, которая характерна для алканов.
Алканы также проявляют реакцию горения на воздухе или в присутствии кислорода. При горении алканов образуется углекислый газ и вода. Уравнение реакции горения алкана может быть записано следующим образом: алкан + кислород → углекислый газ + вода.
Другой качественной реакцией на алканы является их взаимодействие с кислотой хрома(VI). При этом образуется хромат атома алкена, который имеет ярко-желтый цвет. Эта реакция может быть использована для определения наличия алканов в органическом веществе.
Взаимодействие алканов с цинком и кислотой приводит к образованию аминов. Эта реакция также может быть использована для проверки наличия алканов в органических соединениях. Образующийся при реакции осадок цинка можно обнаружить по его серебристому цвету.
Качественные реакции на алкены
Одной из таких реакций является обесцвечивание бромной воды. Бромная вода имеет желтый цвет вследствие наличия брома в растворе. При взаимодействии с алкенами происходит реакция, в результате которой бром добавляется к двойной связи алкена:
Соединение + Br2 → Соединение-Br2
Таким образом, при добавлении бромной воды к алкену раствор становится бесцветным, а бром добавляется к алкену.
Еще одной качественной реакцией на алкены является реакция с серной кислотой. При реакции алкена с серной кислотой образуется сульфид алкена и вода:
Соединение + H2SO4 → Сульфид алкена + H2O
Реакция с серной кислотой является качественным тестом на алкены и позволяет их обнаружить. При этой реакции наблюдается образование сероводорода, который имеет характерный запах.
Кроме того, алкены могут реагировать с аммиачным реактивом. В результате реакции образуется аммония алкена, аммоний сульфид и вода:
Соединение + 2NH3 → Аммоний алкена + (NH4)2S + H2O
При этой реакции можно установить наличие алкена на основе образования аммонийного сульфида, который имеет ярко-желтый цвет.
Таким образом, качественные реакции на алкены позволяют их обнаружить и определить тип алкена. Различные реактивы, такие как бромная вода, серная кислота и аммиачный реактив, позволяют установить наличие алкена вследствие характерных изменений цвета или образования продуктов реакции, таких как сульфиды и аммонии.
Качественные реакции на алкины
Один из газов, который может осуществлять качественные реакции с алкинами, это газ обесцвечивающий бромную воду. Бромная вода в присутствии алкена обесцвечивается, что является результатом окисления алкенов кислородом. Это происходит благодаря реакции между бромной водой и алкеном. Бромной воде отделяется газ.
Для наглядности реакции приведена формула газа:
$$C2H2+Br2->C2H2Br2$$
В результате образуется дибромэтан. Такая реакция может использоваться в химическом тренажере для демонстрации процесса обесцвечивания бромной воды алкенами.
Кислота-реагент, которая может использоваться для проявления реакции, — это азотная кислота. Если алкены поместить в раствор азотной кислоты в присутствии H2SO4, то будет наблюдаться реакция окисления алкенов кислородом. В результате образуются нитроаэдилен и вода сульфата. Данная реакция записана в виде:
$$C2H2+HNO3->C2H2(NO2)2$$
Также качественные реакции на алкины включают взаимодействие соляной кислоты. В присутствии HCl возникает реакция аддиции, в результате которой образуются хлорированные продукты. Формула реакции записана как:
$$C2H2+HCl->C2H3Cl$$
Значительное количество газов может образовываться в реакциях между алканами и водородом. Так, в результате реакции между алканами и водородом образуется вода. Реакция записана как:
$$C2H2+2H2->C2H6$$
Также в результате горения алканов образуется углекислый газ и вода:
$$C2H2+5O2->4CO2+2H2O$$
Таким образом, алкены могут реагировать с различными реагентами, в результате чего образуются новые соединения. При этом образовавшиеся продукты могут иметь разнообразные свойства и состав в зависимости от реагента, используемого в реакции.
Качественные реакции на альдегиды
Обесцвечивающий бромную воду газ
Исходное вещество, обладающее обесцвечивающим свойством в бромной воде, имеет сложную органическую формулу. В результате взаимодействия с избытком серы и натрия в присутствии воды образуется сложный органический сульфид. Цвет бромной воды в этом случае изменяется с бурого на белый.
Для установления наличия альдегидов в органическом веществе исследуемое вещество обрабатывают раствором перманганата калия (KMnO4) в присутствии серной кислоты. Результатом взаимодействия является окисление альдегидов до кислоты и образование безцветного раствора.
Если же альдегидов в исследуемом веществе не обнаружено, бромная вода будет обесцвечивающим агентом. При взаимодействии с бромной водой альдегиды окисляются, образуется соль (галогенсодержащая) и образуется бесцветное соединение.
Взаимодействие альдегидов с гидроксидом натрия (NaOH) может привести к образованию соли соответствующей кислоты и алканов. Уравнение: CnH2n+2O + 2NaOH → CnH2n+2 + Na2CO3
Также альдегиды проявляют свойство окисления под действием кислорода. Порядок реакции может быть установлен путем измерения количества поглощенного кислорода или окисления серной кислоты до серных окисей. Уравнение установления порядка реакции: HCHO + H2SO4 → H2O + H2SO4 + S
Качественные реакции на спирты
Качественная реакция на спирты может быть представлена следующим уравнением:
алкен + бромная вода → алкан + бромная кислота
Водный раствор бромной кислоты в этом случае обесцвечивается из-за полученного реакцией органического вещества.
Алкены, а также алкины, под действием хлорной воды окрашиваются в красный цвет в результате образования соответствующих галогеналканов или галогеналкинов.
Если добавить спирт к реагирующему органическому веществу, после чего нагреть смесь с добавлениями цинка и концентрированной серной кислоты, полученное соединение будет иметь белый цвет, что указывает на качественную реакцию. В результате взаимодействия присутствующих элементов образуется сера.
Еще одним вариантом качественной реакции является горение. При горении органической серы происходит образование серы и диоксида серы. Это происходит непосредственно при взаимодействии с кислородом или пригорании в кислородном воздухе.
Алдегиды, а также алкоголи и кислоты, при взаимодействии со спиртовым раствором серебряного нитрата окрашиваются в белый цвет, что говорит о присутствии хлора, брома или их солей в этом состоянии.
Таким образом, зная различные качественные реакции на спирты, можно установить их состав и определить химическую природу вещества.
Видео:
Пожарных затопило водой!
Пожарных затопило водой! by Vladimir Kovalev 17,651 views 4 years ago 52 seconds