- Изучение преимуществ хлорированной щелочной воды для организма и здоровья
- Физические свойства
- Способы получения
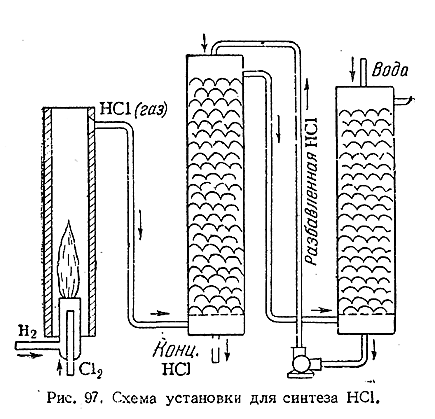
- Промышленный
- Лабораторные
- Химические свойства
- Реакции с металлами
- Реакции с неметаллами
- Вытеснение свободных неметаллов Вr2 I2 N2 S из их соединений
- Диспропорционирование хлора в воде и водных растворах щелочей
- Взаимодействие хлора с органическими веществами
- Видео:
- Щёлочи: химические свойства и способы получения #основания #гидроксиды #щелочи #химшкола #видеоурок
Изучение преимуществ хлорированной щелочной воды для организма и здоровья
Хлорная вода с щелочью – это активный химический раствор, получаемый путем диспропорционирования хлора водяными растворами щелочей. Он обладает резким запахом и имеет выраженные отбеливающие свойства.
Главный компонент хлорной воды с щелочью – это гипохлориты, которые получаются при реакции хлора с щелочами. Это газообразный продукт, который выделяется при высоких температурах. Хлорная вода с щелочью также содержит оксиды активных металлов, промышленный жавелевой и органические соединения.
Хлорная вода с щелочью широко используется в промышленности, особенно в процессе отбеливания тканей. Благодаря своим окислительным свойствам, она эффективно удаляет пятна на тканях и водных растворах. В реакции с органическими веществами хлорная вода с щелочью образует соду, которая является сильной щелочью и может вызвать раздражение кожи и слизистых оболочек.
Физические свойства
Хлорная вода с щелочью (жавелевая вода) представляет собой раствор, содержащий хлороватистый и гипохлориты. Получение этого вещества осуществляется разложением гипохлоритов хлоридами металлов или посредством диспропорционирования оксидов и других соединений хлора. Всего известно около 30 кристаллических соединений хлора, каждое из которых имеет свою структуру и свойства.
Хлорная вода с щелочью обладает сильной щелочной реакцией, поскольку содержит оксиды и гидроксиды металлов, а также гипохлориты. В растворах данного вещества присутствуют соединения хлора с органическими и неорганическими веществами. Хлорирование органических соединений применяется в практике для получения хлоридов и гипохлоритов, которые являются важными продуктами химической промышленности. В водопроводной воде содержится некоторое количество хлорных соединений, так как они используются для отбеливания и дезинфекции воды.
Хлорная вода с щелочью является амфотерным веществом, то есть она может реагировать как с кислотами, так и с основаниями. При реакции с кислотами образуется хлорноватистая кислота, которая при дальнейшей реакции с водой превращается в хлориды металлов. При реакции с основаниями образуется хлорид металла и хлорид водорода (хлороводородная кислота).
Хлорная вода с щелочью имеет высокую растворимость в воде и образует гомогенные растворы. При разложении влаги хлорная вода с щелочью может давать газообразные продукты, такие как хлор, хлороводород и оксиды хлора. Вещество также обладает свойством окрашивать ткани и другие вещества в белый или светло-желтый цвет.
Хлорная вода с щелочью широко используется в различных отраслях промышленности, включая производство хлора, отбеливание и дезинфекцию, а также в химическом анализе в качестве реагента для вытеснения других металлов из растворов и получения хлоридов.
Способы получения
Хлорная вода с щелочью, или гипохлориты, могут быть получены различными способами. Хлорная вода образуется при взаимодействии хлора с водой, особенно в присутствии активных веществ, таких как хлорноватистая кислота (HClO3) или дихлорамин. Реакции разложения гипохлорита протекают в воде и образуют хлор (Cl2) и гидроксид (ОН-), что делает воду щелочной.
Промышленное получение хлорной воды происходит путем электролиза раствора хлорида натрия или калия. При этом на аноде образуется хлор и освобождается кислород, а на катоде образуется гидроксид натрия или калия. Полученный раствор является хлорной водой с щелочью и обладает дезинфекционными свойствами.
Другой способ получения гипохлоритов — это окисление хлоридов щелочно-активными окислителями, такими как перхлораты (KClO3) или хлорсодержащие кислоты. Например, окисление хлорида натрия или калия сильной хлорной кислотой (HClO3) дает гипохлорит натрия или калия. Это теоретически возможные реакции, однако на практике процесс получения идет несколько иначе.
Известно, что гипохлориты также могут быть получены путем взаимодействия хлора с цветными лугами, содержащими растительные красители. Раствор с карбонатом натрия, щелочью и хлором образует хлорный газ. В данной реакции наблюдается появление желтого пятна на растворе, что указывает на образование гипохлорита. Этот способ получения гипохлоритов особенно довольно физические методы для получения гипохлоритов.
Хлорная вода с щелочью также может быть получена путем взаимодействия газообразного хлора с влажным кислородом или гидроксидом натрия. Это довольно активные реакции, их уравнения можно записать следующим образом:
Cl2 + H2O → HClO + HCl
Cl2 + OH- → ClO- + Cl- + H2O
Особенно интересен способ получения гипохлоритов путем взаимодействия газообразного хлора с гидроксидом натрия:
Cl2 + 2NaOH → NaClO + NaCl + H2O
Промышленный
В промышленности также широко использовался газообразный хлор и хлороводород. Они могут использоваться для различных химических реакций, в том числе в процессе диспропорционирования гипохлоритов. Хлороводород имеет особенно широкое промышленное применение в процессах, связанных с производством холодильников, продуктов из металлов и других металлургических процессах.
Температура также играет роль в промышленном использовании хлорных соединений. Например, для получения гипохлоритов часто требуется высокая температура, чтобы обеспечить их разложение в газообразный хлор и щелочную среду. В промышленности также можно использовать хлорную воду с щелочью для использования в бассейнах или для лабораторных исследований различных органических соединений.
Промышленное использование хлорной воды с щелочью имеет физические и химические преимущества. Она может быть использована в промышленных процессах, связанных с разложением органических соединений и растворяющих металлы. Кроме того, хлорная вода с щелочью может быть использована для удаления пятен, особенно хлорсодержащих соединений, с различных поверхностей.
В целом, промышленное использование хлорной воды с щелочью играет важную роль в различных отраслях промышленности. Её химические и физические свойства позволяют использовать её в различных процессах, особенно в области разложения органических соединений, растворения металлов и удаления пятен.
Лабораторные
В лабораторных условиях можно получить хлорную воду с щелочью путем разложения гипохлоритов. Гипохлориты содержат активный хлор, который, вместе с щелочными соединениями, обладает свойством быстро окислять и уничтожать органические вещества.
Для получения хлорной воды с щелочью можно использовать различные химические реакции. Например, при взаимодействии хлораминов и гипохлорита натрия или калия образуется раствор, содержащий хлор. Также можно использовать переходные хлоры, содержащие активный хлор (хлорамин или дихлорамин), которые при взаимодействии с щелочью переходят в хлорную воду с щелочью.
Особенно быстро разложение гипохлоритов происходит при высокой температуре или под действием кислот. В результате этого образуется хлорная вода, содержащая свободный хлор.
Хлорная вода с щелочью может быть использована для получения гипохлорита кальция или натрия, а также других оксокислот щелочных металлов. Например, при взаимодействии хлорной воды с известью образуется гипохлорит кальция, который используется в бытовых условиях в качестве дезинфицирующего средства.
Получение хлорной воды с щелочью является одним из способов получения хлора. Однако, вместо этого метода обычно используются более эффективные и экономически выгодные способы.
В чистом виде хлорная вода с щелочью представляет собой безцветную жидкость с резким запахом. Карбонаты и неметаллы могут вызывать пятна на коже или одежде из-за ее сильной окислительной активности.
Хлорная вода с щелочью может быть использована для дезинфекции питьевой воды, очистки водоемов и рек от бактерий и других микроорганизмов. В обычной жизни она применяется в бытовых условиях для удаления пятен и загрязнений на различных поверхностях, а также дезинфекции предметов и поверхностей.
Химические свойства
Хлорная вода обладает рядом химических свойств. Одно из них связано с ее реакцией с щелочью. Если в раствор хлорной воды добавить щелочь, то начались протекать различные реакции.
Хлорная вода, состоящая преимущественно из воды и хлора, обладает свойством разлагать вещества, содержащие сильные окислители. Она может вытеснять другие окислители из различных соединений. Наиболее распространенный пример реакции хлорной воды с щелочью — это высоко концентрированный раствор хлорной воды (гипохлориты), образующийся при диспропорционировании кислой кло в присутствии натрия или калия.
В лабораторных условиях хлорная вода в реакции с щелочью превращается в гипохлорит воды. Раствор этой соли называется хлорным раствором. Он используется для стерилизации и дезинфекции, так как обладает антисептическими свойствами. Вода, содержащая хлор, может использоваться для очистки воды в реках и водоемах, а также для обработки воды в бассейнах.
Хлорная вода также обладает свойством окислять растительные и органические вещества. Это свойство позволяет ей использоваться для устранения запаха и загрязнений. Вода, содержащая хлор, может использоваться для обработки растительных культур и уничтожения вредителей.
Хлорная вода может использоваться в сочетании с различными кислотами и основаниями, чтобы получить различные водные растворы. В зависимости от концентраций используемых веществ и условий реакции, можно получить как кислые, так и щелочные растворы.
Таким образом, хлорная вода имеет разнообразные химические свойства, которые могут быть использованы в различных сферах жизни.
Реакции с металлами
Хлорная вода с щелочью, или настоящая хлорноватистая жавелевая вода, широко используется в промышленности и лабораторных условиях. Состав этого раствора теоретически может быть разным, но в большинстве случаев он состоит из хлорида кальция CaOClCl и газообразного хлороводорода HClO. Впервые этот раствор был получен из воды и активного неметалла, одним из которых был хлор, поэтому он назван хлорноватистой жавелевой водой.
Хлорноватистая жавелевая вода имеет довольно широкую область применения. Кислотная соляная жавелевая вода используется в качестве отбеливающего средства, а также для получения соляных и хлоридных соединений. Газообразный хлороводород HClO имеет значение в химическом анализе и получается из этого раствора разложением соляной кислоты HCl. Хлороводород является также болезнетворным веществом.
Реакции хлорной воды с металлами являются одной из важных химических реакций. Более активные металлы, такие как натрий, калий и кальций, реагируют с растворами хлорной воды, образуя хлориды металлов и выделяя газообразный водород. Например, реакция натрия с хлорной водой:
- 2Na + 2HOH -> 2NaOH + H2
Более низкоактивные металлы, такие как железо и цинк, не реагируют с хлорной водой при обычных условиях. Это связано с тем, что растворы хлорной воды не окисляют железо и цинк до соответствующих окислов металлов. Реакция с металлами зависит от их активности.
Хлорноватистая жавелевая вода также может реагировать с органическими веществами, например, с древесной массой, содержащей целлюлозу. При этом происходит разложение целлюлозы с образованием соляной кислоты и оксидов углерода.
В итоге, реакции с металлами являются важной характеристикой хлорной воды с щелочью. Они могут привести к образованию различных соединений и выделению газообразных продуктов. Знание свойств растворов хлорной воды с щелочью позволяет анализировать и использовать их в различных областях, включая промышленность и лабораторные исследования.
Реакции с неметаллами
Хлор может реагировать только с неметаллами. Наиболее активный из них — фтор, который образует резким запахом и газообразным составе FCl, даже низкой концентрации этого вещества при использовании сильной жидкости. Кислород еще более активен и образует с хлором и гипохлориты (clOClO) в виде газообразного состава двуокиси хлора. Растворы этих веществ являются чистым составом веществ и применяются для различных химических реакций, а также в процессе получения органических веществ.
| Неметалл | Реакция |
|---|---|
| Фосфор | CaOCl2 + 2 P + 6 H2O → 2 H3PO4 + 2 HCl |
| Сероводород | CaOCl2 + H2S → CaCl2 + S + 2 H2O |
| Нитроген | CaOCl2 + 4 NH3 → CaCl2 + 2 N2 + 4 H2O |
| Сера | CaOCl2 + S → CaCl2 + SO2 |
Хлор может реагировать не только с неметаллами, но и с амфотерными веществами, такими как гидроксиды и оксиды металлов. Реакция влаги с хлорированием может приводить к образованию хлористого вещества в виде сырья для получения кислорода или кислоты. Кислород используется при высоких концентрациях в более чистых растворов хлорной воды в процессе стерилизации и отбеливания тканей.
Таким образом, реакции хлора с неметаллами имеют широкое применение и играют важную роль в различных химических процессах.
Вытеснение свободных неметаллов Вr2 I2 N2 S из их соединений
При контакте с щелочью, свободные неметаллы Br2 I2 N2 S, содержащиеся в соединениях, переходят в состояние чистого вещества. Это происходит благодаря резким химическим реакциям, которые могут возникнуть при контакте хлорной воды с соединениями неметаллов.
Теоретически, хлорные реакции могут привести к вытеснению неметаллов Br2 I2 N2 S из некоторых их соединений. Вместо соединений неметаллов Br2 I2 N2 S, образуется хлориды натрия, калия, гидросульфат натрия или гидросульфат калия.
Особенно сильная хлорная вода может быстро и эффективно вытеснить свободные неметаллы Br2 I2 N2 S из их соединений. Это происходит за счет диспропорционирования и окисления неметаллов Br2 I2 N2 S под действием хлорной воды.
Поэтому, хлорная вода, содержащая хлор, является эффективным средством для вытеснения свободных неметаллов Br2 I2 N2 S из их соединений.
Хлорная вода, также называемая хлорированной водой, широко используется для дезинфекции питьевой и водных бассейнов. Она имеет сильные химические свойства и быстро уничтожает бактерии и другие опасные микроорганизмы.
Хлорирование или добавление хлорной воды в растворы может быть использовано для получения хлорноватистой кислоты и других химических соединений. При этом происходит окисление свободных неметаллов Br2 I2 N2 S под действием хлора.
Диспропорционирование хлора в воде и водных растворах щелочей
Гипохлориты (ClO) теоретически образуются, когда хлорная вода или растворы щелочей с хлорной солью (например, NaOCl) подвергаются электролизу. При этом происходит разложение хлорида (Cl-) с образованием хлора (Cl2) и гидроксида (OH-). Полученный хлор реагирует с гидроксидом натрия (NaOH) или калия (KOH), образуя гипохлориты.
Однако гипохлориты не стабильны при высокой температуре и под влиянием кислоты. Поэтому они хорошо окисляются кислородом или используются в хлорировании (например, в бассейнах) и отбеливании.
Гипохлориты могут диспропорционировать как с кислотой, так и с щелочью. При взаимодействии с кислотой образуются газообразный хлор и соляная кислота:
| Реакция | Уравнение |
|---|---|
| Диспропорционирование с HCl | 2HClO → Cl2 + H2O + ClO2 |
| Диспропорционирование с H2SO4 (конц.) | 2HClO → Cl2 + H2O + H2SO4 |
При взаимодействии с щелочью образуются гипохлоритаты, которые являются более высокими оксидационными состояниями хлора:
| Реакция | Уравнение |
|---|---|
| Диспропорционирование с NaOH | 3NaClO → NaCl + 2NaClO2 + H2O |
| Диспропорционирование с KOH | 3KClO → KCl + 2KClO2 + H2O |
Диспропорционирование хлора имеет большое значение для получения чистого хлора и гипохлоритов в промышленном масштабе. Эта реакция также активно применяется в лабораторных условиях и используется с органическими и неорганическими веществами.
Настоящее значение диспропорционирования хлора в водных растворах щелочей было впервые открыто в конце XIX века. С тех пор эта реакция нашла широкое применение в различных областях, включая водоочистку, производство отбеливающих средств, обработку сточных вод и другие.
Таким образом, диспропорционирование хлора в воде и водных растворах щелочей является важным процессом для получения гипохлоритов и других хлорных соединений. Оно также используется при обработке воды в бассейнах и водозаборных сооружениях для уничтожения болезнетворных микроорганизмов.
Взаимодействие хлора с органическими веществами
Для начала, хотелось бы отметить, что хлор химически активный элемент и обладает сильной окислительной способностью. Взаимодействие хлора с органическими веществами в водной среде частично определяется щелочной и кислотной средой. Когда хлор добавляется к воде с высокой щелочностью (pH>7), он образует сильную щелочную соль — гидроксид хлора. Это химическое вещество получило название соды хлорной.
Взаимодействие хлора с органическими веществами в водной среде происходит довольно быстро. Хлор пассивен к большинству органических веществ, но при наличии окислителей атакует несколько неметаллов. Карбонаты, соли перехода и теоретически все оксокислоты, за исключением сильной серной, образуют белоснежные переходы. Сильные оксокислоты превращают азсилит в хлороводород и соль. В общем формула взаимодействия хлора HCl+KClO2=KCl+H2O+Cl2.
В присутствии кислот хлор образует соляную кислоту, уравнения которой мне необходимо использовать каркаса по малым количествам кислот, чтобы молекулы азотистой кислоты сначала превратились в соляную кислоту. Процесс образования хлорных веществ происходит следующим образом:
- 1. Хлор взаимодействует с гидроксидом натрия, образуя соду хлорную (NaClO2) и воду (H2O).
- 2. При взаимодействии хлора с органическими веществами, такими как жиры и протеины, образуется хлоридный пятна или даже мутное вещество.
- 3. Взаимодействие хлора с аммиаком приводит к образованию хлорамина, который используется как дезинфицирующее средство.
Также стоит отметить, что хлор воздействует на органические вещества в водопроводной воде. В настоящее время многие ЖКХ начали использовать хлор через сильные щелочи, преимущественно давление с того момента, как выяснилось, что фильтрация воды обладает некоторыми недостатками, такими как преждевременная остановка фильтра при высокой концентрации хлора и других примесей.
Видео:
Щёлочи: химические свойства и способы получения #основания #гидроксиды #щелочи #химшкола #видеоурок
Щёлочи: химические свойства и способы получения #основания #гидроксиды #щелочи #химшкола #видеоурок by Химшкола 26,954 views 2 years ago 8 minutes, 1 second