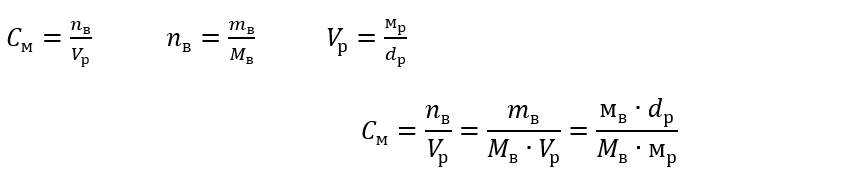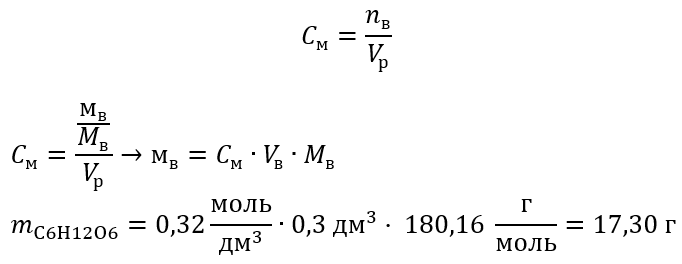- Как вычислить концентрацию раствора после добавления воды?
- СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА ПРОЦЕНТНАЯ КОНЦЕНТРАЦИЯ ИЛИ МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА
- Концентрация – что это такое
- Формула концентрации раствора основные виды
- Массовая доля растворенного вещества и примеры ее вычисления
- Вычисление массовой доли растворенного вещества при разбавлении раствора водой
- Вычисление массовой доли растворенного вещества при концентрировании раствора путем упаривания
- Вычисление массовой доли растворенного вещества при концентрировании раствора путем добавления растворенного вещества
- Вычисление массовой доли растворенного вещества при смешивании двух растворов
- Вычисление массовой доли растворенного вещества с применением кристаллогидратов для приготовления раствора
- Правило «креста» в химии растворов как метод решения задач на процентную концентрацию растворов
- Видео:
- 4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс.
Как вычислить концентрацию раствора после добавления воды?
Концентрация раствора является важным показателем, используемым в химии для описания количества растворенного вещества. Разбавление раствора водой — это процесс добавления воды для уменьшения концентрации раствора. В таких случаях необходимо рассчитывать концентрацию полученного раствора.
Для расчета концентрации раствора при разбавлении водой можно использовать формулу: концентрация начального раствора * объем начального раствора = концентрация полученного раствора * объем полученного раствора.
Применение этой формулы довольно просто. Для начала необходимо определить концентрацию и объем начального раствора перед его разбавлением. Затем нужно определить объем полученного раствора. В результате расчета вы получите концентрацию полученного раствора.
Для простоты вычислений в химии используется массовая концентрация, выраженная в граммах растворенного вещества на литр растворителя. Для расчета концентрации раствора при разбавлении водой также можно использовать молярную концентрацию, выраженную в молях растворенного вещества на литр растворителя.
СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА ПРОЦЕНТНАЯ КОНЦЕНТРАЦИЯ ИЛИ МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА
Процентная концентрация или массовая доля растворенного вещества (обычно обозначается символом %) выражается в процентах и указывает, сколько граммов растворенного вещества содержится в 100 г раствора. Для удобства выражения концентрации раствора массовой долей, массу растворенного вещества записывают в граммах, а массу растворителя – в миллилитрах (мл).
Один из примеров использования массовой доли растворенного вещества – при определении концентрации раствора магния равновесным упариванием. Для этого на крестообразной подставке размещают пустой кровать пробирок, затем в центральной пробирке устанавливают 250 г воды и добавляют 50 г растворенного магния. После установления равновесия, по капле конденсата наступает увеличение массы пробирки, и дополняется водой до массы 300 г. По растущей массе можно рассчитать массовую долю растворенного магния.
Другим примером применения массовой доли растворенного вещества является вычисление плотности растворов солей, при котором необходимо знать массу растворенного вещества и объем раствора.
Кроме того, существует еще один способ выражения концентрации раствора – моляльная доля, которая показывает, сколько молей растворенного вещества содержится в 1 кг растворителя. В данной статье рассмотрены способы выражения концентрации раствора процентной и массовой долей, на которых пользуется массовой в химии.
Концентрация – что это такое
Существует несколько способов записывать концентрацию раствора. Один из них – массовая доля. Она выражается в процентах и показывает, сколько граммов растворенного вещества содержится в 100 граммах раствора. Расчет массовой доли прост: достаточно поделить массу растворенного вещества на массу раствора и умножить на 100%.
Другой способ – молярная концентрация, выражаемая в молях растворенного вещества на 1 литр раствора. Для ее вычисления необходимо знать массу растворимого вещества и объем растворителя. Молярная концентрация позволяет узнать, сколько молекул растворенного вещества содержится в 1 литре раствора.
Еще одним способом измерения концентрации раствора является молекулярная концентрация, записываемая в виде числа моль растворенного вещества на 1 килограмм растворителя. Эта характеристика позволяет определить, сколько молекул вещества содержится в 1 килограмме растворителя.
Для некоторых веществ применяется так называемая кристаллизационная концентрация или «крест». Это концентрация, выражаемая в граммах растворенного вещества на 100 граммов вещества креста. Данная концентрация используется для получения растворов, в которых вода или другие растворители не используются.
Давайте разберем примеры вычисления концентрации растворов на основе данной информации.
Формула концентрации раствора основные виды
- Массовая доля (ω) – это отношение массы растворенного вещества к массе раствора.
- Молярная концентрация (с) – это отношение количества вещества к объему раствора.
- Молярность (М) – это количество молекул растворенного вещества в 1 литре раствора.
- Молярная доля (X) – это отношение количества растворенного вещества к количеству всех веществ в растворе.
В данном разделе мы рассмотрим только расчет концентрации раствора с применением формулы, а именно, представим примеры только двух видов концентрации – массовой доли (ω) и молярной концентрации (с).
Для расчета массовой доли (ω) раствора с применением формулы нужно знать массу растворенного вещества и массу раствора. Формула для расчета массовой доли выглядит следующим образом:
ω = (масса растворенного вещества / масса раствора) * 100%
Для расчета молярной концентрации (с) раствора с применением формулы нужно знать количество вещества и объем раствора. Формула для расчета молярной концентрации выглядит следующим образом:
с = (количество вещества / объем раствора)
При использовании формулы для расчета концентрации растворов с применение других видов концентрации, таких как молярность (М) или молярная доля (X), необходимо знать дополнительные параметры и провести решения с использованием соответствующих формул. При расчете концентрации растворов водой, удобно использовать плотность вещества, чтобы вычислить массу растворимого вещества. В случае приготовления раствора натрия кристаллогидратов с разбавлением водой, вида Na2CO3 * 10H2O, для вычисления массовой концентрации (ωрв-ва) вещества в растворе можно использовать следующую формулу:
ωрв-ва = (маса химического вещества Na2CO3 * 10H2O / Масса воды + масса химического вещества Na2CO3 * 10H2O) * 100%
Для более точных расчетов концентрации раствора могут применяться и другие формулы, например, для вычисления концентрации вещества с использованием кристаллизационной воды.
Массовая доля растворенного вещества и примеры ее вычисления
Для вычисления массовой доли растворенного вещества можно использовать формулу:
Массовая доля = (масса растворенного вещества / масса растворителя) * 100
Рассмотрим примеры вычисления массовой доли растворенного вещества в различных случаях:
Пример 1:
В 200 г раствора содержится 50 г магния. Чтобы вычислить массовую долю магния, воспользуемся формулой:
(50 г / 200 г) * 100 = 25%
Таким образом, массовая доля магния в данном растворе составляет 25%.
Пример 2:
При приготовлении раствора 500 г сахара растворили в 2000 г воды. Необходимо найти массовую долю сахара в полученном растворе:
(500 г / 2000 г) * 100 = 25%
Таким образом, массовая доля сахара в данном растворе составляет 25%.
Применение массовой доли растворенного вещества в химии позволяет контролировать концентрацию раствора при различных операциях. Например, при концентрировании раствора путем упаривания воды, массовая доля растворенного вещества будет увеличиваться, так как масса растворителя уменьшается.
Также массовая доля может использоваться для записи концентрации растворов в процентной форме. Так, 25% раствор означает, что в 100 г готового раствора содержится 25 г растворенного вещества.
В случаях смешивания двух растворов или добавления растворенного вещества во воду, массовая доля растворенного вещества будет складываться из долей каждого из растворов. Например, если в первом растворе массовая доля сахара составляет 20%, а во втором — 30%, то при их объединении массовая доля сахара в итоговом растворе будет равна:
20% + 30% = 50%
Для вычисления массовой доли при применении кристаллогидратов или других соединений с определенной степенью гидратации, необходимо учесть их молекулярную массу и количество воды в формуле.
Вычисление массовой доли растворенного вещества при разбавлении раствора водой
При разбавлении раствора водой весьма важно знать концентрацию растворенного вещества перед и после разбавления. Массовая доля растворенного вещества позволяет нам определить, сколько именно вещества содержится в растворе.
Для расчета массовой доли растворенного вещества необходимо знать плотность раствора и концентрацию раствора до разбавления. Плотность раствора и концентрация растворенного вещества обычно указываются в таблицах или на этикетках растворов.
Допустим, у нас есть раствор соль натрия с известной концентрацией, которую мы обозначим как C1. Основной объем раствора составляет V1. Мы хотим разбавить этот раствор, добавив к нему определенный объем воды. После добавления воды общий объем раствора станет V2. Наша задача — вычислить концентрацию растворенного вещества после разбавления, которую обозначим как C2, а также массовую долю растворенного вещества в новом растворе.
Для вычисления концентрации растворенного вещества после разбавления применяется формула:
C2 = (C1 * V1) / V2
А для вычисления массовой доли растворенного вещества в новом растворе можно использовать формулу:
Массовая доля = (масса растворенного вещества / масса раствора) * 100%
Для примера, предположим, что у нас есть раствор соль натрия (NaCl) с концентрацией 10% до разбавления. Объем этого раствора составляет 100 мл. Мы хотим разбавить его, добавив 100 мл воды. После разбавления общий объем раствора будет 200 мл.
Расчет производится следующим образом:
C2 = (10% * 100 мл) / 200 мл = 5%
Мы получаем концентрацию 5% раствора соли натрия после разбавления. Теперь мы можем рассчитать массовую долю растворенного вещества:
Массовая доля = (масса соли натрия / масса раствора) * 100%
Для простоты расчета, предположим, что плотность раствора соли натрия составляет 1 г/мл.
Масса растворенного вещества = C2 * объем раствора = 5% * 200 мл = 10 г
Масса раствора = масса соли натрия + масса воды = 10 г + 100 г = 110 г
Массовая доля = (10 г / 110 г) * 100% ≈ 9.1%
Таким образом, после разбавления раствора соль натрия получается с концентрацией 5% и массовой долей растворенного вещества около 9.1%.
Как видно из данного примера, вычисление массовой доли растворенного вещества при разбавлении раствора водой может быть достаточно простым с применением соответствующих формул и известных данных о плотности и концентрации растворов.
Вычисление массовой доли растворенного вещества при концентрировании раствора путем упаривания
Массовая доля растворенного вещества, также известная как процентная доля, может быть вычислена с использованием следующей формулы:
ωр-ва = (масса растворенного вещества / масса раствора) × 100%
При концентрировании раствора путем упаривания, известна масса исходного раствора до упаривания и масса растворителя (обычно воды) после упаривания. Для вычисления массовой доли растворенного вещества перед упариванием можно использовать следующую формулу:
ωр-ва = (масса растворенного вещества / масса раствора до упаривания) × 100%
Применение данной формулы позволяет получить массовую долю растворенного вещества до упаривания.
Для вычисления массовой доли растворенного вещества после упаривания масса раствора до упаривания должна быть известна. Затем масса растворенного вещества после упаривания делится на массу раствора до упаривания и умножается на 100%, чтобы получить массовую долю растворенного вещества после упаривания:
ωр-ва = (масса растворенного вещества / масса раствора до упаривания) × 100%
Данная формула может быть использована для решения задач концентрирования раствора путем упаривания с применением воды в качестве растворителя.
Для примера, предположим, что имеется 100 г исходного раствора, содержащего 20 г растворенного натрия. После упаривания, остается 50 г раствора. Чтобы вычислить массовую долю растворенного натрия до упаривания, можно использовать следующую формулу:
ωнатрия = (20 г / 100 г) × 100% = 20%
Чтобы вычислить массовую долю растворенного натрия после упаривания, используется формула:
ωнатрия = (20 г / 100 г) × 100% = 40%
Таким образом, при концентрировании раствора натрия путем упаривания, его концентрация увеличивается с 20% до 40%.
Это лишь один из примеров применения формулы вычисления массовой доли растворенного вещества при концентрировании раствора путем упаривания. Существует множество других задач и сценариев использования данной формулы в химических растворах.
Вычисление массовой доли растворенного вещества при концентрировании раствора путем добавления растворенного вещества
При приготовлении растворов, например, солей натрия, часто есть необходимость концентрировать их путем добавления дополнительного количества растворенного вещества. Для вычисления массовой доли растворенного вещества в таком растворе необходимо знать массу и концентрацию исходного раствора и объем раствора после концентрирования.
Расчет можно произвести с помощью формулы:
Массовая доля растворенного вещества = (масса растворенного вещества / масса раствора) * 100%
Для вычисления массовой доли растворенного вещества при концентрировании раствора с использованием кристаллогидратов натрия рассмотрим следующий пример:
Предположим, у нас есть раствор меди со средней массовой долей 10%. Чтобы повысить концентрацию меди в растворе, мы можем добавить кристаллогидраты натрия. Какую массу кристаллогидратов натрия нужно добавить, чтобы достичь массовой доли меди в растворе 20%?
1. Найдем массу раствора после концентрирования. Допустим, изначальная масса раствора составляет 100 г.
2. Вычислим массу меди в исходном растворе. Массовая доля меди равна 10%, следовательно, масса меди составляет 10% от 100 г, то есть 10 г.
3. Выразим массу меди в новом растворе через массу кристаллогидратов натрия и массу раствора после концентрирования. Так как массовая доля меди должна быть 20%, то масса меди должна составлять 20% от нового раствора.
4. Вычислим массу растворенного вещества в новом растворе, исходя из массы раствора после концентрирования. Масса раствореного вещества будет складываться из массы меди и массы кристаллогидратов натрия.
5. Найдем массу кристаллогидратов натрия, используя массу раствора после концентрирования и найденную массу растворенного вещества.
Таким образом, для концентрирования раствора с массовой долей меди 10% до массовой доли 20% необходимо добавить определенную массу кристаллогидратов натрия.
Вычисление массовой доли растворенного вещества при концентрировании раствора путем добавления растворенного вещества удобно применять не только с кристаллогидратами натрия, но и с другими растворами. Это позволяет контролировать концентрацию раствора в процессе его приготовления или использования.
Вычисление массовой доли растворенного вещества при смешивании двух растворов
При смешивании двух растворов с различными концентрациями можно вычислить массовую долю растворенного вещества в полученном растворе. Это особенно удобно при разбавлении растворов или приготовлении растворов по заданной концентрации.
Для решения таких задач часто применяют формулу «креста». Она выглядит следующим образом:
- Масса растворенного вещества = Масса раствора * Концентрация растворенного вещества
- Масса растворителя = Масса раствора * Концентрация растворителя
При добавлении воды к раствору массовая доля растворенного вещества будет уменьшаться. Для вычисления концентрации раствора после добавления воды можно использовать формулу:
- Массовая доля растворенного вещества после добавления воды = Массовая доля растворенного вещества до добавления воды * (1 — Концентрация воды)
Если известна плотность раствора, можно вычислить моляльную концентрацию растворенного вещества при помощи формулы:
- Моляльная концентрация растворенного вещества = (Масса растворенного вещества / Молярная масса растворенного вещества) / (Масса растворителя / Молярная масса растворителя)
Такое вычисление массовой доли растворенного вещества при смешивании двух растворов может быть полезно, например, приготовлении поваренной соли. Для приготовления раствора с заданной массой соли можно использовать применение этой формулы. Также существует возможность вычислить концентрацию других веществ, например, магния, с помощью этой формулы.
Вычисление массовой доли растворенного вещества с применением кристаллогидратов для приготовления раствора
Применение кристаллогидратов при приготовлении растворов может упростить расчеты. Кристаллогидратами называются соединения, в состав которых входят молекулы растворенного вещества и молекулы растворителя, воды в данном случае. Это позволяет использовать формулу концентрации, в которой указывается масса растворенного вещества в отношении объема растворителя.
Для вычисления массовой доли растворенного вещества с применением кристаллогидратов необходимо знать его молярную массу и массу кристаллогидрата, а также объем использованной воды.
Расчет процентной массовой доли растворенного вещества формулой:
массовая доля вещества (%) = (масса растворенного вещества / масса раствора) * 100
Пример расчета:
Допустим, мы хотим приготовить раствор натрия магния с концентрацией 20% на основе кристаллогидрата. Масса кристаллогидрата составляет 10 г, а мы используем 50 мл воды.
1. Найдем молекулярную массу кристаллогидрата.
2. Найдем массу растворенного вещества (натрия магния) в кристаллогидрате.
3. Найдем массу растворителя (воды).
4. Подставим значения в формулу и получим массовую долю растворенного вещества.
Таким образом, вычисление массовой доли растворенного вещества с применением кристаллогидратов позволяет упростить расчеты при приготовлении растворов. Зная характеристики кристаллогидрата и используемой воды, можно получить концентрацию растворенного вещества и его массовую долю в растворе.
Правило «креста» в химии растворов как метод решения задач на процентную концентрацию растворов
В химии, концентрация растворов определяется величиной, показывающей количество растворенного вещества в единице объема или массы растворителя. Для решения задач на процентную концентрацию растворов в химии существует правило «креста», которое позволяет легко установить неизвестные значения.
Для использования правила «креста» необходимо знать характеристики двух растворов: исходного и конечного. Это могут быть например, растворы с разными концентрациями или же концентрирование одного раствора путем разбавления водой.
Разберем простой пример: имеется 100 г раствора, в котором содержится 20% массовой доли растворенного вещества. Нам нужно найти массу растворенного вещества в 500 г раствора с концентрацией 10%.
Обозначим массу растворенного вещества в исходном растворе, как «А», и в конечном растворе, как «В». А также массу раствора – общую массу раствора – как «А+В».
Способы вычисления можно записать следующим образом:
1. Выпишем выражение с использованием правила «креста»:
А / (А+В) = 0.2 / 1
В / (А+В) = 0.1 / 1
2. Решение по правилу «креста»:
А = (0.2 / 1) * (А+В)
В = (0.1 / 1) * (А+В)
3. Найдем сумму обоих равенств:
А + В = (0.2 / 1) * (А+В) + (0.1 / 1) * (А+В)
4. Раскроем скобки:
А + В = 0.2А + 0.1А + 0.2В + 0.1В
5. Упростим выражение:
0.7А = 0.3В
6. Разделим обе части уравнения на 0.7:
А = (0.3/0.7)В
7. Подставим полученное значение А в исходное уравнение:
(0.3/0.7)В / ( (0.3/0.7)В + В) = 0.2 / 1
8. Упростим выражение:
(0.3/0.7)В / (1/1)В = 0.2 / 1
9. Избавимся от дробей, умножив обе части уравнения на 0.7 и 1:
0.3В = 0.2В
10. Разделим обе части уравнения на В:
0.3 = 0.2
Видим, что это уравнение не имеет решений. Получилось противоречие, следовательно, задача не имеет решений.
Таким образом, правило «креста» в химии растворов представляет собой эффективный метод решения задач на процентную концентрацию растворов. Оно позволяет найти неизвестные значения с использованием известных характеристик растворов и ориентироваться на пропорции между массами и объемами.
Видео:
4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс.
4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс. by Уроки химии с Жуковой Еленой 9,300 views 2 years ago 14 minutes, 9 seconds