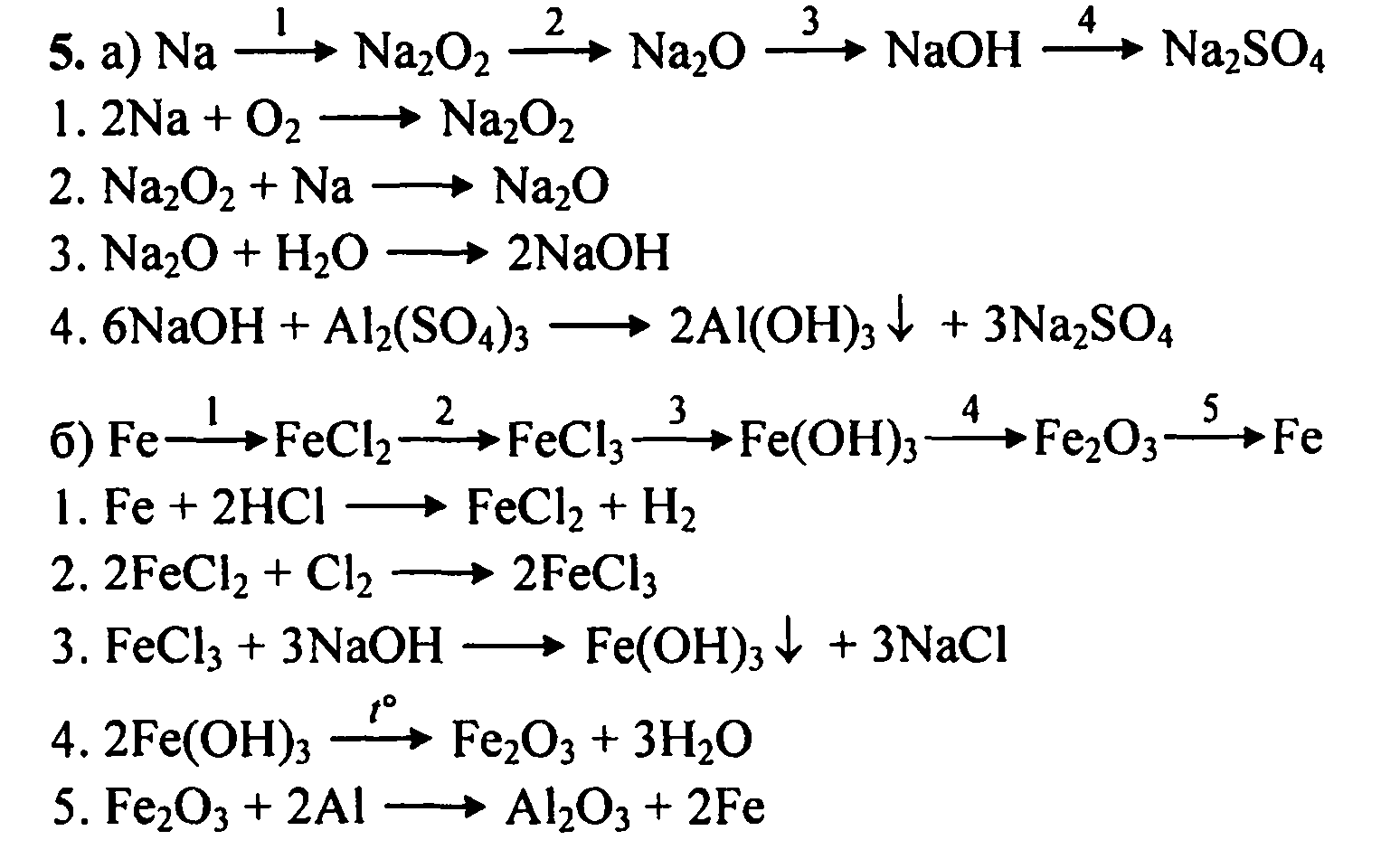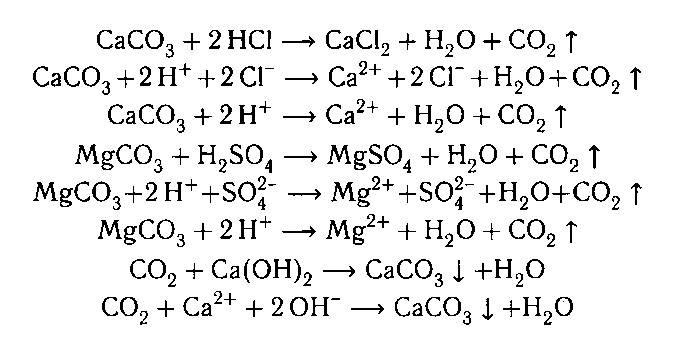- Как происходит реакция между карбонатом кальция и водой?
- Карбонат кальция способы получения и химические свойства
- Способы получения карбоната кальция
- Химические свойства карбоната кальция
- Способ получения
- Качественная реакция
- Характеристики качественной реакции:
- Примеры применения качественной реакции:
- Химические свойства
- CaCO3 + CO2 + H2O уравнение реакции
- Карбонат кальция
- Физические и химические характеристики
- Применение и решение задач
- Видео:
- 🔥 Получил МЕТАЛЛ из СОДЫ. Старинный способ ДОБЫЧИ НАТРИЯ.
Как происходит реакция между карбонатом кальция и водой?
Реакция между карбонатом кальция и водой — одна из самых известных химических реакций, которая происходит при смешивании этих двух веществ. При взаимодействии карбоната кальция (CaCO3) с водой (H2O) получается новое вещество — гидрокарбонат кальция.
Существует несколько способов решения данной задачи. Один из них — добавление определенного количества карбоната кальция к воде и наблюдение за реакцией. Другой способ — проведение данной реакции в лабораторных условиях и анализ результатов.
Примеры реакций карбоната кальция с водой:
1. Реакция гидрокарбоната кальция с кислотой:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
2. Реакция гидрокарбоната кальция с солями:
CaCO3 + NaCl → CaCl2 + Na2CO3
При проведении данной реакции в водном растворе происходит образование гидрокарбоната кальция, в результате которого вода мутнеет.
Рассчитаем массу гидрокарбоната кальция, который можно получить при реакции заданного количества карбоната кальция с водой. Для этого необходимо учитывать молярную массу вещества и количество вещества по уравнению реакции.
Таким образом, реакция между карбонатом кальция и водой является химическим способом получения гидрокарбоната кальция. При взаимодействии этих веществ происходит разложение карбоната кальция и образование нового соединения, а именно гидрокарбоната кальция. Реакция имеет свои физические характеристики, такие как масса и объем образующихся веществ, а также взаимодействие с окружающей средой, например, с хлороводородной кислотой.
CaCO3 + 2H2O → Ca(HCO3)2
Разложение карбоната кальция при взаимодействии с водой осуществляется в качественной химической реакции, основанный на пропускании двух веществ через воду. При этом получается гидрокарбонат кальция, который можно использовать для различных физических и минеральных образований.
Карбонат кальция способы получения и химические свойства
Способы получения карбоната кальция
Карбонат кальция может быть получен путем реакции кислоты, содержащей карбонатный анион, с раствором кальция. Примеры таких кислот — соляная (HCl) и уксусная (CH3COOH) кислоты. Реакция происходит при смешивании растворов, и в итоге получается осадок белого цвета — карбонат кальция.
CaCO3 + CO2 → CaO + 2CO2
Еще одним способом получения карбоната кальция является прокаливание солей этого металла. В результате прокаливания получается твердое соединение, состоящее из ионов карбоната и катионов кальция.
Химические свойства карбоната кальция
Карбонат кальция малорастворим в воде (H2O), что свидетельствует о его низкой растворимости. При добавлении растворов карбоната кальция в воду она мутнеет из-за образования твердого осадка. Это качественная реакция, при помощи которой можно выделить данное соединение.
Карбонат кальция реагирует с кислотами, образуя соль и выделяя углекислый газ. Такая реакция приводит к образованию реакционной среды, богатой CO2.
Изучение химических свойств карбоната кальция позволяет получить ценную информацию о его поведении при взаимодействии с другими веществами. Это позволяет более полно использовать его в различных областях науки и промышленности.
Способ получения
CaO + CO2 → CaCO3
Другим способом получения карбоната кальция является реакция хлорида кальция (CaCl2) с углекислым газом в растворе. В результате образуется гидрокарбонат кальция (Ca(HCO3)2). Эта реакция записывается следующим образом:
CaCl2 + CO2 + H2O → Ca(HCO3)2 + HCl
Вода (H2O) играет важную роль в процессе получения карбоната кальция. Она реагирует с оксидом кальция, приводя к образованию гидроксида кальция:
CaO + H2O → Ca(OH)2
Данная реакция особенно полезна при получении карбоната кальция из оксида кальция при прокаливании, так как образовавшийся гидроксид кальция можно легко преобразовать в карбонат кальция путем взаимодействия с углекислым газом.
Способ получения карбоната кальция также может быть осуществлен путем смешивания растворов сильных щелочей (например, гидроксида натрия NaOH) и сильных кислот (например, соляной кислоты HCl). В результате образуется хлорид кальция и карбонат натрия:
Ca(OH)2 + HCl → CaCl2 + H2O
Ca(OH)2 + 2NaOH → Ca(OH)2 + 2H2O
CaCl2 + Na2CO3 → CaCO3 + 2NaCl
Таким образом, существуют различные способы получения карбоната кальция, которые обусловлены его характеристиками и свойствами взаимодействия с другими веществами.
Качественная реакция
Карбонат кальция (CaCO3) взаимодействует с водой (H2O) и приводит к образованию мутного вещества, которое называется гидрокарбонатом кальция. Данная реакция можно описать следующим уравнением:
CaCO3 + H2O → Ca(HCO3)2
Характеристики качественной реакции:
- При прокаливании карбоната кальция реакция протекает с образованием единственного соединения — гидрокарбоната кальция.
- Реакция происходит только при взаимодействии карбоната кальция с водой, при этом образуется мутное вещество.
- Карбонат кальция не реагирует с сильными кислотами, минеральными солями и другими веществами.
- При растворении карбоната кальция в воде происходит разложение соединения и образуется хлорид кальция (CaCl2).
- Взаимодействие карбоната кальция с концентрированными кислотами приводит к выделению углекислого газа (CO2)
Примеры применения качественной реакции:
- Качественное определение наличия карбоната кальция в препаратах.
- Использование реакции для очистки воды от кальция и получения чистой питьевой воды.
- Использование качественной реакции в химическом анализе для определения содержания карбоната кальция в различных образцах.
Химические свойства
При взаимодействии карбоната кальция с водой возможно образование гидрокарбоната (Ca(HCO3)2), что приводит к мутности растворов после реакции.
При нагревании карбонат кальция разлагается на оксид кальция (CaO) и углекислый газ (CO2), что подтверждается следующим уравнением:
CaCO3 → CaO + CO2
Качественная реакция на наличие карбоната кальция вводится с помощью сильных кислот, например, соляной, при которой образуется углекислый газ:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
Пропускание углекислого газа через растворы щелочей, таких как натрий гидроксид (NaOH), приводит к образованию карбоната кальция:
Ca(OH)2 + CO2 → CaCO3 + H2O
Карбонат кальция обладает молярной массой 100,09 г/моль и химической формулой CaCO3.
Описание химических свойств карбоната кальция включает также его применение в различных областях, например, в производстве строительных материалов, пищевой промышленности и в медицине.
CaCO3 + CO2 + H2O уравнение реакции
Данная реакция может происходить, например, при растворении карбоната кальция в воде (H2O) и дальнейшем пропускании углекислого газа (CO2) через раствор. В результате такой реакции получается углекислая кислота (H2CO3).
Уравнение реакции:
CaCO3 + CO2 + H2O → Ca(HCO3)2
Такое уравнение реакции свидетельствует о получении углерода в виде углекислого газа в результате реакционной смеси карбоната кальция с хлороводородной кислотой и воды.
Решение задач по данной реакции приводит к получению объема углекислого газа по массе кальция карбоната (CaCO3) и другими характеристиками взаимодействия реагентов в конкретной среде.
Примеры применения данной реакции и описание ее физических и химических характеристик можно найти в различных задачах и заданиях по химии. Например, при решении задач на рассчет молярной массы, массы раствора, концентрированными растворами, реакционной средой, пропускании газов через раствор и т.д.
Таким образом, уравнение реакции CaCO3 + CO2 + H2O свидетельствует о возможности получения углерода в виде углекислого газа при взаимодействии карбоната кальция с кислотой в водном растворе и его значение в различных областях исследований.
Карбонат кальция
Карбонат кальция обладает рядом характеристик, которые делают его полезным в различных задачах. Одна из них — его растворимость в водных реакционных средах. При взаимодействии с водой карбонат кальция мутнеет, что свидетельствует о образовании твердого вещества. Это результат химической реакции между карбонатом кальция и водой.
Физические и химические характеристики
Карбонат кальция образует белый кристаллический порошок с формулой CaCO3. Его молекулярная масса равна примерно 100 г/моль. В чистом виде это соединение не растворимо в воде, однако оно может реагировать с углеродным диоксидом (CO2) и превращаться в растворимый гидрокарбонат кальция.
Также карбонат кальция может реагировать с кислотами, например, соляной кислотой. В результате такой реакции образуется растворимый хлорид кальция и углекислый газ (CO2). Углекислый газ можно производить достаточно легко, обрабатывая карбонат кальция концентрированными кислотами.
Применение и решение задач
Карбонат кальция имеет широкое применение и может использоваться в различных отраслях. Он используется в производстве строительных материалов, таких как цемент и известь, и является одним из основных компонентов при производстве стекла, керамики и эмалей.
Также карбонат кальция применяется в фармацевтической промышленности в качестве добавки в препараты для укрепления костей и зубов. В минеральных водах и витаминах также может присутствовать карбонат кальция в качестве добавки.
Решение задач, связанных с реакциями карбоната кальция с другими веществами, основывается на химических уравнениях и концентрации реагентов. Данная информация позволяет получить качественное и количественное описание реакции.
Например, можно рассмотреть задачу о реакции прокаливания карбоната кальция. При нагревании карбонат кальция разлагается на оксид кальция (CaO) и углекислый газ. Уравнение реакции выглядит следующим образом:
CaCO3 -> CaO + CO2
Это лишь один из примеров реакций, в которых участвует карбонат кальция. Взаимодействие этого соединения с различными веществами может привести к образованию разных реакционных продуктов.
Видео:
🔥 Получил МЕТАЛЛ из СОДЫ. Старинный способ ДОБЫЧИ НАТРИЯ.
🔥 Получил МЕТАЛЛ из СОДЫ. Старинный способ ДОБЫЧИ НАТРИЯ. by Огненное ТВ 471,249 views 2 years ago 19 minutes