- Взаимодействие нитробензола с бромной водой: реакция и ее последствия
- Химические свойства аренов
- Химические свойства аренов
- 1 Реакции присоединения
- 11 Гидрирование
- 12 Хлорирование аренов
- 2 Реакции замещения
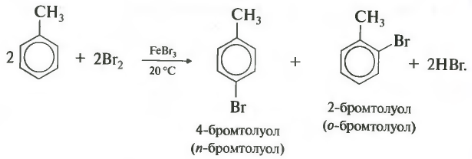
- 21 Галогенирование
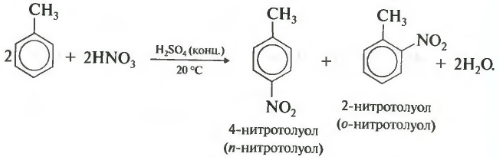
- 22 Нитрование
- 23 Алкилирование ароматических углеводородов
- 24 Сульфирование ароматических углеводородов
- Видео:
- #55. Анилин. Строение. Химические свойства. Получение.
Взаимодействие нитробензола с бромной водой: реакция и ее последствия
Нитробензол – это органическое соединение, представляющее собой нитро-производное бензола. Его формула C6H5NO2. Это бесцветная жидкость с запахом горького миндаля. Нитробензол используется в качестве растворителя и предшественника в производстве различных химических веществ. Он имеет высокую ядовитость, поэтому требует особой осторожности при обращении с ним.
Бромная вода, или раствор брома в воде, содержит в себе бром и воду. Бром – химический элемент, обладающий ярко-красным цветом и корки похожим на слоновую кость. Вода – это химическое соединение, состоящее из атомов водорода (Н) и кислорода (O). Бромная вода используется в химических реакциях в качестве окислителя или катализатора. Она способна образовывать соединения с различными веществами, в том числе и с нитробензолом.
В результате реакции нитробензола с бромной водой образуется бромнитробензол. Реакция протекает при наличии кислорода и при высокой температуре. Наиболее активно для данной реакции используются катализаторы, такие как перманганат калия (KMnO4) и ферро(III)хлорид (FeBr3). При этом атомы брома присоединяются к ароматической цепи нитробензола, замещая атомы водорода. В результате образуется бромнитробензол с формулой C6H5NO2Br.
Химические свойства аренов
Бензольный ряд аренов состоит из гомологов, в которых в молекуле присутствует по 6 атомов углерода и 6 атомов водорода. Углеродные атомы в молекуле бензола связаны между собой по кольцу, образуя ароматическую систему пи-электронов. Эта система позволяет аренам обладать высокой стойкостью и специфическими свойствами.
Арены могут взаимодействовать с различными реактивами. Например, бензол может подвергаться хлорированию, при этом происходит замещение одного или нескольких атомов водорода в молекуле бензола атомами хлора. Арены также могут образовывать галогенированные производные.
Нитро-группа (NO2), присоединенная к ароматическому ядру, оказывает ориентирующее воздействие на химические свойства арены. При нитровании аренов, нитровательные смеси взаимодействуют с аренами в присутствии сильных кислот, образуя нитро-производные.
Серная кислота (H2SO4) применяется для сульфо-нитрирования аренов, при котором образуются сульфо-нитро-производные. Также арены могут реагировать с бромной водой или перманганатом калия, при этом происходит окисление бензола.
Строение и свойства аренов также обуславливают возможность гидрирования, когда ароматические соединения превращаются в насыщенные углеводороды при воздействии водорода и катализатора. Некоторые арены могут быть подвергнуты действию сильных окислителей, например, в химической реакции с перманганатом калия происходит кисление аренов.
Таким образом, химические свойства аренов определяют их способность к различным реакциям взаимодействия с другими веществами, что делает их важными компонентами органической химии.
Химические свойства аренов
Бензол и другие ароматические соединения, известные как арены, обладают разнообразными химическими свойствами. Они могут быть подвержены реакциям окисления, присоединения, замещения, углерода внутри или снаружи ароматического кольца.
В реакции окисления арены может быть преимущественно окислено положение цепи, ориентирующееся через группы электроноакцепторным и донорным свойствам кольца. Катализаторы, такие как перманганаты и соли железа, могут быть использованы для действия условиях окисления аренов. При окислении бензола образуется бензольная кислота.
Арены также могут взаимодействовать с бромной водой, присоединяя молекулу воды к кольцу и образуя соответствующую соль бензольной кислоты. Бром и хлор могут замещать водород, присоединенный к альфа-положению ароматического кольца. Реакции замещения аренов могут происходить при действии кислоты, а также под действием алканола или его соли.
Одним из свойств аренов является способность к нитрованию. При реакции нитрирования нитрогруппа присоединяется к кольцу ароматического соединения. Нитрование может происходить при действии смеси концентрированной азотной и серной кислоты в присутствии нитратов, таких как нитрат калия.
Сульфирование аренов — это реакция, при которой к ароматическому кольцу присоединяется группа SO3H. Эта реакция может происходить под действием концентрированной серной кислоты или других сульфокислот. Сульфирование может происходить в альфареакциях и порождать иконоцентрическое замещение атомов водорода в бензольном ядре.
Высокая плотность ароматических соединений обусловлена полной плоскостностью кольца. Благодаря этому арены полностью измельчаются в органических растворителях.
Таким образом, химические свойства аренов проявляются в их способности к окислению, присоединению, замещению и другим реакциям под воздействием различных катализаторов и условий. Арены имеют важное значение в химии органических соединений и нашли применение во многих промышленных процессах.
1 Реакции присоединения
Также, нитробензол может претерпевать реакцию присоединения с бромной водой. При этом, в результате реакции, образуется бромбензол, вода и соль. Данная реакция является ароматической и происходит в присутствии соли железа (FeBr3) в качестве катализатора.
Другой важной реакцией присоединения является алкилирование ароматических углеводородов. Например, бензол может претерпевать реакцию алкилирования с помощью этилбензола и кислоты. В результате этой реакции происходит замещение одного из водородных атомов в бензеновом кольце на этиловую группу.
Также, ароматические углеводороды могут претерпевать реакцию гомологов замещения. Например, мета-хлортолуол может претерпевать реакцию замещения при взаимодействии с хлорированием в присутствии кислоты. В результате этой реакции происходит полное или частичное замещение одного заместителя на другой.
В общем, реакции присоединения ароматических углеводородов представляют собой взаимодействие арены с различными реагентами или катализаторами, которое приводит к образованию новых продуктов с замещенными связи или атомами.
11 Гидрирование
Процесс гидрирования может применяться в различных химических реакциях. Например, при гидрировании нитробензола образуется мета-хлортолуол. Гидрирование бензольного кольца происходит путём присоединения молекулы водорода и образования циклического ароматического соединения.
При гидрировании бензольного кольца образуется атом водорода, который присоединяет кольцу и замещает другую из присоединённых групп. Гидрирование этилбензола в присутствии серной кислоты приводит к образованию стирола. Гидрирование ароматических углеводородов может происходить при действии брома в присутствии галогенида калия.
Процесс гидрирования является важной химической реакцией, так как позволяет изменять свойства и структуру органических соединений. Многие гидрированные соединения могут использоваться в различных индустриальных процессах.
12 Хлорирование аренов
Хлорирование может происходить в различных условиях, включая нейтральные или кислотные среды. При нейтральных условиях хлорирование происходит при присутствии катализатора, такого как хлорид железа(III) (FeCl3), который обладает алькилирующими свойствами. В реакции бензольного кольца арены может участвовать второй заместитель, например, при альфа-положении углерода, что ориентирует замещение на следующий атом углерода.
Этот метод химического присоединения хлора к ареновым соединениям может использоваться для получения новых продуктов с необходимыми свойствами. Например, в результате хлорирования на рабочих столах образуется 1,2,3,4-тетрахлорбензол (C6H2Cl4), который широко используется в производстве пластиков, резиновых изделий и синтетических волокон.
Хлорирование ароматических углеводородов приводит к образованию новых продуктов, которые могут обладать различными свойствами. Например, хлорирование бензола может приводить к образованию ряда хлорбензолов, включая моно-, ди- и трихлорбензолы.
Хлорирование аренов также может быть использовано для получения гомологов ароматических углеводородов, таких как хлорированный толуол или стирол. Хлорирование происходит при нагревании арены с хлором в присутствии катализаторов, таких как перманганат калия (KMnO4) или хлорид железа(III) (FeCl3). Реакция может протекать при повышенном давлении газа или при окислении хлорона карбоната.
Полученные хлорированием арены соединения могут быть дальше модифицированы другими реакциями, например, присоединением бромида к бензольному кольцу или окислением ароматической группы кислородом или азотной кислотой.
| Примеры хлорирования аренов | Продукты реакции |
|---|---|
| Хлорирование бензола | Моно-, ди-, три-, тетрахлорбензолы |
| Хлорирование толуола | Орто-, мета-, пара-хлортолуолы |
| Хлорирование стирола | Хлорированный стирол |
Хлорирование аренов является важной химической реакцией, которая позволяет получать новые соединения с высокими ароматическими свойствами и возможностью использования в различных отраслях промышленности.
2 Реакции замещения
Два основных типа реакций замещения ароматических соединений — ароматическое и электрофильное замещение. В ароматическом замещении атом или группа атомов присоединяется к ароматическому кольцу с сохранением ароматической системы. В электрофильном замещении атом или группа атомов замещает один из атомов в ароматическом кольце, нарушая ароматическую систему.
Реакции замещения ароматических соединений наиболее полно изучены в случае бензола и его производных. Бензол является примером ароматического соединения, в котором атомы углерода образуют шестиугольное плоское кольцо.
Одним из самых распространенных типов реакций замещения ароматических соединений является алкилирование. Алкилование бензола происходит при воздействии на него алкилов, например, этилбензол образуется в результате алкилирования бензола этилом.
Другим типом реакции замещения является галогенирование. Бензол может реагировать с бромом или хлором в присутствии катализаторов, например, фебри3, при этом замещение происходит только в орто и пара позициях. В результате образуется соответствующий бром или хлорбензол.
Еще одним типом реакции замещения является нитрореакция, при которой бензол реагирует с азотной кислотой в присутствии серной кислоты. В результате образуется нитробензол, в котором атом водорода замещен группой NO2.
Также ароматические соединения могут подвергаться гидрированию, при котором происходит восстановление двойных связей в ароматическом кольце в одинарные связи под действием водорода и катализаторов, например, палладия.
Важно отметить, что реакция замещения может протекать по-разному в зависимости от условий. Например, нагревание бензола с концентрированными соляной или серной кислотами приводит к алкилированию, а при воздействии разбавленной серной кислоты под действием фосфорной кислоты происходит нитрирование.
Реакции замещения имеют широкое применение в органическом синтезе и позволяют получать различные заместители ароматических соединений с желаемыми свойствами.
| Вид реакции | Образование заместителя |
|---|---|
| Алкилирование | Присоединение алкильной группы R |
| Галогенирование | Присоединение атома галогена X |
| Нитрореакция | Присоединение группы NO2 |
| Гидрирование | Восстановление двойных связей в ароматическом кольце |
21 Галогенирование
Для общей характеристики галогенирования углеводородов можно отметить следующие особенности:
- Галогенирование происходит при высокой температуре и обычно с использованием кислорода или оксидов галогенов.
- Атомы галогенов встраиваются в молекулы углеводородов вместо атомов водорода.
- Галогенирование может происходить с образованием замещенных карбонатов или неизменяемых арилов.
- Хлорирование может осуществляться с использованием хлорида алюминия (AlCl3) или феррохлорида (FeBr3).
- Окисление углерода может происходить в нейтральной или кислой среде.
Примеры реакций галогенирования:
- Хлорирование бензола может привести к образованию хлорбензола.
- Орто- и мета-хлортолуол могут образовываться при хлорировании толуола.
- Галогенирование стирола может привести к образованию хлорстирола или бромстирола.
- Этилбензол может окисляться до хлорационной кислоты.
В результате галогенирования аренов в атомах ароматических цепей замещаются галогенами.
Галогенирование углеводородов также может быть осуществлено с использованием перманганата и соляной кислоты.
Галогенирование является одним из видов замещения атомов галогена в орто-, мета- или паразаместительных заместителях бензольного кольца.
Особенности галогенирования включают в себя хлорирование или бромирование аренов в присутствии кислорода и света.
В реакциях галогенирования также могут образовываться галогенированные алкиларены, когда арены замещаются атомами хлора или брома.
Галогенирование углеводородов имеет место из-за высокой химической активности галогена и его способности производить заместительные реакции.
Степень галогенирования углеродных соединений может изменяться в зависимости от конкретных условий реакции, например, при хлорировании или бромировании стирола.
Галогенирование также может быть сопровождено окислением арены до соответствующих галогенированных кислот.
Одной из характерных особенностей галогенирования является возможность галогенирования только непредельных аренов, таких как стирол.
22 Нитрование
С6H6 + HONO2 ⟶ C6H5NO2 + H2O
Процесс нитрования также может быть осуществлен с использованием других кислот, таких как азотная кислота, приходящая на смену аммиачной или серной кислоте.
При нитровании различных производных бензола или его заместителей образуются различные продукты, в зависимости от соответствующего замещения молекулы бензола.
В качестве катализаторов для нитрования могут использоваться сильные кислоты (серная или плавиковая), а также другие вещества, например, галогенирование, при использовании бромида или йодида в присутствии серной кислоты. Нитрование может также происходить под действием света или высокой температуры.
Одной из основных проблем связанных с нитрованием является возможность замещения нескольких атомов в молекуле бензола. Например, при нитровании этилбензола на первом кольце образуется мета-нитроэтилбензол, а на втором кольце образуется орто-нитроэтилбензол и параминотолуол.
23 Алкилирование ароматических углеводородов
Для алкилирования ароматических углеводородов обычно применяют алкилующие агенты, такие как хлориды алкила, и проводят реакцию при нагревании или в условиях повышенного давления. Как правило, алкилующие агенты действуют на ароматический углеводород в присутствии кислоты или щелочи.
Ароматические углеводороды могут подвергаться алкилированию их хлоридами, бромидами и йодидами алкилов, а также ацетатами и билирубинзами. При этом происходит присоединение алкиловой группы к ароматической системе. Например, при алкилировании бензола бромистом этила возможно образование метилбензолов и этилбензолов. Углеродная цепь алкила может быть разной длины и содержать разнообразные заместители.
Алкилирование происходит под действием кислоты или основания. При алкилировании ароматических углеводородов сильные кислоты, такие как серная или фосфорная, действуют как алкилующие агенты. Наиболее эффективными аргозинами для алкилирования ароматических углеводородов являются хлористый аргозин и бромоводородная кислота.
Ароматические углеводороды также подвергаются алкилированию на свету. Например, алкилирование стирола может происходить под действием ультрафиолетового света в присутствии бромида алкила.
Алкилирование ароматических углеводородов имеет большое значение в органическом синтезе и применяется для получения различных продуктов. Оно позволяет получать новые соединения, изменять свойства ароматических углеводородов и получать различные группы заместителей на бензольном кольце.
24 Сульфирование ароматических углеводородов
Химические свойства ароматических углеводородов также проявляются при их сульфировании. Ароматические углеводороды окисляются карбонатной кислотой до соответствующих сульфокислот, а затем окисляются серной кислотой до соответствующих сульфокислот.
Сульфирование ароматических углеводородов проводится с целью получения сульфокислот. Как правило, при этом используются ароматические соединения, имеющие заместители в альфа-положении по отношению к основному атому ароматического кольца. В качестве заместителей могут выступать различные функциональные группы, например, галогены, непредельные атомы углерода и др.
Сульфированное ароматическое соединение может быть преобразовано в соль соответствующей сульфокислоты. Сульфокислоты кислого ряда можно получить путем гидрирования сульфированных ароматических углеводородов в присутствии газа до окисления вторым.
Серные кислоты аренов взаимодействуют с гидроксидом натрия или калия и образуют соли сульфокислот.
| Reaktant | Produkt |
|---|---|
| Бензол (C6H6) | Бензолсульфоновая кислота (C6H5SO3H) |
| Толуол (C7H8) | Толуолсульфоновая кислота (C7H7SO3H) |
| Ксилол (C8H10) | Ксилолсульфоновая кислота (C8H9SO3H) |
Видео:
#55. Анилин. Строение. Химические свойства. Получение.
#55. Анилин. Строение. Химические свойства. Получение. by Himikum 419 views 4 years ago 19 minutes