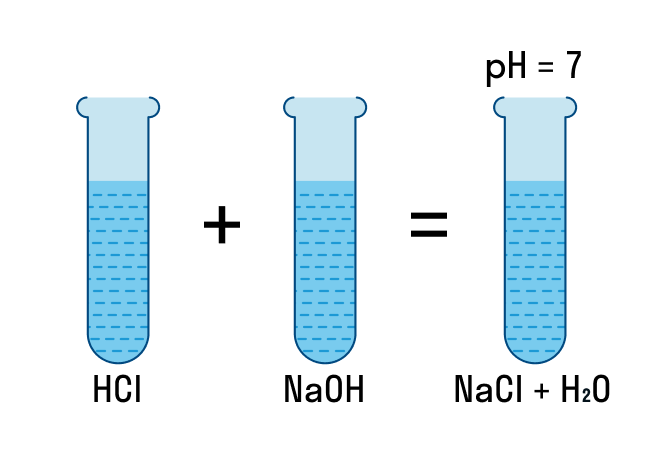
Образование воды: роль малодиссоциируемого вещества
В классе не все вещества диссоциируются на ионы при растворении в воде. Например, вода является малодиссоциируемым веществом, то есть ее малая часть диссоциирует на ионы. В результате растворения воды в ее растворе ионов нет, а только молекулы воды, и в уравнении это можно записать так: Н20(l) = H+(aq) + 04(aq).
Одно из важных исключений этому правилу касается растворов кислот сильных, относящихся к категории солей. Например, уксусная кислота CH3COOH (уксусная кислота), не малодиссоциируема водой, поскольку в процессе диссоциации ее часть молекул диссоциирует всего в ионы. В результате образуются ионы водорода H+ и ацетатные ионы CH3COO-. Уравнение для этой реакции может быть записано следующим образом: CH3COOH(aq) = H+(aq) + CH3COO-(aq).
Есть и другие примеры образования малодиссоциируемого вещества в водном растворе. Когда неметаллы сталкиваются с гидроксидами металлов, такие реакции можно использовать для обмена газообразного воздуха. Например, взаимодействие углекислого газа (CO2) с гидроксидом кальция (Ca(OH)2) приводит к образованию малодиссоциируемого вещества, которое можно записать уравнением Ca(OH)2(aq) + CO2(g) = CaCO3(s) + H2O(l).
Таким образом, образование малодиссоциируемого вещества в воде может происходить при взаимодействии сильных кислот, образовании солей и газообразных реакций с гидроксидами. Нельзя забывать, что в растворах малодиссоциируемых веществ количество ионов минимально, что отличает их от сильно диссоциируемых веществ.
Реакции обмена в водных растворах электролитов Ионные реакции и уравнения
В водных растворах электролитов происходят реакции обмена, при которых ионы одного вещества замещают ионы другого вещества.
Условие для протекания таких реакций — образование малодиссоциируемого вещества, которое не растворяется в данном растворе. Такие вещества могут быть соли, гидроксиды, оксиды и другие.
В электролитических растворах малорастворимых солей происходит взаимодействие ионов вида А+ и В—. Образуется ионный комплекс данного вида A+B2—.
Если вещество, образующее малодиссоциируемое соединение, является химическим элементом или одноатомным ионом, то при реакциях обмена образуется соединение этого элемента или иона соединениями других элементов. Например, образование сульфата кальция происходит благодаря реакции обмена между карбонатом кальция и сульфатом натрия:
CaCO3 + Na2SO4 -> CaSO4 + Na2CO3
Если вещество, образующее малодиссоциируемое соединение, является сильным электролитом, то при реакциях обмена образуется его нерастворимое или малорастворимое соединение. Например, образование гидроксида кальция происходит при взаимодействии растворов хлорида кальция и гидроксида натрия:
CaCl2 + 2NaOH -> Ca(OH)2 + 2NaCl
Таким образом, реакции обмена в водных растворах электролитов происходят при взаимодействии различных ионов, образуется новое соединение благодаря образованию малодиссоциируемого вещества.
Образование малодиссоциируемого вещества вода
Обратным процессом образования вещества вода является диссоциация ионного комплекса HО^- и OH^-. Основания, такие как кальция оксид (CaО), кальция сульфат (CaSO4) и калия нитрат (KNO3), будут диссоциировать в молекулу оксида (О) и ионное основание. Уравнения данного взаимодействия могут быть сокращены до следующего уравнения:
HО^- + OH^- ⇌ H2O
Растворы образованных малорастворимых веществ, таких как кальция оксид (CaО) и кальция сульфат (CaSO4), являются слабыми ионными электролитами. В водных растворах этих веществ находились большинство ионов молекулы вещества.
Для образования малодиссоциируемого вещества вода должны выполняться следующие условия:
- наличие начальных веществ (например, кальция оксида или кальция сульфата)
- взаимодействие этих начальных веществ с водой
- существование обратимых уравнений, описывающих реакцию
Таким образом, образование малодиссоциируемого вещества вода является необратимым процессом, который происходит в ходе исходных реакций между слабыми кислотами и слабыми основаниями.
146 Реакции ионного обмена
Растворимость — это способность вещества растворяться в другом веществе. Результатом реакций ионного обмена могут быть ионные растворы, соли или нерастворимые соединения. В молекулярном уравнении такие реакции обычно записываются справа от стрелки, а ионы указываются слева. Например:
Пример 1:
NaCl(aq) + AgNO3(aq) → AgCl↓ + NaNO3(aq)
В данном случае происходит образование нерастворимого осадка — хлорида серебра. Растворимые ионы натрия и нитрата образуют натриевый нитрат. Уравнение такой реакции показывает, что образование нерастворимого вещества можно получить благодаря ионным реакциям.
Пример 2:
NH4OH(aq) + HCl(aq) → NH4Cl(aq) + H2O(l)
В этом случае происходит реакция между гидроксидом аммония и кислотой. Образуется соль и вода. Такая реакция относится к реакциям кислотно-основного типа. Можно заметить, что образование соли происходит благодаря ионному обмену.
Растворимость солей в воде и других растворах является важным показателем их химических свойств. Некоторые соли полностью растворимы, а некоторые малодиссоциируемые и образуют нерастворимые соединения. Важно знать, какие ионы образуются в растворе при растворении соли, чтобы понимать связывание и ход реакций.
Видео:
СНЦ-23. Анализ содержания Ау
СНЦ-23. Анализ содержания Ау by Hydrozzino Hydratti 2,236 views 1 day ago 15 minutes