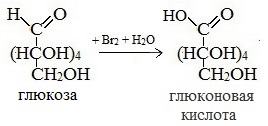
Заголовок: Реакция окисления альдегидов бромной водой: уравнение и механизм.
Альдегиды представляют собой одну из классов органических соединений, содержащих карбонильную группу, которая связана с одним или несколькими атомами водорода. Они обладают характерным полуацетальным строением, в котором атомы углерода окружены атомами водорода и кислорода. Окисление альдегидов может происходить при взаимодействии с различными веществами, такими как бромная вода.
Окисление альдегидов бромной водой является одной из химических реакций, характерных для карбонильных соединений. При этой реакции происходит присоединение брома к карбонильной группе альдегида, образуется кислота или её соль, атомы брома присоединяются к атому углерода вторичного алкоголя.
Уравнение реакции окисления альдегидов бромной водой может быть представлено следующим образом:
Альдегид + Бромная вода → Кислота или её соль + Вторичный алкоголь (с образованием полуацетальной молекулы)
Окисление альдегидов бромной водой характерно для алдегидов, содержащих два атома углерода в молекуле. В реакции происходит присоединение бромной воды к карбонильной группе, что приводит к образованию кислоты или её соли и вторичного алкоголя. Реакция может протекать в нейтральной среде или под действием кислот или оснований.
Альдегиды
Свойства альдегидов характерными для карбонильных соединений. Альдегиды могут окисляться до карбоновых кислот или кетонов. Окисление альдегидов происходит за участия бромной воды, при котором происходит присоединение бромных атомов к двойной связи карбонильной группы, образуется бромгидрин (продуктом реакции окисления).
Альдегиды могут также образовывать альдегидные кислоты путем окисления. Окисление альдегидов может происходить с помощью различных окислителей, например, с хромовой кислотой, окислителями Фехлинга или Толленса, или с помощью хлорной воды.
Имеется также общая реакция конденсации альдегидов с аммиаком или аминами, при которой образуются альдолы — соединения, содержащие две карбонильные группы. В результате такой реакции образуется гидроксилметилениловая группа, которая может подвергаться дальнейшему окислению до карбоновых кислот.
Изомерия также возможна у альдегидов, в результате чего они могут образовывать полуацетали и ацетали. В полуацеталах атом углерода с присоединенной карбонильной группой присоединение атома водорода и одного радикала гидроксильной группы. Ацеталы же образуются при присоединении двух гидроксильных групп к атомам углерода с карбонильной группой.
Структурная изомерия также имеющаяся у альдегидов. В результате замещения группы окисляющий агент или реактив может произойти окисление и других групп атомов. Например, окисление серебром или медью приводит к образованию солей альдегидов.
Физические и химические свойства альдегидов и кетонов
Физические свойства альдегидов и кетонов в основном определяются их молекулярной структурой. Общая тенденция состоит в том, что молекулы альдегидов и кетонов имеют меньшую массу, а следовательно, и более низкую температуру кипения, по сравнению с аналогичными соединениями, такими как алканы и алкены. Это связано с наличием карбонильной группы, которая обладает полярностью и может быть взаимодействовать с средой.
Химические свойства альдегидов и кетонов являются важными для их применения в различных областях. Например, альдегиды могут проявлять установку к повышенной активности окисления. Наиболее типичным примером является окисление формальдегида с использованием бромной воды, в результате которого образуется гликоль. При этом кетоны не проявляют активность окисления, и в присутствии бромной воды они образуют лишь слабую осадок.
Карбонильная группа альдегидов и кетонов также может присоединяться к различным видам химических соединений. Например, альдегиды могут вступать в конденсацию с аммиачным основанием, образуя полуацетальное вещество. Кетоны могут присоединяться к фенолам, образуя ацеталы. Общим химическим свойством альдегидов и кетонов является их способность к полимеризации при воздействии кислоты, составленной из циановодородной кислоты, соединений серебра и перманганатов меди.
Таким образом, физические и химические свойства альдегидов и кетонов имеют ряд общих черт, но также существуют специфические различия, которые определяют их применение в различных областях.
Химические свойства альдегидов и кетонов
У альдегидов карбонильная группа расположена на конце углеводородной цепи, а у кетонов — внутри цепи. Это структурное различие приводит к различным химическим свойствам этих классов соединений.
Одной из важных реакций альдегидов является окисление. Альдегиды окисляются раствором бромной воды или серебра окисью аммония в присутствии нуклеофильного основания, такого как аммиак. В результате окисления атом карбонильной группы присоединяет кислородную атом и образуется кислота или полуацетальное соединение.
Например, реакцией альдегида с раствором бромной воды образуется кислота:
R-CHO + Br2 → R-COOH
Окисление альдегидов может происходить и с помощью других окислителей, таких как серебра меди или калий перманганат. В результате окисления атом кислорода присоединяется к атому углерода карбонильной группы, и образуется карбонильная кислота или полуацетальное соединение.
С другой стороны, кетоны не подвергаются окислению с помощью бромной воды, так как внутренний углерод атом в карбонильной группе затрудняет присоединение кислорода. Кетоны могут быть окислены только при использовании сильных окислителей, таких как кислород или хлор.
Количество окисления карбонильного атома в молекуле альдегида или кетона зависит от окружающей среды и условий окисления. Карбонильная группа также может подвергаться изомерии, при которой карбонильный атом перемещается между различными положениями в молекуле.
Таким образом, химические свойства альдегидов и кетонов отличаются в зависимости от их структуры и взаимодействия с различными реагентами. Эти органические соединения широко используются в различных химических реакциях и процессах в промышленности и лаборатории.
Химические свойства альдегидов и кетонов
Первое физическое свойство, которое присуще альдегидам и кетонам, это высокая растворимость в воде. Эта растворимость объясняется образованием водородных связей между положительно заряженными атомами водорода и отрицательными атомами кислорода. Например, формальдегид, который является самым простым альдегидом, легко смешивается с водой, образуя гидратированный формальдегид.
Химические свойства альдегидов и кетонов также обусловлены присутствием карбонильной группы (C=O). Эта группа атомов карбонила способствует различным реакциям с другими веществами.
Например, альдегиды взаимодействуют с аммиачным гидроксидом, образуя аммония соли. Карбонильный атом альдегида присоединяется к атомам аммиака, образуя соли гидроксила. Эта реакция, называемая циановодородной конденсацией, характерна для альдегидов.
Кетоны, с другой стороны, образуют ацетали при взаимодействии с водой. В результате реакции, один атом карбонила замещается на атом водорода и образуется кеталь. Такое присоединение карбонильная группы с молекулой воды уникально для кетонов.
Важными химическими свойствами альдегидов и кетонов являются их окислительные свойства. Альдегиды легко окисляются до соответствующих карбоновых кислот, например, этаналь может окислиться до уксусной кислоты. Кетоны же не подвергаются окислению без присутствия сильного окислителя, такого как калийный перманганат.
Кетоны и альдегиды также проявляют свойства, связанные с образованием полимеров. Например, формальдегид может претерпевать полимеризацию, образуя сополимеры с другими соединениями, такими как фенол. Этот процесс полимеризации формальдегида широко используется в промышленности, например, для производства пластмасс.
Таким образом, альдегиды и кетоны обладают уникальными химическими свойствами, которые связаны с карбонильной группой и другими функциональными группами, присутствующими в их молекулах. Они имеют важное значение в органической химии и находят широкое применение в различных отраслях промышленности и быту.
Видео:
Окисление ВСЕХ органических веществ за 4 часа | Химия ЕГЭ 2023 | Умскул
Окисление ВСЕХ органических веществ за 4 часа | Химия ЕГЭ 2023 | Умскул by Химия ЕГЭ Умскул 26,762 views Streamed 1 year ago 4 hours, 22 minutes