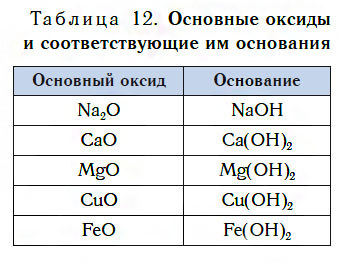
Реакция оксидов с водой и образование в результате оснований
Оксиды — это неорганические соединения, состоящие из кислорода и других элементов, таких как металлы или неметаллы. Способность образования основания при взаимодействии с водой является одной из интересных характеристик оксидов. Взаимодействие оксидов с водой позволяет получить изначально кислотные соединения, назвываемые солями, и представляет собой процесс нейтрализации.
Оксиды, которые при взаимодействии с водой образуют основания, могут быть расположены в ряду растворимости, легко определяемой исходным элементом. Кислотные оксиды, такие как N2O5 или P2O5, образуют кислоты в результате реакции с водой. Между тем, оксиды, подразделяющиеся на основные, образуют основания при взаимодействии с водой.
Процесс взаимодействия оксидов с водой можно упростить, представив его следующим образом: оксид + вода = основание. Например, Сульфат меди II (CuSO4) при взаимодействии с водой восстанавливает оксид меди II (CuO), который, в свою очередь, образует гидроксид меди II (Cu(OH)2). Благодаря этому, оксид меди II считается кислотным оксидом, а гидроксид меди II — основным соединением.
Химические свойства основных оксидов
Щелочные оксиды, такие как Na2O (натрия оксид), K2O (калия оксид) и Li2O (лития оксид), называются также основными оксидами. Они хорошо растворимы в воде и образуют сильные щелочные растворы.
Щелочноземельные оксиды, такие как CaO (оксид кальция) и MgO (оксид магния), похожи на щелочные оксиды, но их растворы обладают слабой щелочной реакцией.
Кислотные оксиды — это оксиды, которые взаимодействуют с водой, образуя кислоты. Они обычно состоят из неметаллов и имеют такие химические свойства, которые делают их кислотными. Некоторые примеры кислотных оксидов включают CO2 (двуокись углерода) и SO2 (двуокись серы).
Оксиды, которые образуют основания, легко разлагаются в воду, взаимодействуя с ней и образуя растворы основания. Например, оксиды щелочных металлов, такие как Na2O, K2O и Li2O, растворяются в воде, образуя гидроксиды NaOH, KOH и LiOH соответственно. Это реакция нейтрализации, при которой щелочные оксиды реагируют с водой и образуют основание, а вода разлагается на водород и гидроксидный ион.
Сольобразование осуществляется с помощью взаимодействия оксидов с кислотами. Когда основной оксид реагирует с кислотой, образуется соль и вода. Например, реакция между оксидом натрия (Na2O) и кислотой серной (H2SO4) приводит к образованию соли (Na2SO4) и воды.
Основные оксиды также могут реагировать с аммиаком (NH3) и образовывать аммиакатный комплекс. Например, реакция между оксидом натрия (Na2O) и аммиаком (NH3) приводит к образованию комплекса NaOH·NH3.
Классификация основных оксидов:
- Оксиды щелочных металлов: Na2O, K2O, Li2O
- Оксиды щелочноземельных металлов: CaO, MgO
Химические свойства основных оксидов связаны с их взаимодействием с водой, кислотами и аммиаком. Они образуют основания, реагируют с кислотами для образования солей и воды, а также могут образовывать комплексные соединения с аммиаком.
Оксиды, которые образуют основания, часто используются в различных процессах и промышленных производствах. Например, оксид натрия (Na2O) используется в производстве стекла, а оксид алюминия (Al2O3) — в производстве алюминия.
Таким образом, химические свойства основных оксидов являются очень важными для понимания их роли в взаимодействии с другими веществами, а также для классификации их в контексте неорганической химии.
Классификация неорганических веществ
Кислотные соединения
Кислотными соединениями являются вещества, способные образовывать ион водорода (H+) при взаимодействии с водой. В результате этого взаимодействия образуется кислота. Кислотные соединения обычно записываются в виде формулы HX, где X — анион (например, Cl, SO4, CO3). Примерами кислотных соединений являются HCl (соляная кислота) и H2SO4 (серная кислота).
Основные соединения
Основные соединения образуют основания при взаимодействии с водой. Взаимодействие основного соединения с водой протекает следующим образом: вещество передает ион гидроксида (OH-) в воду, образуя основание. Основные соединения обычно записываются в виде формулы MOH, где M — катион (например, Na, K, Ca). Примерами основных соединений являются NaOH (натриевая гидроксид) и Ca(OH)2 (кальциевый гидроксид).
Основные соединения могут быть амфотерными, то есть они могут проявлять свойства и кислот и оснований в зависимости от условий.
Соль — это продукт нейтрализации кислоты и основания. Взаимодействие кислоты и основания приводит к образованию соли и воды. Например, при нейтрализации серной кислоты H2SO4 с натриевым гидроксидом NaOH образуется соль Na2SO4 и вода H2O.
Соли в химической классификации обычно расположены между кислотными соединениями и основными соединениями. Однако, существуют и нерастворимые соли, которые могут быть расположены в других группах.
Таким образом, согласно классификации неорганических веществ, основания соответствуют основным соединениям, а соли взаимодействуют с кислотами и основаниями при образовании оксидов или гидроксидов. Растворимые соли обычно образуются в результате нагревания оксидов или гидроксидов соответствующих металлов с кислотами, водные растворы которых имеют характерный вкус.
Видео:
ОСНОВАНИЯ В ХИМИИ — Химические свойства оснований. Реакции оснований с кислотами и солями
ОСНОВАНИЯ В ХИМИИ — Химические свойства оснований. Реакции оснований с кислотами и солями door INTENSIVKURS — Учебный Центр для Школьников 87.050 weergaven 2 jaar geleden 3 minuten en 43 seconden