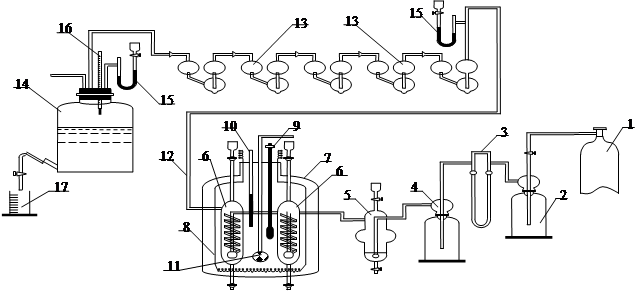
- Исследование реакции аммиака с водой: изучение свойств и применение.
- Практическая работа 2 Получение аммиака и изучение его свойств
- Практическая работа 5 Получение аммиака и изучение его свойств
- Получение аммиака и растворение его в воде
- Горение аммиака в кислороде
- Взаимодействие аммиака с кислотами
- Видео:
- Борьба с аммиаком в воде из скважины.
Исследование реакции аммиака с водой: изучение свойств и применение.
Один из самых практических опытов, который можно провести в домашних условиях, — это опыт аммиак с водой. Для его проведения нам понадобятся всего несколько простых реагентов, которые найдутся в любом доме. Результат этого опыта не оставит вас равнодушными!
Для начала, возьмите маленькую баночку и наполните ее водой до половины. Затем добавьте несколько капель аммиака, чтобы вода стала синего цвета. Итак, смесь из аммиака и воды готова к изучению.
Теперь самое интересное. Постепенно заполните баночку аммиаком, при этом будьте осторожны и не допускайте попадание газа в воздух! Если вы будете проводить этот опыт в закрытом контейнере, то по мере добавления аммиака у вас образуется своеобразный «фонтанчик» голубого цвета, который вырывается из отверстия. Но даже если опыт будет проведен в обычной колбе с отверстием, вы увидите воздушный столб, окрашенный в синий цвет.
Почему же это происходит? Объяснить это явление довольно сложно. Один из вариантов объяснения — взаимодействие аммиака и кислорода в присутствии воды. При взаимодействии аммиака с водой образуется вещество синего цвета, называемое нашатырным купоросом (indh2o), которое обычно используется в медицине. Этот газ очень тяжелый и имеет характерный запах.
Цель проведения этого опыта – продемонстрировать вам интересное взаимодействие аммиака, воды и воздуха. Несмотря на то, что образующийся газ имеет неприятный запах, вода образовавшаяся в результате опыта можно немедленно использовать для полезных целей, например, для промывки различных поверхностей.
Практическая работа 2 Получение аммиака и изучение его свойств
Для получения аммиака потребуются следующие реагенты: водород (H2), щелочь (NaOH или KOH) и тимоловый индикатор (indh). Процесс получения аммиака основан на взаимодействии водорода с водным раствором щелочи. Реакцию можно представить следующим образом:
H2 + NaOH → Na + H2O + NH3
Во время проведения опыта необходимо соблюдать меры предосторожности. Опыты следует выполнять в хорошо проветриваемом помещении или под вытяжкой. При работе с аммиаком внутрь лаборатории следует использовать специальные средства индивидуальной защиты (респиратор, защитные очки и т.д.). В случае необходимости, обратитесь к врачу.
Инструкция по выполнению опытов:
- В ёмкость поместите некоторое количество воды.
- Добавьте щелочь в воду, хорошо перемешайте.
- Закройте ёмкость пробкой с отверстием.
- Вставьте трубку в отверстие пробки так, чтобы один конец трубки погружался в воду, а другой – выпирал из ёмкости.
- Переверните ёмкость, обратившись к ней отверстием вниз. Зафиксируйте ёмкость в таком положении при помощи держателя.
- Поднесите конец выпирающей из ёмкости трубки к живой части тимолового индикатора.
- После образования фонтанчика аммиака тимоловый индикатор окрашивается в синий цвет.
- Проведите другие аналогичные опыты, меняя концентрацию раствора щелочи или количество водорода.
Полученный аммиак можно использовать для дальнейших опытов. Он является химическим реагентом, который часто применяется для получения других веществ или взаимодействия с другими реагентами. Важно помнить, что аммиак – тяжёлый газ, поэтому его хранение следует осуществлять в специальных условиях.
Во время проведения опытов не рекомендуется вдыхать аммиачный газ, так как он может вызвать раздражение дыхательных путей и повреждение органов дыхания. Если во время опыта вы почувствовали дискомфорт или ничего необычного, обратитесь к врачу.
| Задаваемые вопросы | Ответы |
|---|---|
| 1. Что происходит при взаимодействии водорода с водным раствором щелочи? | При взаимодействии водорода с водным раствором щелочи образуется аммиак и вода. |
| 2. Как можно обнаружить образование аммиака во время опыта? | Образование аммиака можно обнаружить по появлению фонтанчика и окрашиванию тимолового индикатора в синий цвет. |
| 3. Какие ещё свойства обладает аммиак? | Аммиак является щелочным раствором, способным реагировать с кислотами. Он также обладает характерным запахом. |
| 4. Как следует хранить аммиак? | Аммиак следует хранить в специальной ёмкости под ублажку, чтобы избежать его испарения и контакта с кислородом. |
| 5. Какие ещё опыты можно провести с аммиаком? | С аммиаком можно провести ряд других опытов, используя его реактивные свойства и взаимодействие с другими веществами. |
Практическая работа 5 Получение аммиака и изучение его свойств
Главная цель данной работы — изучить взаимодействие аммиака с водой и понять, какие реакции происходят при этом процессе.
Читайте внимательно, это очень интересно!
Для проведения опыта потребуются следующие реагенты:
- Аптечный аммиак (NH3)
- Вода (H2O)
- Раствор синей медной (II) кислоты
Первое дело, что следует сделать, это смешать аммиак с водой. Для этого поднесите открытый флакон с аммиаком к воронке, собирающей воду. Из-за реакции между аммиаком и водой образуется аммиакальная солевая смесь, которая собирается в воронку.
В результате взаимодействия аммиака (NH3) с водой (H2O) образуется гидроксид аммония (NH4OH). Во время реакции аммиакальная смесь принимает голубой цвет – это происходит за счет образования комплексов меди, которые остаются в воде.
Подобным образом можно получить аммиак и из раствора синей медной (II) кислоты. Для этого нагрейте раствор синей медной (II) кислоты, чтобы все она испарилась, и осталось только синие кристаллы меди. Затем добавьте к ним аммиак (NH3) и снова наблюдайте голубую жидкость.
Важно отметить, что при длительном хранении аммиака образуются соли аммония (NH4) и углекислая кислота (H2CO3). Если собираетесь собирать аммиак в фильтровальной банке, то ничего страшного, просто промойте ее водой и все будет в порядке.
Для проведения опытов с аммиаком следует помнить о том, что он является едким газом с резким запахом. Во время работы с аммиаком следует использовать резиновые перчатки и никогда не подносить аптечный аммиак к лицу.
Итак, что можно сказать о взаимодействии аммиака с водой? Сначала образуется гидроксид аммония (NH4OH), который, в свою очередь, связывает углекислую кислоту (H2CO3) и образует соединение гидрокарбонат-аммония (NH4HCO3). Приступив к этому способу, немедленно закройте флакон с аммиаком и смешайте его с гидроксидом натрия (NaOH) или гидроксидом калия (KOH), чтобы исключить образованиие гидрокарбоната аммония.
Во время опытов с аммиаком можно заметить, что цвет голубой жидкости почти не меняется — это связано с тем, что аммиак кислоту не окрашивает. Во время работы с аммиаком следует помнить, что он обладает резким запахом, поэтому перед проведением опытов следует проветрить помещение.
Практическая работа 5 Полуячение аммиака и изучение его свойств позволяет более детально изучить взаимодействие аммиака с водой и понять, какие процессы происходят при этом взаимодействии.
Получение аммиака и растворение его в воде
Для получения аммиака и его растворение в воде можно провести простой опыт. Для этого потребуются несколько пробирок, аммиак (его можно купить в аптеке или использовать готовый набор для химического эксперимента), немного воды и гидроксида натрия (NaOH) или гидроксида аммония (NH4OH).
- Возьмите одну пробирку и поместите в нее немного аммиака. Закройте пробирку, чтобы газ не выходил в атмосферу.
- Возьмите другую пробирку и приготовьте в ней раствор гидроксида натрия или гидроксида аммония (1-2 грамма в 100 мл воды).
- Соедините пробирки (поместите одну пробирку в другую вверх ногами), так, чтобы отверстие верхней пробирки было погружено в раствор гидроксида натрия или гидроксида аммония.
- Основной газ, образующийся при реакции, – это аммиак (NH3). Он связывается с гидроксидом в пробирке с раствором и находится в виде газа. Со временем он начинает медленно растворяться в воде, образуя гидроксид аммония (NH4OH).
- Между аммиаком и водой существует особая связь – водородная связь. Именно она делает аммиак подобным своего рода «элегазом» и приводит к его растворению в воде.
- В результате этого опыта в пробирке с раствором гидроксида аммония будет наблюдаться образование пены и «фонтанчика» белого цвета.
- Аммиак также можно наблюдать в виде паров над раствором гидроксида аммония. Этот пар находится выше раствора и образует «легкую» плотность.
- Важно помнить, что аммиак является весьма токсичным веществом и требует аккуратного обращения и хранения.
Таким образом, получение аммиака и его растворение в воде является интересным опытом для изучения химических свойств этого вещества.
Горение аммиака в кислороде
Для проведения этого опыта необходимо предоставить безопасность и соблюдать меры предосторожности. Перед началом работы обратитесь к инструкции и обязательно проконсультируйтесь с врачом.
Чтобы произвести горение аммиака, необходимо смочить ватку в жидком аммиаке и поместить ее в кислородную среду. Можно использовать специальную ёмкость с газоотводной трубкой или отверстием для сбора газов. Сначала аммиак окрашивает воду в синий цвет, поэтому внутри можно наблюдать синий фонтанчик.
Когда в добавок к аммиаку присутствует кислород, происходит горение газа. Реакция очень быстрая и сопровождается высокой температурой. В результате горения образуется азот и водородные кислоты. Вода, получающаяся в результате горения аммиака, окрашивается в жёлтый цвет из-за образования азотных кислот.
Важно помнить, что горение аммиака может быть опасным процессом из-за высокой температуры и образования химических веществ. Поэтому при проведении опытов рекомендуется быть очень внимательным и осторожным.
По окончании опыта необходимо тщательно промыть реактивы и другие инструменты, чтобы устранить возможное заражение остатками газов. Не забудьте также проветрить помещение, чтобы убрать остаточные запахи аммиака.
Горение аммиака в кислороде – сложный и интересный опыт, который позволяет наблюдать химические реакции и свойства вещества. Этот эксперимент может быть использован в образовательных целях для изучения различных аспектов химии и физики.
Читайте также:
- Образование аммиака
- Свойства аммиака
- Получение аммиака другими методами
Взаимодействие аммиака с кислотами
При взаимодействии аммиака с кислотами образуются газоотводная реакция и образование солей. Этот процесс может быть опасен и требует осторожности в проведении опытов.
Если вы хотите провести такой опыт, вам потребуется хорошо проветриваемое помещение с открытыми окнами или вентиляционной системой. Лабораторная поверхность должна быть чистой и аккуратной.
Для проведения опыта возьмите стакан с водой и добавьте к нему немного аммиака. Почему это важно делать с аммиаком? Аммиак – это крайне едкое и едкий газ, который может вызывать опасные последствия для здоровья, поэтому следует обратиться к врачу в случае попадания его на кожу или обнаружения симптомов отравления.
Для защиты рук наденьте перчатки и с учетом соблюдения всех правил безопасности приступайте к проведению опыта.
Возьмите еще один стакан с водой и добавьте в него немного аммиака, чтобы получить раствор аммиака. Поместите пробку с газоотводным отверстием в горлышко этого стакана.
Теперь возьмите еще одну маленькую баночку и наполните ее водным раствором аммиака. Важно заполнить ее лишь на 4/5 объема, чтобы у вас было место для газов, которые образуются при этой реакции.
С помощью проволоки закрепите пробирку в середине колбы. Поставьте колбу в эпруветку, чтобы она не падала, и нагревайте колбу смесью аммиака, которую вы приготовили ранее. Обратите внимание, что колба и ее содержимое должны быть закрытыми, поэтому они должны нагреваться в закрытой среде.
После нагрева аммиачного раствора газы начинают устремляться через газоотводную пробку и образуется фонтан газов.
Не забудьте сделать пару капель этой смеси на фильтровальную бумагу или другую бумажную основу. Если они сквозь основу не падают, значит, взаимодействие прошло успешно.
Возможны также другие интересные аммиак с водой опыты, которые позволяют наблюдать за образованием солей и газов, а также взаимодействовать с кислотами. Но важно помнить о безопасности и соблюдать все необходимые меры предосторожности.
Видео:
Борьба с аммиаком в воде из скважины.
Борьба с аммиаком в воде из скважины. by Айвазов Дмитрий — Московский Теплотехник 2,740 views 3 years ago 9 minutes, 33 seconds