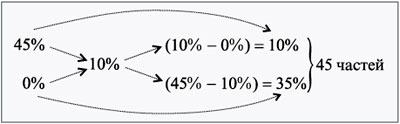
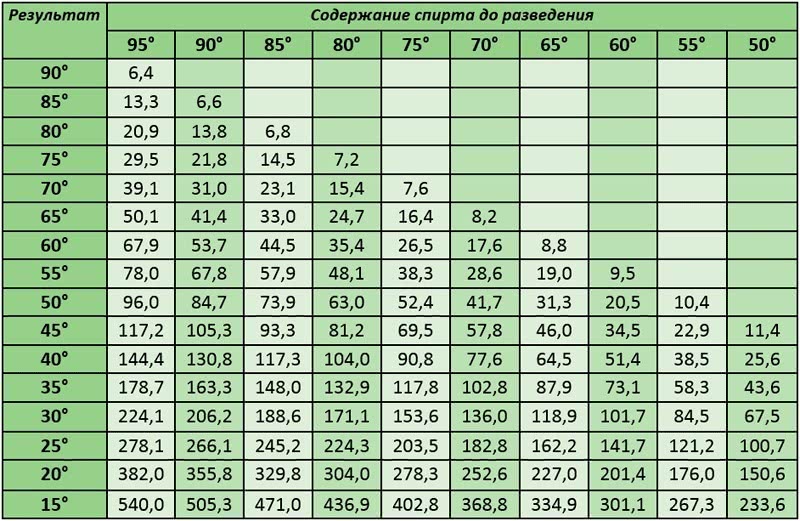
- Определение изменения концентрации вещества при разведении водой
- Формулы для пересчета концентраций растворов
- Калькулятор разбавления растворов
- Концентрация растворов
- Молярная концентрация
- Калькулятор разбавления растворов
- Пример из реальной жизни
- Разбавление раствора
- Заключение
- Калькулятор разбавления концентрированного химического вещества
- Количество вещества и молярная масса
- Видео:
- 4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс.
Определение изменения концентрации вещества при разведении водой
Приготовление растворов является основной задачей химического анализа. Часто встречается ситуация, когда нужное количество вещества растворимо только в небольшом объеме воды, а для проведения анализа необходимо использовать гораздо большее количество раствора. В таком случае возникает задача разбавления концентрированного раствора до нужной концентрации.
Пусть у нас есть определенная масса вещества, которое мы хотим растворить в заданном объеме воды. После добавления воды масса растворимого вещества не изменяется, и задача состоит в расчете объема воды, необходимого для приготовления раствора с нужной концентрацией.
Для решения подобных задач используется формула пересчета концентрации при разбавлении: К1 * V1 = К2 * V2, где К1 — концентрация исходного раствора (количество вещества, используемого для приготовления раствора, деленное на объем этого раствора), V1 — объем исходного раствора, К2 — концентрация раствора после разбавления, V2 — объем раствора после разбавления.
Формулы для пересчета концентраций растворов
Когда необходимо разбавить раствор для достижения нужной концентрации, используются специальные формулы для пересчета концентраций. Этот процесс уменьшения концентрации раствора формулами называется разбавлением.
В лаборатории, приготовление и разбавление химических растворов является одной из важнейших задач. Такие растворы могут представлять собой как твердое вещество, добавленное к определенному количеству воды, так и жидкости, смешанные в необходимом соотношении и объеме.
Когда мы говорим о концентрации раствора, мы имеем в виду количество вещества в данном объеме раствора относительно массы или объема растворителя (в данном случае воды). Для облегчения расчетов в химической лаборатории имеются специальные формулы, позволяющие с легкостью пересчитывать концентрацию растворов.
Однако, сначала необходимо знать молярную массу данного вещества, чтобы использовать формулу пересчета концентрации массы (грамм) в молярную концентрацию (моль на литр). Эта формула выражается следующим образом:
Концентрация (моль/л) = масса вещества (г) / (молярная масса × объем растворителя (л))
Тогда, при разбавлении, чтобы получить нужную концентрацию, можно использовать формулу:
Концентрация (моль/л) после разбавления = (Концентрация (моль/л) до разбавления × объем раствора (л)) / объем раствора после разбавления (л)
Из этих формул можно выразить различные концентрации в зависимости от задачи. Так, моляльная концентрация (моль на литр) зависит от массы вещества и объема раствора:
Моляльная концентрация (моль/л) = масса вещества (г) / (молярная масса × объем раствора (л))
Также существует онлайн-калькулятор молярной концентрации, который позволяет легко сделать расчеты. Путем добавления известных элементов, таких как масса вещества, объем растворителя и нужная концентрация, калькулятор вычислит необходимый объем раствора для достижения нужной концентрации в заданном объеме раствора.
Одной из более простых формул пересчета концентраций является формула для расчета мольной концентрации:
Мольная концентрация (моль/л) = количество вещества (моль) / объем раствора (л)
Подобные формулы пересчета концентраций растворов используются для различных расчетов и анализов в химической лаборатории. Они позволяют с легкостью вычислять необходимые объемы и доли веществ, а также контролировать концентрацию раствора для достижения требуемых результатов.
Важно помнить, что при пересчете концентрации при разбавлении нужно быть внимательным и следить за правильностью расчетов, чтобы обеспечить жизненно важные расчеты в лаборатории.
Калькулятор разбавления растворов
Для расчетов концентрации данного раствора можно воспользоваться онлайн-калькулятором или выполнить ручные расчеты.
Определение концентрации раствора можно произвести с помощью молярной концентрации или массовой концентрации. Молярная концентрация выражается в молях растворенного вещества на литр раствора, а массовая концентрация – в граммах растворенного вещества на литр раствора.
Пример реальной задачи: Необходимо приготовить 1 литр раствора соляной кислоты с концентрацией 2 М. Весит лилитр концентрированного раствора соляной кислоты 4 г/мл. Какое количество воды необходимо для разбавления?
Решение:
- Находим молярную массу HCl по формуле: H(1) + Cl(35.5) = 36.5 г/моль.
- Находим массу раствора соляной кислоты: 1 литр * 4 г/мл = 4000 г.
- Находим количество вещества в молях по формуле: масса раствора / молярная масса = 4000 г / 36.5 г/моль = 109.59 моль.
- Находим количество вещества в молях, нужное для приготовления разбавленного раствора: объем разбавленного раствора * концентрация в молях = 1 л * 2 М = 2 моль.
- Находим количество воды, которое необходимо добавить для разбавления: количество вещества в молях разбавленного раствора — количество вещества в молях исходного раствора = 2 моль — 109.59 моль = -107.59 моль.
Из этого расчета видно, что для приготовления 1 литра 2 М раствора соляной кислоты необходимо добавить 107.59 моль воды. Обратите внимание, что при разбавлении концентрация снижается, так как количество воды увеличивается относительно раствора.
Используя подобные расчеты, можно определить количество воды, необходимое для приготовления разбавленного раствора с заданной концентрацией и для других химических соединений, таких как кислоты, соли или этанол.
Заключение: калькулятор разбавления растворов – полезный инструмент для химиков и широко используется в химической лаборатории при проведении различных химических экспериментов.
Концентрация растворов
Приготовление растворов различной концентрации можно осуществить путем разбавления концентрированного раствора нужной концентрации водой. При этом объем раствора увеличивается, а концентрация снижается.
Для расчета концентраций растворов можно использовать необходимую формулу. Например, для расчета молярной концентрации раствора следует выразить массу вещества в молях и поделить на объем раствора в литрах. Формула для расчета молярной концентрации выглядит так:
молярная концентрация (М) = количество вещества (в молях) / объем раствора (в литрах)
Представим, что приготовлен раствор этанола, где масса этанола составляет 15 грамм, а объем раствора равен 500 миллилитров. Чтобы рассчитать молярную концентрацию этанола, необходимо учесть, что молярная масса этанола (C2H5OH) равна 46,07 г/моль.
Вначале выразим массу этанола в молях:
масса (в граммах) / молярная масса = количество вещества (в молях)
15 г / 46,07 г/моль ≈ 0,326 моль
Тогда подставим полученные значения в формулу молярной концентрации:
молярная концентрация (М) =0,326 моль / 0,5 л ≈ 0,652 М
Таким образом, молярная концентрация раствора этанола составляет примерно 0,652 М.
В жизни иногда нам нужно расчитать концентрацию кислоты в растворе. Рассмотрим пример: если в 1000 литрах раствора содержится 50 г кислоты, то какова массовая концентрация раствора этой кислоты?
Для расчета массовой концентрации воспользуемся следующей формулой:
массовая концентрация = масса вещества / объем раствора
50 г / 1000 л ≈ 0,05 г/л
Таким образом, массовая концентрация раствора кислоты составляет примерно 0,05 г/л.
При необходимости провести разбавление раствора до требуемой концентрации, можно использовать формулу:
конечная концентрация (Ск) = (изначальная концентрация (Си) × объем исходного раствора (Vi)) / конечный объем раствора (Vк)
Допустим, у нас есть исходный раствор с концентрацией 0,2 М и объемом 1 л, а требуется получить раствор с концентрацией 0,05 М и объемом 2 л. Тогда формула для расчета конечной концентрации будет выглядеть следующим образом:
(0,2 М × 1 л) / 2 л = 0,1 М
Таким образом, для получения раствора с концентрацией 0,05 М и объемом 2 л необходимо добавить 1 л исходного раствора с концентрацией 0,2 М.
В повседневной жизни для расчета концентраций растворов можно воспользоваться специальными онлайн-калькуляторами и формулами. Например, калькулятор разбавления позволяет быстро и легко рассчитать необходимое количество вещества или объем раствора при разбавлении.
Таким образом, концентрация растворов является важной величиной при приготовлении и использовании растворов различного назначения. Понимание концентрации растворов позволяет проводить нужные расчеты и разбавления с помощью соответствующих формул и таблиц.
Молярная концентрация
Пределы концентрации молярного раствора зависят от растворителя. Водород является одним из элементов, для которого можно использовать молярную концентрацию.
Представим, что в лаборатории нам необходимо рассчитать молярную концентрацию водорода в воде. Пусть мы знаем массу растворенного вещества (водород) и объем раствора (воды). Для определения молярной концентрации водорода можно использовать следующую формулу:
Молярная концентрация = количество вещества (мол) / объем раствора (л)
Путем использования этой формулы и зная массу водорода и объем воды, можно рассчитать молярную концентрацию водорода.
Однако, для более строгого расчета концентрации в лаборатории нужно учесть и другие факторы, такие как общее количество растворенного вещества, масса раствора и молярная масса элемента.
В химической лаборатории можно использовать калькулятор для расчета молярной концентрации. Для этого необходимо ввести массу растворенного вещества и объем раствора.
Таким образом, молярная концентрация выражается в молях растворенного вещества в единице объема раствора и позволяет определить соотношение концентраций разбавленного и растворенного вещества.
| Символ | Определение |
|---|---|
| М | Молярная концентрация |
| моль/л | Единицы измерения концентрации |
| моль | Количество вещества |
| л | Объем раствора |
Калькулятор разбавления растворов
При приготовлении химической жидкости растворы часто нужно разбавлять водой. Для определения необходимого количества воды для разбавления, требуется пересчет концентрации раствора.
Концентрация растворов может быть выражена в разных величинах, таких как молярность, молярная концентрация, а также весовая концентрация. Расчеты при разбавлении растворов применяются для определения количества элементов или соединений в объемных величинах, таких как граммы или литры.
Для пересчета концентрации при разбавлении водой используются следующие формулы:
| Величина | Формула |
|---|---|
| Молярность | Молярность после разбавления = (Молярность до разбавления * объем до разбавления) / (объем до разбавления + объем воды) |
| Молярная концентрация | Молярная концентрация после разбавления = (Молярная концентрация до разбавления * объем до разбавления) / (объем до разбавления + объем воды) |
| Весовая концентрация | Весовая концентрация после разбавления = (Вес вещества до разбавления * объем до разбавления) / (объем до разбавления + объем воды) |
При разбавлении раствора вода добавляется до необходимого объема. Содержание элементов или соединений в разбавленном растворе рассчитывается с использованием строгой математической формулы.
Например, для приготовления 1 литра насыщенного раствора кислоты, который вначале содержит 100 грамм кислоты, необходимо добавить воды до объема 1 литр. При разбавлении концентрация кислоты после добавления воды будет расчитываться по формуле:
Молярность после разбавления = (Молярность до разбавления * объем до разбавления) / (объем до разбавления + объем воды)
где:
- Молярность до разбавления — количество молекул кислоты в объеме до добавления воды;
- объем до разбавления — количество литров кислоты до добавления воды;
- объем воды — количество литров воды, которые необходимо добавить для разбавления.
Таким образом, для данного примера при расчете молярности кислоты после разбавления требуется знать начальную молярность кислоты, объем кислоты и объем воды, которые необходимо добавить. После проведения расчетов можно определить точную молярность кислоты после добавления воды и, соответственно, ее концентрацию в разбавленном растворе.
Аналогичные расчеты могут быть применены для других веществ, таких как соли или твердые растворы, при разбавлении с использованием различных объемных или массовых величин. Для этого необходимо знать начальные данные о концентрации и объеме и добавления воды по определенным формулам для расчета конечной концентрации.
В химии расчеты при разбавлении растворов являются важным инструментом приготовления нужной концентрации для химических экспериментов или процессов. Точные расчеты позволяют получить необходимую концентрацию раствора путем добавления определенного количества воды.
Пример из реальной жизни
Допустим, в химической лаборатории требуется приготовить 200 мл раствора соляной кислоты с концентрацией 0,5 моль/л. С помощью формулы Авогадро, представим это в объемных единицах. Раствор с концентрацией 0,5 моль/л означает, что в каждом литре раствора содержится 0,5 моль соли.
Для реализации задачи по разбавлению раствора, путем добавления нужного количества воды, необходимо знать массу соли, которая нужна для приготовления 200 мл раствора. Однако, масса соли будет различаться в зависимости от концентрации первоначального раствора и желаемой концентрации после разбавления.
Таким образом, для точного расчета необходимости добавления воды возможно использовать онлайн-калькулятор моль-литр или следовать строгой химической формуле. В реальной жизни, в химической лаборатории, обычно используются таблицы или программы, которые учитывают все данные и выдают точные результаты.
Например, пусть мы хотим разбавить 100 мл раствора с концентрацией 1 моль/л до концентрации 0,5 моль/л. С помощью онлайн-калькулятора моль-литр, следуя примеру, можно узнать, что для достижения желаемой концентрации требуется добавить 100 мл дистиллированной воды.
Таким образом, разбавление растворов с различными концентрациями водой может быть произведено с использованием онлайн-калькулятора моль-литр или строгой химической формулы. Это позволяет точно определить необходимое количество воды для достижения нужной концентрации раствора в химической лаборатории.
| Растворы | Количество молей | Объем (литры) | Масса (граммы) |
|---|---|---|---|
| Соляная кислота | 0,5 | 1 | 36,5 |
| Дистиллированная вода | — | 1 | 0 |
| Этанол | 1 | 1 | 46 |
Разбавление раствора
Избежание неправильных концентраций химического раствора может быть обеспечено путем пересчета концентраций после разбавления. Необходимая концентрация после разбавления может быть выражена в молярной концентрации, массовой концентрации или в других соответствующих единицах концентрации.
Для определения нужного количества разбавляющего растворителя, такого как вода, можно воспользоваться онлайн-калькулятором или использовать стандартные методы расчета на основе молярности и объема раствора. В случае с разбавлением соли, масса разбавления можно рассчитать с помощью расчета объемных концентраций.
Приготовление разбавленного раствора может быть осуществлено путем добавления нужного объема растворителя, какой-либо химической вещества, к заданному объему и концентрации данного раствора. Тогда концентрация раствора изменится в соответствии с объемом разбавителя.
Разбавление растворов имеет большое значение, так как может использоваться для подготовки растворов с нужной концентрацией в химической лаборатории или для достижения определенных концентраций веществ в различных процессах, например, в медицине или в химической промышленности.
Важно отметить, что при разбавлении раствора концентрация химического раствора уменьшается, а объем раствора увеличивается. Это может быть полезной информацией при работе с химическими растворами и молярными концентрациями.
Заключение
При пересчете концентрации этанола при разбавлении водой необходимо учитывать количество молекул этанола и объем полученного раствора. Для избежания ошибок при приготовлении необходимой концентрации раствора можно использовать онлайн-калькулятор. Например, для приготовления 1 литра раствора с концентрацией 40% можно использовать массу этанола в количестве 400 грамм. Приготовление растворов с разными концентрациями с использованием данного примера можно представить в виде таблицы:
| Концентрация, % | Масса этанола, г | Объем воды, л |
|---|---|---|
| 10 | 100 | 0.9 |
| 20 | 200 | 0.8 |
| 30 | 300 | 0.7 |
| 40 | 400 | 0.6 |
| 50 | 500 | 0.5 |
Таким образом, для приготовления раствора с заданной концентрацией этанола можно использовать формулу:
Масса этанола = концентрация * объем раствора
Расчеты проводятся в граммах для удобства использования онлайн-калькулятора, однако, при реальном приготовлении раствора, массу этанола можно преобразовать в моль, используя формулу:
Масса этанола (в моле) = масса этанола (в граммах) / молярность этанола (г/моль)
Таким образом, для точного пересчета концентраций в разных единицах можно использовать соответствующие формулы для разных растворителей и их молярностей, а также учитывать массу добавляемой соли или другого твердого вещества при растворении. Важно помнить о правильной записи и расчете количества растворителя при изначальном добавлении жидкости.
Калькулятор разбавления концентрированного химического вещества
При работе с химическими веществами часто требуется разбавить концентрированный раствор, чтобы получить раствор нужной концентрации. Калькулятор разбавления позволяет определить необходимое количество концентрированного вещества и объем воды для получения желаемого раствора.
Концентрация химического вещества обычно выражается в молярности (моль на литр) или в процентах массы растворенного вещества. Концентрация в процентах массы может быть измерена в г/100 мл или % (объемных).
Для расчета разбавления раствора с известной концентрацией используют следующую формулу:
М1 x V1 = М2 x V2
- М1 — начальная концентрация (моляльная или процентная)
- V1 — объем начального раствора (литры)
- М2 — конечная концентрация (моляльная или процентная)
- V2 — объем конечного раствора (литры)
Разбавление концентрированного химического вещества производится путем добавления определенного объема воды. Чтобы избежать ошибок, следует строго соблюдать правила химической безопасности при работе с химическими веществами.
Допустим, у нас есть концентрированный раствор соляной кислоты (HCl), молярность которого составляет 12 М. Необходимо разбавить этот раствор до 1 М. Для этого нужно определить объем концентрированного раствора, который надо взять, и добавить соответствующее количество воды.
Сначала проведем расчет для определения количества концентрированного вещества (HCl):
М1 x V1 = М2 x V2
12 М x V1 = 1 М x 1 л
V1 = 1 л / 12 М
V1 = 0,083 л
Таким образом, необходимо взять 0,083 л (83 мл) концентрированного раствора соляной кислоты и добавить 917 мл воды для разбавления до 1 М.
Полученный раствор будет иметь моляльную концентрацию 1 М.
Однако, при работе с другими химическими веществами или при других условиях задача может быть более сложной. Например, для разбавления концентрированного раствора соли (NaCl) с массой 35 г до концентрации 1% массы, требуется провести следующий расчет:
М1 x V1 = М2 x V2
35 г / 100 мл x V1 = 1% x 1000 мл
V1 = (1% x 1000 мл) / (35 г / 100 мл)
V1 = 2,86 л
В данном случае, чтобы получить 1% раствор соли (NaCl), необходимо взять 2,86 л концентрированного раствора и добавить 1130 мл (1,13 л) воды.
Этот пример демонстрирует, что при разбавлении концентрированного вещества объем воды для разбавления может быть значительно больше, чем объем концентрированного вещества. Также необходимо учесть массу концентрированного вещества, которая может быть выше, чем масса этого вещества в готовом растворе.
Расчет разбавления концентрированного химического вещества с помощью калькулятора позволяет точно определить нужное количество вещества и объем воды для получения желаемого раствора. Это помогает избежать возможных ошибок при проведении химических экспериментов и обеспечивает безопасность в лабораторных условиях.
Количество вещества и молярная масса
Для пересчета концентрации при разбавлении водой необходимо учитывать количество вещества и молярную массу.
Количество вещества выражается в молях и определяется как отношение массы вещества к его молярной массе.
Молярная масса химического вещества выражается в граммах на моль и показывает, сколько граммов данного вещества содержится в одной молекуле или атоме.
При разбавлении концентрированного раствора водой концентрация вещества снижается, так как объем раствора увеличивается, а количество вещества остается таким же.
Для расчета концентрации разбавленного раствора можно использовать соотношение между концентрацией концентрированного и разбавленного растворов:
- Концентрация разбавленного раствора = (Концентрация концентрированного раствора * Объем концентрированного раствора) / Объем разбавленного раствора
Пусть у нас есть задача: в лаборатории необходимо приготовить 1 литр раствора определенной концентрации. В данном растворе нужно добавить 500 мл дистиллированной воды. Тогда объем концентрированного раствора составит 1 литр, а объем разбавленного раствора — 1.5 литра. Из известных данных можно определить концентрацию концентрированного раствора и применить формулу расчета для получения концентрации разбавленного раствора.
Таким образом, добавление воды при разбавлении раствора приводит к уменьшению его концентрации. Если нужно получить раствор с большей концентрацией, необходимо добавить меньше воды.
Видео:
4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс.
4.Молярность и нормальность растворов. Подготовка к олипиадам по химии 8-9 класс. by Уроки химии с Жуковой Еленой 9,240 views 2 years ago 14 minutes, 9 seconds