- Образование кислот при реакции хлора с водой
- Соединения хлора
- Хлороводород соляная кислота HCl
- Свойства хлороводородной кислоты:
- Использование хлороводородной кислоты:
- Хлорноватистая кислота HClO и ее соли
- Реакция получения хлорноватистой кислоты:
- Реакция образования хлоратов:
- Реакция образования перхлоратов:
- Реакция образования хлористой соли:
- Видео:
- Взаимодействие хлора с фосфором
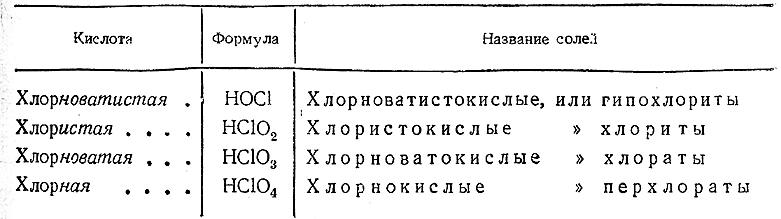
Образование кислот при реакции хлора с водой
Реакция хлора с водой является одной из самых сильных и резких химических реакций. Когда хлор вступает в контакт с водой, он растворяется в ней, образуя хлорноватую кислоту (HClO) и хлороводород (HCl). Оба этих соединения обладают сильными кислотными свойствами.
Хлороватая кислота (HClO) и хлорноватистая кислота (HClO2) — это два главных соединения, образующихся при взаимодействии хлора с водой. Хлороватая кислота (HClO) присутствует в растворах хлора, а хлорноватистая кислота (HClO2) может быть получена в лабораторных условиях.
Хлорная кислота (HClo3) и хлорная кислота (HClo4) являются кислородными кислотами, которые образуются при взаимодействии хлора с водой. Эти кислоты проявляют себя как сильные окислители и реагируют с различными веществами, в том числе с металлами, образуя соли.
Кроме того, есть и другие кислоты, образующиеся при взаимодействии хлора с водой. Кислота хлористоватистая (HClO4) и кислота хлорноватистоватистая (HClO2) — это два примера таких кислот. Они обладают сильными кислотными свойствами и растворяются в воде с образованием кислотных растворов.
Соединения хлора
Одним из таких соединений является хлорная кислота (HClO), которая образуется при растворении хлора в водных растворах. Она проявляет реакцию с основаниями и образует соли — хлориды. Хлорная кислота является сильной кислотой и обладает резким запахом.
В лаборатории можно получить ее окислением хлорноватой кислоты (HClO3) с помощью сильного окислителя, например, перманганата калия. Хлорноватая кислота, ihrer_turn HClO3, является сильным окислителем и сама разлагается при комнатной температуре, образуя хлористую кислоту (HClO2).
Другим соединением хлора является хлорид кислоты (H2O + Cl2O). Оно образуется при взаимодействии хлорной кислоты с хлорной двуокисью (Cl2O7), которая является сильным окислителем. Хлорид кислоты может вступать в реакцию с органическими соединениями и образовывать хлористые соли.
Еще одно соединение хлора — хлористый газ (Cl2). Он имеет зеленовато-желтый цвет и является сильным окислителем. Хлористый газ обладает резким запахом и может вызывать ожоги при длительном воздействии на кожу или слизистые оболочки.
Таким образом, соединения хлора включают хлорную, хлорноватую и хлористую кислоты, а также хлориды и газообразный хлор. Они проявляют реакцию при взаимодействии с водой, окислением органических соединений и вступают в реакции с основаниями, образуя различные соли.
Хлороводород соляная кислота HCl
Хлороводородная кислота образуется при взаимодействии хлора с водой по следующему уравнению:
Cl2 + H2O → HCl + HClO
Хлороводородная кислота обладает сильными кислотными свойствами и может реагировать с основаниями, образуя соль и воду:
HCl + NaOH → NaCl + H2O
Однако, по сравнению с некоторыми другими кислотами, хлороводородная кислота является слабой, так как она лишь частично диссоциирует в растворе. Тем не менее, в концентрированной форме она обладает сильным обжигающим запахом.
Свойства хлороводородной кислоты:
- При комнатной температуре и давлении хлороводородная кислота представляет собой бесцветную газообразную вещество с остро-раздражающим запахом.
- Хлороводородная кислота растворяется в воде, образуя раствор, который называется хлороводородной кислотой или соляной кислотой.
- Хлороводородная кислота является сильным окислителем и может взаимодействовать с некоторыми веществами, такими как хлор, окислением которого образуется высокооксидное соединение — хлорная кислота Cl2O7.
- Хлороводородная кислота образует два серии солей — хлористые и хлористоватистые соли.
- Хлороводородная кислота является одной из основных кислот в химической лаборатории и применяется в различных процессах получения кислот, солей и других химических веществ.
Использование хлороводородной кислоты:
Хлороводородная кислота широко применяется в химической промышленности и лабораторных исследованиях. Она используется для получения многих других кислот, солей и других химических веществ. Кроме того, хлороводородная кислота используется в процессе обработки металлов, при производстве пищевых продуктов и в медицине.
Хлорноватистая кислота HClO и ее соли
В лаборатории хлорноватистую кислоту можно получить путем окисления хлористого серебра (AgCl) с помощью сильного окислителя, таким как перманганат калия (KMnO4). При этой реакции образуется хлорноватистая кислота и осаждается серебро:
Реакция получения хлорноватистой кислоты:
- AgCl + H2SO4 + H2O + KMnO4 → HClO + MnSO4 + Ag2SO4 + K2SO4
Хлорноватистая кислота HClO обладает окислительными свойствами и может реагировать как с веществами, содержащими водород, так и с неорганическими и органическими веществами. В присутствии сильных окислителей, таких как перманганат калия, хлораты (NaClO3) могут образовываться из хлорноватистой кислоты.
Реакция образования хлоратов:
- 3 HClO + 6 KMnO4 → 3 KClO3 + 6 MnO2 + 3 H2O + 3 KOH
Хлорноватистая кислота HClO также может реагировать соединениями хлора (HI, KI) с образованием перхлоратов. При этой реакции хлорноватистая кислота выступает в качестве окислителя.
Реакция образования перхлоратов:
- 6 HClO + 10 HI → 5 H2O + 10 ClO4I + I2
Хлорноватистая кислота HClO также образуется при взаимодействии диоксида хлора (ClO2) с водой. Эта реакция происходит при комнатной температуре и результатом является образование хлорноватистой кислоты и хлористой соли:
Реакция образования хлористой соли:
- ClO2 + H2O → HClO + HCl
Хлорноватистая кислота HClO и ее соли являются важными веществами в химической промышленности и научных исследованиях. Они используются в процессах окисления, дезинфекции и производстве различных химических соединений.
Видео:
Взаимодействие хлора с фосфором
Взаимодействие хлора с фосфором de Vladimir Kuznetsov 381 vues il y a 10 ans 28 secondes