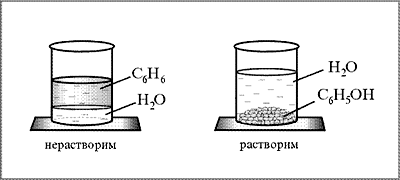
- Исследование растворимости многоатомных спиртов в воде
- Характеристика спиртов
- Растворимость многоатомных спиртов воде
- Свойства и получение многоатомных спиртов
- Физические характеристики многоатомных спиртов
- Растворимость многоатомных спиртов в воде
- Получение многоатомных спиртов
- Физические свойства многоатомных спиртов
- Получение многоатомных спиртов
- Химические свойства многоатомных спиртов
- Видео:
- Многоатомные спирты | Химия 10 класс #26 | Инфоурок
Исследование растворимости многоатомных спиртов в воде
Многоатомные спирты – это класс органических соединений, в которых в молекуле содержится более одного гидроксильного (OH) радикала. Они являются важными веществами в различных областях, и их свойства, связанные с растворимостью в воде, получили особенное внимание со стороны научного сообщества. В данной статье будут рассмотрены физические и химические характеристики многоатомных спиртов и их растворимость в воде.
Растворимость многоатомных спиртов в воде является качественной характеристикой, определяющей, насколько хорошо эти соединения смешиваются друг с другом. Многие многоатомные спирты, такие как глицерин, пропиленгликоль и этиленгликоль, широко используются в промышленности и медицине. Например, глицерин является важным компонентом многих сиропообразных препаратов, молекула которого состоит из трех гидроксильных групп.
Причиной более высокой растворимости многоатомных спиртов в воде по сравнению с одноатомными спиртами, например, этанолом, является факт наличия большего числа гидроксильных групп в молекуле. Гидроксильные группы обладают поларностью и могут образовывать водородные связи с молекулами воды, что способствует их растворению в воде. Однако, не все многоатомные спирты одинаково растворимы в воде, так как существуют и другие физические и химические свойства, влияющие на растворимость.
Характеристика спиртов
Многоатомные спирты образуются при гидролизе и дегидратации глюкозы. Глюкоза — это многоатомный спирт, который содержится в организмах животных и является источником энергии для клеток. Окислением этилового спирта получают уксусную кислоту. Это реакция окисления спиртов, одноатомных или многоатомных, которая может происходить в организмах.
Многоатомные спирты имеют растворимость в воде. Их гидроксильные группы могут образовывать водородные связи с молекулами воды, что способствует образованию раствора. Растворимость зависит от молекулярной структуры спирта, числа и положения гидроксильных групп. Некоторые многоатомные спирты, такие как глицерин, могут образовывать растворы с большими количествами воды.
| Название спирта | Свойства |
|---|---|
| Этиловый спирт | Безцветная жидкость с характерным запахом, легко смешивается с водой и многими органическими растворителями. Вкус горький. |
| Глицерин | Бесцветная вязкая жидкость, сладкого вкуса. Хорошо растворим в воде и органических растворителях. |
| Гликоли | Бесцветные жидкости, обладающие сладким вкусом. Растворимость в воде зависит от числа гидроксильных групп и их положения в молекуле. |
Многоатомные спирты также могут использоваться для получения различных соединений, таких как глицераты и соли спиртов. Номенклатура многоатомных спиртов основана на числе гидроксильных групп в молекуле. Например, глицерин имеет три гидроксильные группы, поэтому его систематическое название — пропан-1,2,3-триол.
Окрашивание раствора многоатомных спиртов может быть качественной реакцией для определения их присутствия. Например, добавление к раствору многоатомного спирта некоторых соединений, таких как сульфат натрия, может вызвать окрашивание раствора в определенный цвет.
Растворимость многоатомных спиртов воде
Например, этиленгликоль, пропиленгликоль и глицерин, которые являются многоатомными спиртами, хорошо растворяются в воде. Они также широко используются в многих отраслях, например, в производстве качественной косметики, окрашивании тканей и получении различных химических соединений.
Некоторые из этих спиртов, такие как этиленгликоль и пропиленгликоль, можно использовать для получения ярко-синей краски. Для этого они могут быть окрашены солями меди, например, сульфатом меди. Реакция замещения происходит с гидроксильными группами многоатомных спиртов и образует комплексы меди, которые имеют характерный ярко-синий цвет.
Важно отметить, что не все спирты, содержащие гидроксильные группы, хорошо растворяются в воде. Например, этиловый спирт (этанол), который также имеет гидроксильную группу, растворяется в воде, но не так легко, как многоатомные спирты. Это объясняется различием в их физических и химических свойствах, таких как размер молекулы и плотность раствора.
Можно сказать, что многоатомные спирты более эффективны в растворении в воде по сравнению с одноатомными спиртами, такими как этиловый спирт. Это связано их структурой, в которой присутствуют несколько гидроксильных групп, что способствует лучшему взаимодействию с молекулами воды.
| Название спирта | Температура кипения (°C) |
|---|---|
| Этиленгликоль | -13 |
| Пропиленгликоль | 188 |
| Глицерин | 290 |
Свойства и получение многоатомных спиртов
Физические характеристики многоатомных спиртов
Многоатомные спирты обладают сходными физическими свойствами. Они обычно представляют собой бесцветные жидкости, имеющие характерный запах и вкус. Плотность многоатомных спиртов обычно выше, чем у воды, и они могут образовывать вязкие сиропообразные растворы.
Растворимость многоатомных спиртов в воде
Многоатомные спирты обладают высокой растворимостью в воде, особенно те, у которых имеются гидроксильные группы. Например, этиловый спирт, содержащий одну гидроксильную группу, хорошо смешивается с водой. В результате реакции гидролиза многоатомных спиртов в воде образуется смесь спиртов и их солей.
Некоторые многоатомные спирты, такие как глицерин, могут быть использованы в качестве растворителей для качественной анализа и окрашивания волокон. Например, глицерол ярко-синего цвета и используется в медицине для окрашивания животных организмов.
Получение многоатомных спиртов
Многоатомные спирты могут быть получены различными способами. Например, глицерин можно получить из растительных и животных масел путем гидролиза или переработки гликолей.
| Название спирта | Формула |
|---|---|
| Глицерин | C3H8O3 |
| Этиловый спирт | C2H5OH |
| Гликоли | CnH2n+2O2 |
Физические свойства многоатомных спиртов
Одним из важных свойств многоатомных спиртов является их растворимость в воде. Большинство многоатомных спиртов хорошо растворяются в воде благодаря гидрофильным группам (-OH), которые образуют водородные связи с молекулами воды. Это позволяет им образовывать гомогенные растворы с водой и использоваться в различных химических и биологических процессах.
Многоатомные спирты также имеют особенности во внешнем виде. Например, этиленгликоль, известный как антифриз, является бесцветной сиропообразной жидкостью. Качественной реакцией на присутствие этиленгликоля в жидкости является его окрашивание в ярко-синий цвет при взаимодействии с некоторыми химическими реагентами.
Глицерин, еще один многоатомный спирт, является вязкой безцветной жидкостью со сладким вкусом. Он используется в производстве пищевых добавок, лекарственных препаратов, косметики и других продуктов. Глицерин получают из жиров путем гидролиза в результате замещения этилового спирта на гидроксильные группы.
Другой многоатомный спирт — гликоли, также обладает сходными свойствами. Например, этиленгликоль, применяемый во многих отраслях промышленности, имеет низкую токсичность и хорошую растворимость в воде. Он используется в производстве пластмасс, резиновых изделий, моющих средств, красок и других продуктов.
Также многоатомные спирты, включая глицерин и этиленгликоль, используются в медицине, ветеринарии и других областях. Например, этиленгликоль широко применяется в качестве антифриза и антидота при отравлениях. Глицерин используется в лекарствах, косметических средствах и пищевых продуктах, так как он является безвредным для организма человека.
Окисление многоатомных спиртов происходит под воздействием кислорода, что приводит к образованию дополнительных функциональных групп. Например, окисление глицерина с помощью хлористого кальция приводит к получению глицерата натрия — сульфата меди, что является важным промежуточным соединением в некоторых химических процессах.
Таким образом, физические свойства многоатомных спиртов включают различные свойства растворимости, цвета, консистенции и запаха. Они играют важную роль во многих химических и биологических процессах, а также находят широкое применение в промышленности, медицине и других отраслях.
Получение многоатомных спиртов
Многоатомные спирты, такие как глицерин и этиленгликоль, получают путем гидролиза или окисления соответствующих соединений. Рассмотрим наиболее распространенные способы получения этих спиртов.
Гидролиз глицерина
Глицерин, или глицерол, является одним из наиболее распространенных многоатомных спиртов. Его можно получить путем гидролиза глицеридов – глицериловых эфиров – которые являются основными компонентами мастей и масел животного и растительного происхождения. Глицериды гидролизуются в присутствии щелочей или кислот с образованием глицерина и соответствующих солей (солей глицериновой кислоты).
Окисление пропилена
Этиленгликоль получают путем окисления пропилена – газообразного углеводорода – в присутствии катализаторов. Пропилен окисляют до первичного пропанола, который затем окисляют до этиленгликоля.
Далее в разделе будут рассмотрены свойства и характеристики многоатомных спиртов, а также их растворимость в воде.
Химические свойства многоатомных спиртов
Спирты обладают гидроксильной (-OH) группой, которая является причиной их различных химических свойств. Гидроксильные группы могут быть замещены другими атомами или группами атомов, что приводит к образованию различных многоатомных спиртов.
Многоатомные спирты, такие как гликоли (этиленгликоль, пропиленгликоль и др.) и глицерин, обладают высокой растворимостью в воде. Это обусловлено наличием нескольких гидроксильных групп в молекулах этих спиртов, которые могут образовывать водородные связи с молекулами воды.
Некоторые многоатомные спирты, такие как этиловый спирт, также растворимы в воде, но их растворимость ниже по сравнению с гликолями и глицерином. Это связано с менее количеством гидроксильных групп в молекуле этилового спирта.
Многоатомные спирты также могут использоваться в организмах животных и человека. Например, глюкоза является одним из основных источников энергии для организма и его получение происходит в результате дегидратации глицерата. Глицерин также используется в производстве косметических и фармацевтических препаратов.
Качественная растворимость многоатомных спиртов также может быть проиллюстрирована с помощью эксперимента. Например, при добавлении сульфата меди в раствор этиленгликоля, происходит образование ярко-синего осадка меди. Это обусловлено реакцией меди с гидроксильными группами гликоля.
Одной из характеристик многоатомных спиртов является их способность к дегидратации. Например, при нагревании глицерина происходит дегидратация и образуется вязкая сиропообразная жидкость. Это связано с потерей молекул воды из молекулы глицерина.
| Название | Формула | Гидроксильные группы | Растворимость в воде |
|---|---|---|---|
| Этиленгликоль | C2H6O2 | 2 | Высокая |
| Пропиленгликоль | C3H8O2 | 2 | Высокая |
| Глицерин | C3H8O3 | 3 | Высокая |
| Этиловый спирт | C2H6O | 1 | Средняя |
| Глюкоза | C6H12O6 | 6 | Высокая |
Видео:
Многоатомные спирты | Химия 10 класс #26 | Инфоурок
Многоатомные спирты | Химия 10 класс #26 | Инфоурок by ИНФОУРОК 19,572 views 6 years ago 5 minutes, 57 seconds