Методы и калькуляции по разбавлению кислоты водой.
Разбавление кислоты водой – известная процедура в химической лаборатории. При разбавлении кислоты водой мы изменяем состав исходного раствора. Доля воды в разбавленной кислоте определяет концентрацию раствора и его характеристики.
Для разбавления кислоты с применением воды можно использовать разные способы. Самым простым является добавление воды к кислоте в определенной пропорции. Существует массовая и моляльная концентрация кислоты, и при разбавлении водой нужно учесть эти особенности.
Для расчета необходимой доли кислоты и воды в разбавленном растворе можно использовать разные материалы. Например, при разбавлении серной кислоты (H2SO4) водой можно воспользоваться молекулярной массой и молярным весом вещества. Также можно применить массовые расчеты, основанные на отношении массы кислоты и объема раствора.
Давайте рассмотрим примеры расчетов разбавления кислоты водой. Когда мы хотим приготовить раствор с определенной концентрацией кислоты, нам необходимо знать исходную концентрацию, тогда мы можем вычислить необходимую массу кислоты для приготовления раствора. После этого мы можем посчитать количество воды, необходимое для достижения нужной концентрации. В других случаях, когда мы имеем исходное количество кислоты и хотим разбавить ее водой до нужной концентрации, мы можем вычислить необходимый объем воды для разбавления.
Взаимодействие кислоты с водой может сопровождаться дымлением или другим химическим процессом. Поэтому при разбавлении кислоты водой необходимо соблюдать осторожность и использовать защитные средства. Надо помнить, что водные растворы кислоты могут быть опасными и требуют правильного обращения.
Таким образом, разбавление кислоты водой – это важная процедура в химической практике. При правильных расчетах и применении соответствующих пропорций мы можем получить требуемую концентрацию и состав раствора.
Растворы кислот
Разбавление кислот водой проводят в несколько этапов. Сначала определяют массу кислоты, которую необходимо разбавить. Затем добавляют эту массу в воду, приливая ее постепенно. При этом важно соблюдать правило о добавлении кислоты в воду, а не наоборот. Правильное смешивание обеспечивает безопасность при взаимодействии кислоты с водой и предотвращает возможные взрывы или брызги.
Концентрация кислоты в растворе зависит от соотношения массы кислоты и объема воды. Чем больше масса кислоты относительно объема воды, тем более концентрированным будет раствор. Концентрация обычно выражается в процентах или молях. Например, раствор H2SO4 с концентрацией 1 М (молярный раствор) означает, что в 1 литре раствора содержится 1 моль серной кислоты. Другой способ выражения концентрации — процентная массовая доля кислоты. Например, раствор H2SO4 с концентрацией 10% означает, что в 100 граммах раствора содержится 10 грамм серной кислоты.
Для вычисления необходимой массы кислоты и объема воды при разбавлении используется правило пропорции. Например, если у нас есть 100 мл концентрированной серной кислоты с концентрацией 96% и мы хотим получить раствор с концентрацией 10%, то необходимо разбавить ее с добавлением определенного объема воды.
Основные способы концентрирования или разбавления кислоты включают использование дистиллированной воды, щелочи (например, раствора натрия или гидроксида магния) или добавление других растворов по мере необходимости.
Разбавление кислот водой расчет
Для разбавления кислоты поваренной в лаборатории можно воспользоваться методом приготовления раствора по массовой доле (ωрв-ва) или процентной концентрации.
Путем разбавления кислоты водой можно получить растворы различной концентрации. Пользуясь формулой концентрирования C1V1 = C2V2, где C1 и V1 — концентрация и объем исходного раствора, а C2 и V2 — концентрация и объем разбавленного раствора, можно определить объем воды, необходимый для разведения раствора до требуемой концентрации.
Для получения 1 литра разбавленного раствора, необходимо приготовить раствор концентрированной кислоты массой не более, чем 1/3 от массы кислоты, а затем разбавить его водой до требуемого объема.
Примеры расчетов разбавления кислот:
- Дана концентрация разбавляемой кислоты 50%, масса концентрированной кислоты 40 г. Необходимо разбавить раствор водой до 1 литра. Какое количество воды понадобится для разведения?
- Дана концентрация разбавляемой кислоты 30%, масса концентрированной кислоты 60 г. Необходимо приготовить 500 мл разбавленного раствора. Какое количество воды следует использовать для разбавления?
Решение: Используем формулу концентрирования C1V1 = C2V2. Заменяем известные значения: C1 = 50%, V1 = 1 — V2 (поскольку общий объем раствора 1 литр), C2 = 0% (так как конечная концентрация раствора должна быть 0%), V2 = 40 г / 1.5 г/мл = 26.7 мл. Получаем уравнение: 50% * 1 = 0% * (1 — 26.7). Находим ответ: V2 = 26.7 мл.
Решение: Используем формулу концентрирования C1V1 = C2V2. Заменяем известные значения: C1 = 30%, V1 = 0.5 — V2 (поскольку общий объем раствора 500 мл), C2 = 0% (так как конечная концентрация раствора должна быть 0%), V2 = 60 г / 1.5 г/мл = 40 мл. Получаем уравнение: 30% * 0.5 = 0% * (0.5 — 40). Находим ответ: V2 = 40 мл.
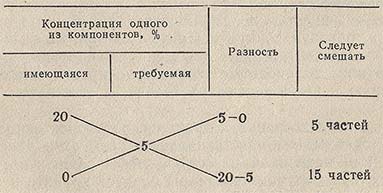
Таким образом, для разбавления кислоты водой приготовления различных растворов используются различные методы и расчеты. При помощи формулы концентрирования и учета массы и объема исходного раствора можно определить необходимое количество воды для получения требуемой концентрации раствора. Схема разбавления кислот водой может быть представлена в виде простого уравнения, позволяющего легко выполнить необходимые расчеты.
Требуемый раствор
Для получения требуемого раствора кислоты необходимо правильно рассчитать его состав и концентрацию. Расчеты можно выполнить, пользуясь массовой долей соли в растворе, массой раствора и плотностью раствора.
Схема расчета такая:
1. Найти массовую долю соли в растворе.
2. Определить массу раствора, необходимую для получения требуемой концентрации.
3. Вычислить массу соли, которую надо растворить.
4. Разогреть определенное количество воды до нужной температуры.
5. Добавить постепенно соль в разогретую воду до полного ее растворения.
Для примера, рассмотрим требуемый раствор соляной кислоты с концентрацией 20%. Нужно найти массу раствора, содержащего 40 г соли NaCl на 100 г раствора.
Виды растворов:
- Исходный раствор: 100 г раствора с 40 г соли NaCl.
- Требуемый раствор: массовая доля соли должна быть 20%.
Решение:
- Массовая доля соли в исходном растворе равна 40 г / 100 г = 0.4.
- Вычислим массу раствора, необходимую для получения требуемой концентрации:
X / (X + 100) = 0.2, где X — масса раствора.
Решаем уравнение и получаем X = 125 г.
- Вычислим массу соли, которую надо растворить:
0.4 * 125 г = 50 г. - Разогреем определенное количество воды до нужной температуры.
- Постепенно добавим 50 г соли в разогретую воду и доведем до полного растворения.
Таким образом, для получения требуемого раствора соляной кислоты с концентрацией 20% на 100 г раствора, берут 125 г воды и добавляют 50 г соли.
Аналогичные расчеты можно провести и для других видов растворов, руководствуясь характеристиками и концентрацией требуемого раствора. Например, для получения требуемого раствора щелочи с определенной концентрацией, необходимо учесть массовую долю растворенного вещества, плотность раствора и количество воды для разбавления.
Исходный раствор
В лаборатории часто проводят вычисления, связанные с разбавлением кислоты водой. Для приготовления растворов с известной массовой долей растворенного вещества в технических случаях пользоваться следующими выражениями:
1. Если для получения требуемого раствора кислоты в воде известна массовая доля растворенного вещества, то вычисление производится по формуле:
- Масса кислоты = Масса раствора * Массовая доля растворенного вещества
- Масса воды = Масса раствора — Масса кислоты
2. Такое вычисление применяется и в случае разбавления кислоты в воде. При разбавлении кислоты в воде сильное разогревание или разбавление поваренной солью необходимо записывать следующее: массу воды, требуемый объем 1 нормального раствора и количество растворенной кислоты, готовят, пользуясь следующими выражениями:
- Масса кислоты = Массовая доля растворенного вещества * Масса раствора
- Масса воды = Масса раствора — Масса кислоты
Такое правило применяется и при приготовлении раствора азотной кислоты из никеля.
Помощью этих выражений и исходного раствора можно проводить вычисления и расчеты с разбавлением кислот водой в лаборатории, а также в технических случаях.
Во всех случаях разбавления кислот в воде вес кислоты, растворенный в единицу объема воды, называется массовой долей растворенной кислоты в разбавленном растворе. При этом существует такое правило: только при массовой доле растворенного вещества более 1% можно пользоваться выражениями для водных растворов.
Поясним, что в разбавленных водных растворах кислоты по сравнению с неразбавленными кислотами массовая доля растворенного вещества всегда уменьшается. Доля растворенного вещества в растворе зависит от его разбавления, температуры воды, а также от вида растворенного вещества.
Таким образом, вычисление разбавления кислоты водой проводят с помощью исходного раствора, при этом следует учитывать физико-химические свойства материалов и правила приготовления растворов.
Видео:
разбавление кислоты
разбавление кислоты by Chemistry Program 16,893 views 7 years ago 1 minute, 51 seconds