- Как достичь нужной концентрации растворов с помощью добавления воды
- Формулы для пересчета концентраций растворов
- Разбавление растворов до нужной концентрации водой
- Требуемый раствор
- Исходный раствор
- Схема разведения раствора
- Разбавление растворов
- Как приготовить раствор с помощью «правила креста»
- Видео:
- Как правильно разбавлять концентрированные составы? Пропорции 1:10 или 1:20
Как достичь нужной концентрации растворов с помощью добавления воды
Приготовление растворов с определенной концентрацией – важная задача в химической лаборатории. Часто нам необходимо подготовить раствор определенной концентрации из данного исходного раствора. В таких случаях мы прибегаем к разбавлению растворов водой до необходимой концентрации. В данной статье мы рассмотрим процесс разбавления растворов и его особенности.
Для разбавления растворов необходимы вода и исходный раствор, массовая концентрация которого известна. В коллегии лаборантов расторопность и точность записывают соответствующими словами – концентрация воды известна всегда, а вот концентрация исходного раствора приготовить можно различными способами.
Во многих случаях необходимо разбавлять исходный раствор до небольших концентраций. Например, если у нас есть исходный раствор уксусной кислоты (в массовом процентном отношении) с содержанием вещества 60% и мы хотим приготовить раствор с концентрацией 2 г/моль, то мы можем представить следующую схему приготовления:
Формулы для пересчета концентраций растворов
При приготовлении растворов с нужной концентрацией вода может использоваться для разбавления уже имеющегося раствора до требуемой концентрации. Для расчета необходимого количества воды или исходного раствора достаточно знать формулы пересчета концентраций.
Основная формула для расчета количества раствора и воды при разбавлении растворов различной концентрации представлена следующим образом:
- Для разбавления раствора до нужной концентрации используется формула концентрации:
к1⋅м1 = к2⋅м2
где:
- к1 — концентрация исходного раствора;
- м1 — масса исходного раствора;
- к2 — требуемая концентрация разбавленного раствора;
- м2 — масса разбавленного раствора.
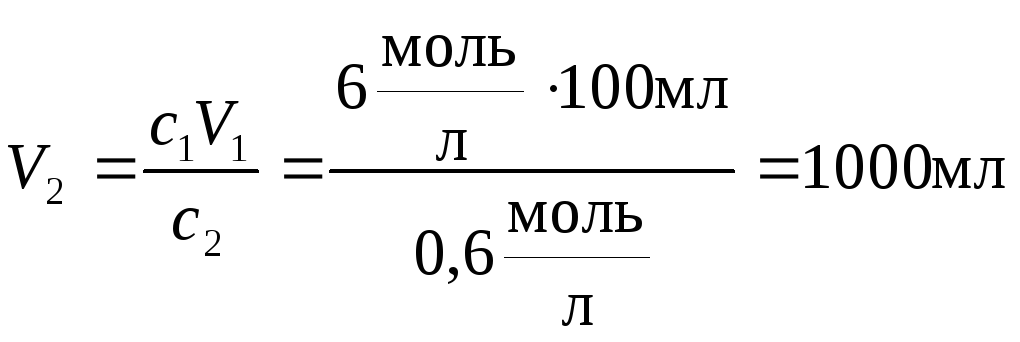
Например, если необходимо приготовить 100 мл раствора с концентрацией 2 моль/л из исходного раствора с концентрацией 4 моль/л, можно использовать формулу концентрации:
4⋅м1 = 2⋅100
м1 = 50
Таким образом, на 100 мл исходного раствора нужно взять 50 мл, а оставшиеся 50 мл заменить водой.
Если же необходимо разбавить изначальный раствор не водой, а другим раствором, то применяется формула пересчета концентраций «креста». Для этого нужно знать концентрации и объемы исходного и добавляемого растворов. Формула выглядит следующим образом:
к1⋅м1 = к2⋅м2
где:
- к1 — концентрация исходного раствора;
- м1 — масса исходного раствора;
- к2 — концентрация добавляемого раствора;
- м2 — масса добавляемого раствора.
Например, если необходимо приготовить 100 мл раствора с концентрацией 2 моль/л из исходного раствора с концентрацией 4 моль/л и добавочного раствора с концентрацией 1 моль/л, можно использовать формулу пересчета концентраций:
4⋅м1 = 2⋅100
где м1 — масса исходного раствора и m2 — масса добавляемого раствора
1⋅м2 = 2⋅100
где м2 — масса добавляемого раствора и m1 — масса исходного раствора
Таким образом, чтобы приготовить раствор с концентрацией 2 моль/л из исходного раствора с концентрацией 4 моль/л и добавочного раствора с концентрацией 1 моль/л, нужно взять 50 мл исходного раствора и 50 мл добавочного раствора.
Такие же правила пересчета концентраций применяются и в других случаях, когда нужно приготовить раствор с требуемой концентрацией из исходных растворов различных концентраций.
Теперь, зная формулы пересчета концентраций, вы можете с легкостью рассчитать необходимое количество раствора и воды для приготовления растворов с нужной концентрацией.
Разбавление растворов до нужной концентрации водой
Для расчета требуемого количества исходного раствора и воды для разбавления можно использовать формулу:
V1C1 = V2C2
где V1 — объем исходного раствора, C1 — концентрация исходного раствора, V2 — объем воды, C2 — концентрация требуемого раствора.
Например, если вам требуется разбавить 50 мл концентрированного уксуса (концентрация которого 1 г/мл) водой до концентрации 0.5 г/мл, можно взять второй сосуд, в котором уже есть определенное количество воды. При помощи пересчета и использования формулы, можно определить необходимое количество уксуса и воды для разбавления.
Смешайте исходный раствор уксуса с водой во втором сосуде при помощи колбы для общей растворимости. После разбавления общий раствор будет иметь концентрацию, которая достигнет значения 0.5 г/мл.
Разбавление растворов до нужной концентрации водой — это важный процесс, который могут использовать не только хомо сапиенсы, но и наши коллегии из других видов животного мира.
Требуемый раствор
Для получения требуемого раствора с определенной концентрацией вещества необходимо применить процесс разбавления исходного раствора с помощью воды. Данная процедура позволяет приготовить раствор с меньшей концентрацией путем добавления определенного количества воды.
Для расчета необходимого количества воды требуется знать исходную концентрацию раствора и желаемую концентрацию в требуемом растворе. Если известны масса раствора и концентрация вещества в нем, то для редкостей можно использовать формулу:
маха = мих*(Сих — Сх)/(Смакс -С)
где маха — масса необходимой аликвоты исходного раствора, мих — масса исходного раствора, Сих — его концентрация, Сх — концентрация растворенного вещества в требуемом растворе, Смакс — максимальная концентрация исходного раствора для данного вещества.
В некоторых случаях, если известны объем и концентрация исходного раствора, а также требуемая концентрация, можно использовать формулу:
Vаха = Vих*(Сих — Сх)/(С — Сх)
где Vаха — объем необходимого аликвота исходного раствора, Vих — объем исходного раствора, Сих — его концентрация, Сх — концентрация растворенного вещества в требуемом растворе, С — требуемая концентрация раствора.
После получения необходимой аликвоты исходного раствора, ее следует разбавить взятым объемом воды до требуемого объема смеси. Для этого аликвоту помещают в сосуд и добавляют воду до необходимого объема, при этом хорошо перемешивая раствор.
Необходимый раствор получается путем разведения исходного раствора до нужной концентрации с помощью воды. Важно соблюдать указанные правила и формулы для получения точного и требуемого раствора.
Исходный раствор
Иногда перед требуемым количеством раствора необходимо разбавить концентрированный раствор водой до нужной концентрации. Разбавление может быть проведено в случаях, когда у нас есть раствор определенной концентрации, и мы хотим приготовить смесь с меньшей концентрацией, или когда у нас есть раствор определенного количества, и мы хотим приготовить смесь в большем объеме. Во всех случаях необходимо знать количество раствора, которое мы взяли и количество воды, необходимое для разбавления.
Для определения количества раствора и воды в смеси используется схема разбавления растворов. Пусть у нас дан исходный раствор с концентрацией С1 гмоль/литр (моль/литр) и объемом V1 литров. Требуется приготовить разбавленный раствор с концентрацией С2 гмоль/литр (моль/литр) и объемом V2 литров.
Для разбавления растворов используются следующие правила:
- Записываем данные исходного раствора: концентрацию С1 и объем V1.
- Записываем необходимую концентрацию С2.
- Определяем разность концентраций ΔС = С1 — С2.
- Записываем объем V2 разбавленного раствора.
- Рассчитываем необходимое количество воды для приготовления разбавленного раствора по формуле: Vводы = V2 * ΔС / С2.
Таким образом, чтобы приготовить разбавленный раствор необходимой концентрации, можно использовать схему разбавления растворов. Этот подход позволяет получить требуемую концентрацию, используя исходный раствор, воду и правильные пропорции.
Схема разведения раствора
Для получения требуемой концентрации раствора необходимо правильно разбавить исходный раствор водой. Схема разведения раствора поможет вам выполнить эту задачу без ошибок.
1. Известна концентрация исходного раствора, которая обозначена как С1 и выражается в моль/л или г/л. Также известна его масса, которая обозначается как М1 и выражается в г.
2. Необходимо определить массу вещества, которую требуется получить в конечном разбавленном растворе. Эта масса обозначается как М2 и выражается в г.
3. Рассчитаем необходимый объем исходного раствора, который требуется для приготовления нужной массы вещества в конечном разбавленном растворе. Для этого воспользуемся формулой:
- В случае массовых концентраций (г/л): V1 = М2 / С1
- В случае мольных концентраций (моль/л): V1 = n2 / C1
где V1 — объем исходного раствора, выраженный в литрах; n2 — количество вещества, выраженное в молях.
4. Приготовьте аликвоту исходного раствора объемом, рассчитанным по формуле из пункта 3.
5. Добавьте нужное количество воды в сосуд с аликвотой исходного раствора, чтобы получить концентрацию, требуемую в конечном разбавленном растворе. Разность объема смеси и объема исходного раствора должна быть равна объему добавленной воды.
6. Записывайте все данные о разведении раствора, включая массу исходного раствора, его концентрацию, объем исходного раствора и добавленной воды. Эти данные могут понадобиться для дальнейших расчетов или для публикации результатов исследования в научном журнале.
С помощью данной схемы разведения растворов вы сможете легко и точно приготовить нужный разбавленный раствор. Учтите, что правила разбавления могут отличаться в зависимости от конкретного вещества, поэтому перед приготовлением следует ознакомиться с указаниями в коллегии по данному веществу или в специальных справочниках.
Разбавление растворов
Когда требуется приготовить раствор определенной концентрации, но имеется раствор другой концентрации, его можно разбавить с использованием воды. Процесс разбавления растворов осуществляется путем добавления воды в колбу с концентрированным раствором, чтобы получить раствор с меньшей концентрацией.
Для разбавления растворов нужно знать исходную концентрацию концентрированного раствора и требуемую концентрацию разбавленного раствора. Во многих случаях разность концентраций раствора и разбавленной воды может быть выражена в процентах.
Формула для пересчета концентраций растворов выглядит следующим образом:
(масса раствора A) * (концентрация раствора A) = (масса раствора B) * (концентрация раствора B)
Приготовление разбавленного раствора можно произвести следующим образом:
- Взять колбу, в которой будет происходить разбавление раствора.
- Записать в журнал исходную концентрацию раствора, которую нужно разбавить, и требуемую концентрацию разбавленного раствора.
- На основании данных из журнала вычислить массу концентрированного раствора, которую нужно взять для получения требуемого разбавленного раствора.
- Взять указанную массу концентрированного раствора и добавить в него воду до получения желаемого объема разбавленного раствора.
- Тщательно перемешать смесь в сосуде, чтобы обеспечить равномерное распределение растворенного вещества.
- Убедиться, что концентрация разбавленного раствора соответствует требуемому значению, записать полученные данные в журнал.
Когда разбавляем раствор, мы должны знать только исходную концентрацию раствора и требуемую концентрацию разбавленного раствора. Расчет массы концентрированного раствора и объема воды проводится по формуле разности концентраций исходного и разбавленного растворов.
Примером разбавления растворов может быть приготовление 1% уксусной кислоты из 5% раствора кристаллогидрата. Если взять один грамм кристаллогидрата, то масса полученного раствора составит 100 г, а масса воды — 99 г. Таким образом, после разбавления 5% раствора кристаллогидрата получится 1% раствор уксусной кислоты.
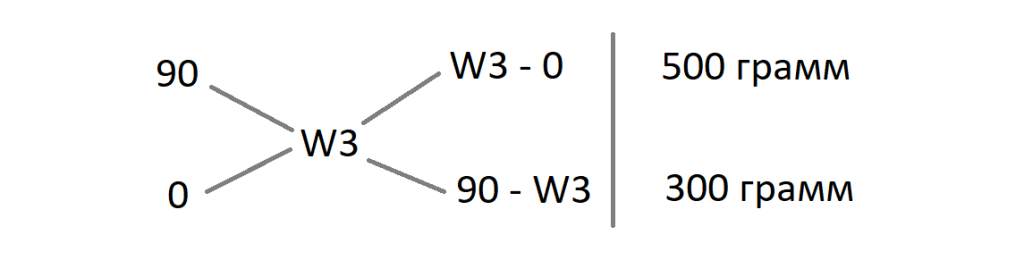
Как приготовить раствор с помощью «правила креста»
При разбавлении концентрированных растворов до нужной концентрации водой можно использовать одно из правил, известное как «правило креста». Это правило позволяет определить необходимый объем концентрированного раствора и воды для достижения заданной концентрации раствора.
Для примера, рассмотрим ситуацию, когда необходимо приготовить раствор данного вещества с определенной концентрацией. Предположим, что вам нужно приготовить раствор, содержащий 0.1 г вещества в 100 мл воды.
Начните с расчета массы вещества, которую необходимо взять из исходного концентрированного раствора. Для этого умножьте необходимую концентрацию (в данном случае 0.1 г) на объем воды (в данном случае 100 мл), и разделите на концентрацию в исходном растворе. Допустим, изначальная концентрация раствора равна 1 г/мл, тогда необходимая масса вещества будет равна:
Масса вещества = (0.1 г / 1 г) * 100 мл = 10 г.
Теперь рассчитаем объем исходного раствора, который нужно взять для приготовления нужного раствора. Для этого воспользуемся формулой:
Объем исходного раствора = (Масса вещества / Концентрация исходного раствора) * 1000;
Рассчитаем:
Объем исходного раствора = (10 г / 1 г/мл) * 1000 = 10000 мл = 10 л.
Таким образом, чтобы приготовить раствор с необходимой концентрацией, необходимо взять 10 л исходного раствора и разбавить его водой до объема 100 мл.
Когда вы уже взяли необходимое количество исходного раствора, добавьте оставшийся объем воды до нужного значения (в данном случае до 100 мл).
Таким образом, вы приготовите раствор с необходимой концентрацией при помощи «правила креста». Этот метод хорошо подходит для разбавления растворов и определения необходимых объемов вещества и растворителя.
Видео:
Как правильно разбавлять концентрированные составы? Пропорции 1:10 или 1:20
Как правильно разбавлять концентрированные составы? Пропорции 1:10 или 1:20 by 1carmarket 38,465 views 1 year ago 2 minutes, 51 seconds