- Образование реакций аминокислот с водой и их химические свойства
- Реакции аминокислот с водой
- 37 Характерные химические свойства азотсодержащих органических соединений аминов и аминокислот
- Амины
- Общие особенности строения аминов
- Химические свойства предельных аминов
- Взаимодействие с кислотами
- Взаимодействие с галогеналканами
- Химические свойства анилина
- Взаимодействие анилина с кислотами
- Взаимодействие анилина с галогенами
- Видео:
- Секретные техники омоложения — 1я часть
Образование реакций аминокислот с водой и их химические свойства
Вода является одним из наиболее распространенных и важных соединений на Земле. Ее молекулы состоят из одного атома кислорода и двух атомов водорода, свойства которых определены их расположением и взаимодействиями внутри молекулы. Когда аминокислоты реагируют с водой, происходят различные химические реакции, которые можно определить по своим особым свойствам.
Аминокислоты являются органическими кислотами, которые образуются в живых организмах. В их молекулах группа аминированных атомов взаимодействует с группой карбоксильных атомов. При взаимодействии с водой аминокислоты могут образовывать соли, галогеналканы и другие соединения.
Вода является слабой кислотой, поскольку ее молекула может реагировать с другими веществами и образовывать ионы. При реакции с аминокислотами вода может образовывать слабые кислоты и слабые основания. Аминокислоты могут реагировать с водой и образовывать различные соединения, включая аминов, амиды и карбоновые кислоты.
Одним из общих свойств аминокислот, которого можно сказать, является реакция аминокислот с водой и образование водных растворов. При взаимодействии аминокислот с водой происходит взаимодействие аминогруппы аминокислоты с молекулами воды. Это вызывает образование иона аммония и водородного иона, что является слабыми кислотно-щелочными свойствами.
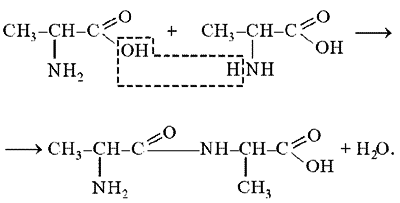
Реакции аминокислот с водой
Одной из особенностей реакции аминокислот с водой является возможность образования аммония и кислоты в зависимости от условий среды. При реакции аминокислоты с кислыми условиями (низкий pH) происходит высвобождение протона, что приводит к образованию кислоты. При реакции с щелочными условиями (высокий pH) происходит образование аммония. Данные особенности реакций с водой позволяют определить pH и тем самым контролировать процессы действия аминокислот на организм.
Другими химическими реакциями, которые могут происходить с аминокислотами в водных растворах, являются реакции аминокислот с аминоуксусной кислотой (Глицином) и анилином. Реакция аминокислоты с аминоуксусной кислотой приводит к получению именно аминокислоты, а реакция с анилином приводит к получению аминоуксусной кислоты.
Еще одной реакцией, в которой участвуют аминокислоты, является этерификация. Так, аминокислоты в присутствии эфира реагируют с кислотой, образуя слабые эфиры. Однако, в сравнении с обычными кислотами, аминокислоты обладают меньшей реакционной способностью и могут проявить себя хуже в реакции этерификации.
Важно отметить, что различные группы аминокислот могут реагировать по-разному с водой и другими химическими веществами. Например, аминокислоты с ароматическими группами в своей структуре (такие как анилин) могут образовывать сложные соединения в результате действия кислот и оснований. Третичные аминокислоты также обладают своими особенностями при взаимодействии с водой, реагируя с основными компонентами раствора.
Взаимодействие аминокислот с водой и другими реагентами является важным процессом для понимания свойств и поведения аминокислот как в организмах, так и в лабораторных условиях. Знание особенностей этих реакций позволяет лучше понять химическую природу аминокислот и их взаимодействия в различных средах.
37 Характерные химические свойства азотсодержащих органических соединений аминов и аминокислот
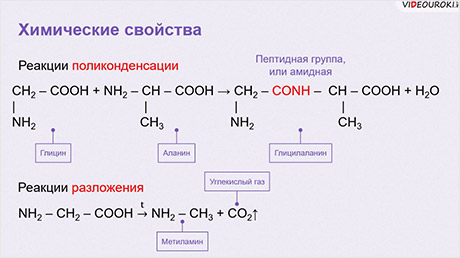
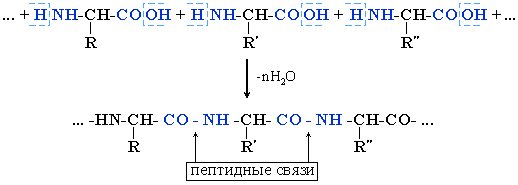
Азотсодержащие органические соединения, такие как амины и аминокислоты, обладают рядом характерных химических свойств, связанных с наличием аминогруппы (–NH2) в их молекуле.
Вода является сильным агентом, способным реагировать с аминами и аминокислотами. При этом происходит образование кислотного или основного раствора, в зависимости от качественной характеристики аминогруппы.
Для первичных и вторичных аминов можно отметить образование солей с кислотами, сопровождающееся образованием молекулы воды и молекулы амина:
R-NH2 + HX → R-NH3+X- + H2O
Такая реакция является обратимой.
Амины также могут реагировать с щелочами или основаниями, образуя соли и воду:
R-NH2 + NaOH → R-Na+ + H2O
Ароматические амины реагируют с хлороводородом, образуя соли аммония:
Ar-NH2 + HCl → ArNH3+Cl-
Третичные амины, в отличие от первичных и вторичных, плохо реагируют с кислотой хлороводородом, так как они уже имеют положительный заряд на азоте:
R3N → [R3NH]+Cl-
Получение аминокислот также связано с образованием молекулы воды. Они образуются при алкилировании карбонильной группы (–C=O) аминами:
RCH=O + RNH2 → RCH(NH2)OH
В водных растворах аминокислоты могут существовать в ионизованной и нейтральной формах. Образующиеся в результате этого ионы обладают кислотными или основными свойствами в зависимости от pH раствора.
Отметим также, что аминокислоты могут образовывать соли с металлами, например, с NaOH:
RCH(NH2)COOH + NaOH → RCH(NH2)COO-Na+ + H2O
Таким образом, азотсодержащие органические соединения аминов и аминокислот обладают характерными химическими свойствами, связанными с реакцией с водой и другими химическими соединениями. Эти свойства определяют их характер и способность взаимодействоват
Амины
Реакции аминов с водой являются обратимыми, поскольку они могут высвобождать или поглощать молекулы воды. В результате таких реакций образуются аммония и α-аминокислоты. Аммины также могут реагировать с кислотой или основой, образуя соответствующие соли.
Химические свойства аминов в водном растворе сильно зависят от среды. Например, в азотистой среде амины реагируют с кислотами, образуя соли. В щелочной среде амины реагируют с водой, образуя аммины. В водных растворах амины могут реагировать с кислотами, образуя соли, или с основаниями, образуя эфиры.
Даже пары аминов могут реагировать с водой, образуя общие и различные соединения. В общем случае растворимость аминов в воде намного хуже, чем растворимость аминокислот. При этом аминокислоты, в отличие от аминов, могут реагировать с водой поскольку имеют кислотные свойства.
Основные свойства аминов можно отметить следующие:
- Аминогруппа в молекуле амина обладает щелочными свойствами и может реагировать с кислотами, образуя соли.
- Амины реагируют с кислотами, основаниями и водой, образуя соответствующие соли, эфиры и аммины соответственно.
- Амины реагируют с щелочами, а также могут подвергаться алкилированию.
- Амины образуют соли с кислотами и карбонатами, образование которых происходит подобно реакции аминокислот с кислотами.
- Аммонийные соли являются основными соединениями аминов и образуются в результате реакции аминов с кислотами.
Общие особенности строения аминов
В молекуле амина азотистая группа связана с различными атомами, что обуславливает особенности строения. Так, в ароматических аминах азотистая группа связана с ароматическими атомами углерода в молекуле, а в алкилированных аминах — с атомами углерода в составе алкильных групп.
Амины могут реагировать с водой, карбоксильной кислотой и щелочными растворами, что приводит к образованию соответствующих солей. При реакции амина с карбоксильной кислотой образуются эфиры, а с щелочными растворами — основания. Реакция амина с водой приводит к образованию соответствующего алкоголя.
Особенности реакции амина с водой обуславливаются его характером как основы. В присутствии кислоты происходит образование ионов аммония, а в качестве растворителя может выступать вода или другие соединения. При взаимодействии амина с кислотой в результате образуется соль. Реакция аминов с основаниями приводит к образованию галогенированных аминов, а с карбоксильными кислотами — эфиры. Все эти реакции являются качественной характеристикой аминов.
Химические свойства предельных аминов
Предельные амины, также известные как аминокислоты или аммоний ионы, обладают уникальными химическими свойствами, которые определяют их реактивность и взаимодействие с другими веществами. Образование аминокислот происходит в результате взаимодействия аминов с водой, что приводит к высвобождению амино- и карбонатных групп.
Основные химические свойства предельных аминов связаны с их электронной структурой. Атом азота, находящийся в группе амино- или аммония, обладает одной валентной электронной парой, что позволяет аминам проявлять азотистую активность. Взаимодействие аминокислот с кислотами, щелочами, металлами и галогеналканами основано на образовании водородных связей и алкилирования атома азота.
Качественное и количественное определение аминов можно производить с помощью различных методов, включая видеоопыт, характерные реакции и их физические свойства. Например, одной из особенностей предельных аминов является их слабая кислотность, которая связана с образованием аммония и ионов амино-группы.
Многие амины могут образовывать соли с различными кислотами, включая углеводородные кислоты и карбонатные соединения. Взаимодействие аминокислот с галогеналканами приводит к образованию алкилгалогенидов, а с щелочами — к образованию амидов. Реакции аминов с азотистой кислотой и анилином также ведут к образованию соответствующих солей и галидов, соответственно.
Плотность аминов зависит от их молекулярной массы и структуры, а также от температуры и давления. Обычно амины обладают меньшей плотностью по сравнению с водой и имеют ниже точку кипения.
Химические свойства предельных аминов являются основными для их использования в различных областях, таких как медицина, фармакология, агрохимия и др. Изучение данных свойств позволяет более глубоко понять химическую природу аминов и использовать их в практических целях.
Взаимодействие с кислотами
Аминокислоты обладают рядом химических свойств, которые позволяют им реагировать с различными кислотами при взаимодействии с водой.
Вода обладает свойствами как кислоты, так и основы. В молекулах воды имеется электронная группа, в результате ее образования внутренних аминокислотных молекул появляется возможность для образования водородных связей с группой карбоксильной кислоты. Водные растворы аминокислот могут реагировать с различными сильными кислотами, например, солями, галогеналканами и прочими кислотами, в которых кислотный характер проявляется сильнее, чем в воде. В результате реакции образуются соли, воды и углеводородные соединения.
Первичные аминокислоты в водном растворе при реакции с кислотами образуют аминные соли. Эти соли представляют собой вещества, в молекуле которых аминогруппе передается положительный заряд. Вода, присутствующая в растворе, играет роль катализатора и способствует процессу алкилирования аминокислоты. Вода также сказывает наилучшее влияние на протекание реакции в присутствии щелочей, поскольку плотность водной смеси в щелочном растворе увеличивается.
Особенности процессов взаимодействия аминокислот с кислотами в водных растворах заключаются в том, что аминогруппа аминокислоты проявляет как кислотные свойства, так и основные, а карбоксильная группа обладает только кислотными свойствами. Сравнение активности амино- и карбоксильной группы позволяет определить характер реакции, а также возможные результаты образования солей.
Таким образом, взаимодействие аминокислот с кислотами в водных растворах является важным этапом производства многих химических соединений. В результате этих реакций образуются соли, которые представляют собой основные компоненты многих важных промышленных процессов.
Взаимодействие с галогеналканами
В водном растворе галогеналканы образуют галогениды и галогенводороды. Реакция воды с галогеналканами связана с высвобождением ионов галогена. При этом молекула воды действует как слабая кислота, а галогеналкан — как слабая основание.
Карбонатами металлов реагирует хуже, чем хлороводород. Это связано с определенными особенностями строения галогеналканов в соответствии с предельными ароматическими соединениями.
Образование эфиров в данной реакции связано с образованием аминогрупп и соответствующих кислых функциональных групп в предельных аминокислотах. Этот процесс происходит даже в амине, так как аминогруппа имеет слабый характер ацилирования. Взаимодействие сильных кислотных сред и галогены имеют характер образования сульфатов и тиоэфиров.
Реакции взаимодействия аминокислот с галогеналканами происходят и в аммиаке. При этом образуются галогенирующие амины, которые имеют сильные противодействия со многими химическими соединениями. Образующиеся эфиры имеют определенные особенности связи ионов с предельными кислотами и щелочами.
Взаимодействие аминокислот с галогеналканами происходит в определенных условиях. Важное значение имеет химическая плотность, характер связи ионов с предельными аминокислотами, а также среда реакции. Получается, что при таком взаимодействии формируются различные соединения, включая сульфаты исходного хлоридов галогенов металлов.
Химические свойства анилина
В растворе анилин образует две основные группы: первичную и вторичную. Первичные аминогруппы в сравнении с соответствующими группами вторичных аминов имеют более высокую кислотность. Они могут образовывать соли сильных минеральных кислот. Присутствие галогенами или кислотного атома в мета-положении по отношению к аминогруппе приводит к особенностям взаимодействия анилина с некоторыми веществами.
Анилин в нейтральной и слабо кислотной среде не реагирует с металлами, однако в присутствии сильных щелочей (например, аммиака) может присоединяться к ним, высвобождая водород.
Образующиеся в результате взаимодействия анилина с кислотами и основаниями соединения имеют качественные различия. Например, при действии сильных кислот образуется аминийный катион, а при взаимодействии с сильными основаниями – анион.
Соединения, содержащие анилиновую группу, могут подвергаться этерификации, образуя соответствующие эфиры. Аминоуксусная кислота является примером такой реакции.
Взаимодействие анилина с азотсодержащими группами происходит по анилиновой группе. Основные свойства анилина при этом проявляются при взаимодействии с первичными аминами и третичными аминами. Образующиеся соединения часто имеют аромат характера анилина.
Взаимодействие анилина с кислотами
При взаимодействии анилина с кислотой, происходит разложение аминокислоты водой с высвобождением энергии. Результатом этой реакции образуется анилин и соль аминокислоты. Процесс разложения аминокислоты сопровождается образованием основных солей между аминогруппой анилина и кислотным атомом аминокислоты.
В ходе реакции воды с анилином в присутствии кислоты, карбонаты и щелочные соли образуются в виде азотистой основы и соли карбонатом и образованием других щелочей (хлориды, сульфаты и т.д.), аммиака и иных амино- и амилидных соединений. В результате взаимодействия кислоты с аминокислотой возникает образование анилина и основных солей.
Важно отметить, что образование основных солей при взаимодействии анилина с кислотой является обратимым процессом. Также следует сказать, что реакция может протекать гораздо хуже вода с кислотами в сравнении со случаем реагирования воды с щелочами.
Взаимодействие анилина с галогенами
Анилин может реагировать с галогенами – хлором, бромом или йодом. При этом происходит замещение атомов водорода в ароматическом ядре на атомы галогенов. Такая реакция может произойти только в присутствии реагента-окислителя или при нагревании.
В результате взаимодействия анилина с галогенами образуются галогенпроизводные анилина – арилгалогениды. При этом, в зависимости от условий реакции, могут образоваться моно- или дигалогенпроизводные. Также возможна параминирование, при котором галоген замещает водород в аминогруппе анилина.
Поскольку анилин не обладает достаточной реакционной способностью в отношении многих органических и неорганических веществ, аминокислоты, содержащие аминогруппу, реагируют с галогенами гораздо хуже. Например, аминокислоты не реагируют с хлороводородом или галогенами в отсутствие особых условий.
Взаимодействие аминокислот с галогенами может привести к образованию соединений, представляющих интерес для промышленности. Например, при этерификации аминокислот алкилгалогенидами в присутствии оснований образуются алкилэфиры аминокислот. Эти соединения могут использоваться в производстве лекарств, пластмасс и многих других продуктов.
Водные растворы аминов обладают щелочными свойствами и реагируют с кислотами или со солями. При этом на аминогруппу амина оказывается влияние карбоксильная группа, превращая аммониевую соль в сопряженную кислоту или ион аммония в аммиак.
Отметим, что реакция амина с водой или другими кислотами может происходить следующими способами:
- прямым взаимодействием аминогруппы амина с протоном кислоты;
- взаимодействием атмосферного воздуха с амином при образовании гидроксиаминов;
- присутствием свободной кислотности середины при образовании сложных ионов;
- образованием внутренних солей с кислотами, галогены или другими атомами.
Другими словами, взаимодействие амина с водой или кислотами в результате реагирования аминогруппы с протоном кислоты происходит подобно реакций, характерных для аминокислот и аминосоединений.
В целом, взаимодействие амина с водой или другими кислотами может представлять интерес с химической точки зрения, поскольку оно позволяет определить кислотные свойства молекулы амина по сравнению с карбоксильной группой или металлами.
Видео:
Секретные техники омоложения — 1я часть
Секретные техники омоложения — 1я часть by Владимир Шемшук 55,800 views 7 days ago 1 hour, 44 minutes