- Исследование взаимодействия ксилолов с бромной водой: описание реакций и их механизмов
- Химические свойства аренов
- Химические свойства аренов
- 1 Реакции присоединения
- 11 Гидрирование
- 12 Хлорирование аренов
- 2 Реакции замещения
- 21 Галогенирование
- 22 Нитрование
- 23 Алкилирование ароматических углеводородов
- 24 Сульфирование ароматических углеводородов
- 3 Окисление аренов
- 31 Полное окисление – горение
- Видео:
- Реакция сульфонирования
Исследование взаимодействия ксилолов с бромной водой: описание реакций и их механизмов
Ксилол является одним из наиболее распространенных изомеров толуола. Он содержит два метильных заместителя и один этильный заместитель в ароматическом кольце. Основные химические свойства ксилола определяются наличием этих заместителей и их влиянием на реакционную способность ксилола в ароматическом кольце.
Ксилол обладает способностью к сульфированию и нитрованию в кольце. При условиях нейтральной кислоты происходит замещение атома водорода на группу — SO2NH2, образуя соответствующую соль. При воздействии азотной кислоты образуются нитрофенолы.
Реакции ксилолов с бромной водой также происходят в ароматическом кольце. Под воздействием бромной воды происходит алкилирование ксилола, при котором этильный заместитель присоединяет бром и образуется соответствующий продукт. Действие бромной воды приводит к присоединению брома к ароматическим кольцам в метильных и этильных позициях. В результате образуется 1,4-дибром-3-метилбензол и 1,4-дибром-2-метилбензол.
Химические свойства аренов
Бензол, который является прототипом арены, имеет формулу C6H6 и является наиболее известным представителем этого класса соединений. Бензол является достаточно устойчивым соединением и плотность его составляет около 0,88 г/см3. Он не окисляется на воздухе и не растворяется в воде.
Однако бензол может подвергаться замещению атомов водорода различными заместителями. Например, в хлорировании бензола присутствие катализаторов, таких как хлорное железо (FeBr3), приводит к замещению атомов водорода хлором. В результате образуются галогенированные ароматические углеводороды, такие как хлорбензол.
Еще одной важной реакцией, которую могут претерпевать арены, является нитрирование. В этой реакции арен присоединяет группу NO2 (нитрогруппу) в присутствии азотной кислоты. Нитрирование бензола, например, приводит к образованию нитробензола.
Помимо замещения атомов водорода, арены могут подвергаться и другим реакциям. Например, при гидрировании ароматических углеводородов, таких как стирол, происходит присоединение молекулы водорода к двойной связи углерода. В результате образуются гидроароматические углеводороды, такие как мета-хлортолуол.
Также арены могут быть подвержены окислению, например, в результате взаимодействия с кислородом или окислительными средами. Одним из примеров является окисление бензола серной кислотой, при котором образуется бензольная кислота (C6H6 + 6H2SO4 → C6H5COOH + 6SO2+ 6H2O).
Таким образом, арены обладают разнообразными химическими свойствами, включая замещение атомов водорода, галогенирование, нитрирование, гидрирование, окисление и другие реакции, которые могут проводиться в соответствии с общей химической структурой арены.
Химические свойства аренов
Бензольное кольцо в аренах может быть замещено различными группами. Например, вводя нитро-группу (-NO2) в альфа-положение карбонильного остова алканальных гомологов, получают альдегиды ароматической серии. При хлорировании ароматических углеводородов хлором в присутствии фторида железа(III) (FeBr3) происходит замещение водорода атомами хлора.
Арены могут быть подвергнуты окислению в виде полного окисления бензольного ядра до образования соответствующей бензойной кислоты. Также арены могут быть хлорированы в присутствии хлора в нейтральной среде, при этом происходит замещение водорода атомами хлора.
Сульфирование ароматических соединений, например, этилбензола и толуола, является реакцией, в ходе которой происходит замещение атома водорода группой сульфо. При гашении серной кислотой образуются продукты сульфо-замещения. Также арены могут претерпевать химические реакции, такие как сульфирование, нитро-, бромирование, особенно в составе соединений аренового типа, например, в орто- и мета-положении.
Арены могут также гореть при нагревании, образуя соль калия (K2C6H6) и образуя связи с кислородом воздуха, например, при окислении бензола или его гомологов. Химические свойства аренов определяются характером связей в бензольном кольце и заместителями.
Таким образом, химические свойства аренов проявляются в их взаимодействии с различными реактивами и возможностью замещения атомов водорода, что открывает широкий спектр перепрограммирования ароматических соединений.
1 Реакции присоединения
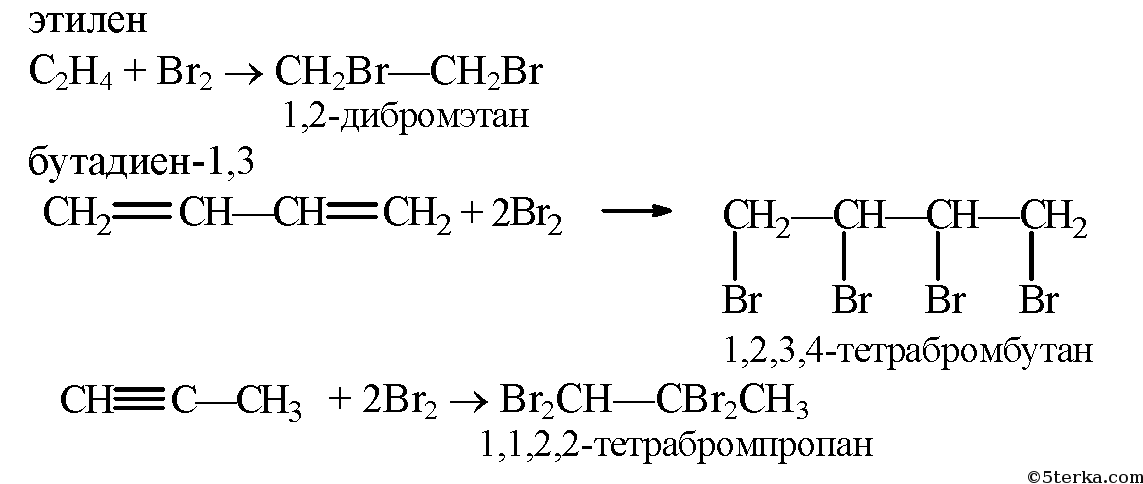
Одним из примеров таких реакций присоединения является бромирование. При этом происходит присоединение брома к кольцу аренов, в данном случае толуола, под действием бромной воды. Формула реакции выглядит следующим образом:
2 C6H5CH3 + 3 Br2 → C6H5CH2Br3 + 3 HBr
Процесс бромирования может также привести к образованию мета- и паравеществ толуола.
Кроме того, ксилолы могут претерпевать хлорирование и гидрирование. Например, при хлорировании ксилолов получается мета- и паравещества хлортолуола:
2 C6H6CH3 + Cl2 → C6H5CH2Cl + HCl
А при гидрировании толуол может превратиться в стирол в присутствии катализаторов, таких как железо или никель:
C6H5CH3 + H2 → C6H5CH2CH3
Также ксилолы могут претерпевать сульфирование, окисление и полимеризацию в присутствии соответствующих реагентов. Например, окисление толуола перманганатом калия приводит к образованию бензольной кислоты:
C6H5CH3 + KMnO4 + H2O → C6H5COOH + KOH + MnO2
Таким образом, реакции присоединения ксилолов с бромной водой представляют собой важные химические процессы, которые могут привести к образованию различных продуктов с высокой степенью замещения в ароматическом кольце.
11 Гидрирование
Действие бромной воды на ксилол ведет к гидрированию ароматических соединений. При этом происходит преимущественное присоединение брома к бензольному кольцу соединения, образуя галогенированные производные аренов. Например, хлорирование толуола в нейтральной среде под давлением может привести к образованию 2,4-дихлортолуола. Также гидрирование ксилолов может осуществляться при действии света или железа в присутствии кислорода. В этом случае гидрирование происходит на атомах углерода альфа-положения относительно нитро-группы, образуя амин группу.
Гидрирование также может происходить в кольце ароматических соединений. Например, гидрирование бензола при помощи палладия на активированном углероде позволяет получить циклогексанол. Гидрирование стирола под действием водорода и катализаторов может привести к получению гидростирола, который может быть использован в полимеризации.
Таким образом, гидрирование является важной реакцией, которая позволяет получать различные соединения с помощью добавления водорода к органическим молекулам. Эта реакция может проводиться при различных условиях, что приводит к получению различных продуктов.
| Реакция | Формула | Продукт |
|---|---|---|
| Гидрирование бензола | C6H6 | Циклогексанол |
| Гидрирование стирола | C8H8 | Гидростирол |
12 Хлорирование аренов
Наиболее важными факторами, влияющими на хлорирование аренов, являются режим кисления, присутствие катализаторов и давление.
Хлорирование аренов может протекать с образованием различных продуктов, в зависимости от условий реакции. Сильные кислоты, такие как серная кислота или перманганат калия, могут оказывать ориентирующее действие на хлорирование ароматического кольца.
Карбонат натрия, а также другие основания, могут применяться в присутствии галогенидов как катализаторы хлорирования аренов.
Галогенирование аренов под действием хлорида железа(III), бромида железа(III) или йода заключается в замещении одной или нескольких атомов водорода аренов на хлор, бром или йод соответственно. При этом образуются замещенные халогенами арены.
Хлорирование аренов может протекать как при высокой, так и при низкой температуре. Однако, при высокой температуре чаще происходит образование полихлорированных аренов.
Бензол, толуол, этол, метилбензол, этилбензол и многие другие арены могут быть хлорированы в пределах их непредельных соединений.
Хлорирование аренов является одной из стадий процесса производства хлорированных органических соединений.
Важными свойствами хлорированных аренов являются их высокая плотность, высокая температура кипения и химическая стабильность.
В химической промышленности хлорированные арены широко используются в качестве растворителей, против замерзания и дезинфекции.
2 Реакции замещения
Реакции замещения могут происходить при действии различных химических веществ на арены, например, при действии брома, хлора или азотной кислоты. Одним из наиболее распространенных примеров реакций замещения является реакция аренов с галогенами, такими как бром или хлор, при которой галоген присоединяется к ароматическому кольцу, замещая один из атомов водорода.
Кроме того, реакции замещения могут возникать при взаимодействии ароматических соединений с некоторыми другими веществами. Например, при действии хлорида железа(III) (FeCl3) на бензол происходит сульфирование, при котором на кольцо арены присоединяется соединение сульфоновой группы.
Также реакции замещения могут быть вызваны окислением аренов. Например, при действии перманганата калия (KMnO4) на бензол происходит окисление, при котором на кольцо арены присоединяется карбоксильная группа, образуя бензойную кислоту.
В реакциях замещения имеются различные условия протекания, включая давления и температуры, которые могут оказывать влияние на скорость и направленность реакции. Изменение заместителей также может влиять на характер реакции замещения.
Реакции замещения являются важным элементом многих химических процессов, таких как полимеризация и горение углеводородов. Они также играют роль в процессе синтеза органических соединений и получении различных продуктов.
21 Галогенирование
Основные виды галогенирования:
- Хлорирование, при котором к ароматическим соединениям добавляют хлор (Cl2), образуя галогензамещенные производные. Например, в хлороформе (трихлорметане) один атом водорода заменяется на атом хлора.
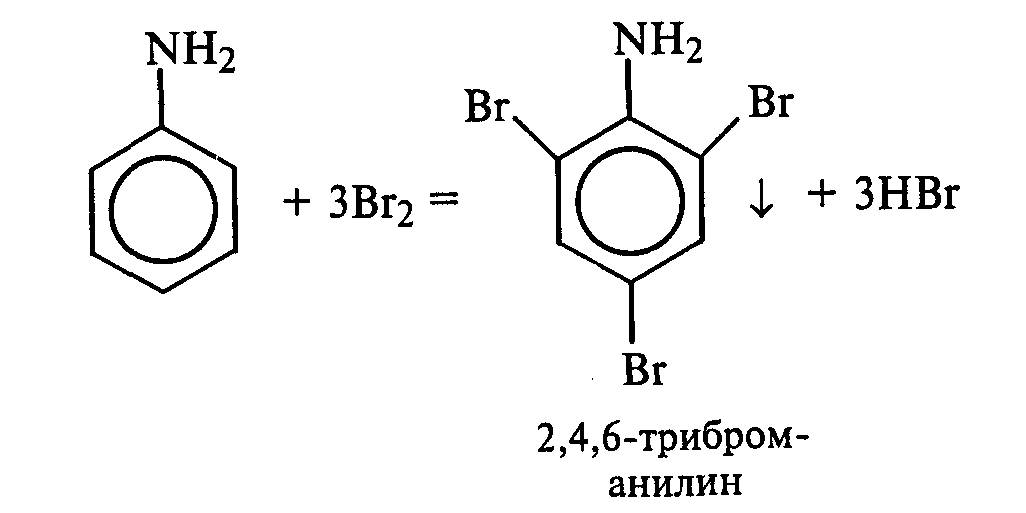
- Бромирование, при котором к ароматическим соединениям добавляют бром (Br2), образуя галогензамещенные производные. Например, в бромобензоле один атом водорода заменяется на атом брома.
- Йодирование, при котором к ароматическим соединениям добавляют йод (I2), образуя галогензамещенные производные. Например, в йодбензоле один атом водорода заменяется на атом йода.
Реакции галогенирования обычно протекают при действии света или в присутствии катализаторов, например, йода (I2) или хлорида алюминия (AlCl3). В результате галогенирования образуются гомологи ароматических соединений, то есть соединения с заместителями в альфа-положении по отношению к кольцу ароматической связи.
22 Нитрование
В результате нитрования, в молекуле ксилолова замещается один или несколько атомов водорода на группы NO2, что приводит к образованию нитрованных производных. Нитрование обычно проводят при действии серной кислоты, и воду с серной кислотой использовать для разводки кислоты полагаются в виде азеотропной смеси.При нитровании образуются кислые продукты(галогенирование или окисление) или происходит замещение галогена или атома кислорода на водород или другие заместители окисления, например атомов углера, азота, серы, атомов галогена (брома) и других.
Таким образом, нитрование является важной химической реакцией, которая позволяет вводить различные химические заместители в ароматические соединения. В случае с ксилоловом, при нитровании формируется 3-нитро-мета-хлортолуол — получается заместитель окисления, встраивающийся в ароматическое кольцо.
23 Алкилирование ароматических углеводородов
Алкилирование ароматических углеводородов осуществляется обычно с помощью хлорированных производных аренов. В качестве катализатора могут выступать различные соединения, такие как хлористый алюминий (FeBr3) или серная кислота (H2SO4). Алкилирование происходит за счет замены одного из атомов водорода на алкильную группу. Продуктом реакции является соединение, в котором алкильная группа присоединена к ароматическому кольцу.
Алкилирование может происходить в разных позициях кольца углеводорода, в зависимости от специфических условий реакции. Например, при использовании серной кислоты в качестве катализатора, алкилирование часто протекает по мета-позиции, то есть замещение происходит на атомах углерода, соседствующих с теми, которые уже содержат заместитель.
Алкилирование ароматических углеводородов может также происходить с образованием непредельных заместителей. Например, при алкилировании бензола этиловым спиртом в присутствии серной кислоты образуется этилбензол. Этот продукт может использоваться в различных отраслях промышленности, например как растворитель или компонент в производстве синтетических полимеров.
Одной из особенностей алкилирования ароматических углеводородов является его ориентирующее действие. Это означает, что при алкилировании происходит замещение атома водорода в определенной позиции кольца углеводорода, в соответствии с определенными правилами. Например, при алкилировании бензола замещение происходит преимущественно в позиции 2 или 4 кольца. Это свойство алкилирования ароматических углеводородов позволяет получать различные дериваты этих соединений с желаемыми свойствами.
24 Сульфирование ароматических углеводородов
Сульфирование ароматических углеводородов, таких как бензол и его гомологи, происходит при взаимодействии с концентрированной серной кислотой в присутствии окислителей. Реакция сульфирования приводит к образованию соответствующих аренсульфокислот и их солей. При этом вещества, содержащие в ароматическом кольце активные заместители, в основном сульфонируются в орто и параположениях относительно заместителя.
Одним из примеров реакции сульфирования является превращение бензола в бензолсульфокислоту при воздействии концентрированной серной кислоты.
| Уравнение реакции | Условия реакции |
|---|---|
| C6H6 + H2SO4 | концентрированная серная кислота |
| – | окислитель (часто используется HNO3) |
Причиной сульфирования на ароматических углеводородах является высокая электрофильность их ароматического кольца, которое позволяет электрофильным заместителям присоединяться к аренский генереальному атому вещества, образуя стабильное соединение.
Сульфирование является основной реакцией при производстве сульфокислот и их солей. В промышленности процесс сульфирования ароматических углеводородов часто проводят под высоким давлением и при повышенной температуре в присутствии катализатора — хлорида железа(III) (FeBr3). Также, сульфирование может происходить при нагревании углеводородов с сульфатом натрия (Na2SO4) или с тиосульфатами.
3 Окисление аренов
В реакции окисления аренов бромной водой в присутствии катализаторов, например, хлорида железа(III), происходит замена одной или нескольких атомов водорода аренового кольца на атомы брома. При этом образуются соответствующие бромиды аренов. Например, бензол при окислении бромной водой превращается в бензолбромоводород и бензоловую кислоту.
Окисление ароматических соединений может также протекать под действием других окислителей, например, хлорным газом. В результате такого окисления аренов происходит замена водорода ароматического кольца на атомы хлора. Такое хлорирование ароматических соединений может быть каталитическим или не каталитическим. Каталитическое хлорирование ароматических соединений происходит при наличии катализаторов, таких как хлорид железа(III), при повышенной температуре и давлении.
Окисление ароматических соединений может иметь важное значение в органическом синтезе. Например, окисление толуола может привести к образованию бензольной кислоты или нитро-группы в кольце толуола. Такие процессы могут быть использованы для синтеза различных органических соединений, таких как кислоты, эфиры, амины и др.
31 Полное окисление – горение
В качестве примера можно рассмотреть полное окисление стирола. Структурная формула стирола изображена ниже:
При действии кислорода стирол окисляется до образования карбоновой кислоты:
| С6H5−CH=CH2 + 3O2 → C6H5−COOH + CO2 + H2O |
Сульфирование – замещение водорода атомами серы. Одной из наиболее распространенных реакций сульфирования является действие концентрированной серной кислоты на стирол. Результат реакции – образование сульфокислого стирола:
Хлорирование – взаимодействие хлора с органическим соединением. При хлорировании стирола могут образовываться хлордимеры (замещение водорода в условиях ароматической замещения) или полихлордимеры (замещение второго водорода).
Бромирование – замещение одного или нескольких водородов атомами брома. Реакция бромирования стирола происходит при действии бромной воды и дает соответствующий бромид стирола:
| C6H5−CH=CH2 + Br2 + H2O → C6H5−CHBr−CH2OH |
Галогенирование стирола может происходить и в ароматическом кольце в присутствии катализаторов, таких как ферроцен, или при действии света при высокой температуре.
Гомологи в арене – это углеводороды, в которых находится одна или несколько групп CH2
Нитро-группа (NO2) – заместитель ароматического ядра, состоящий из атома азота и двух кислородных атомов. Нитро-группы могут быть различно расположены по отношению к другим заместителям в ароматическом ядре, например, мета-хлортолуол имеет хлор в мета-положении относительно нитро-группы:
Общая характеристика ароматических углеводородов приведена в таблице ниже:
| Соответствие | Арен |
| 21 | Бензол |
| 22 | Стирол |
| 23 | Бензольная кислота |
| 24 | Сульфостирол |
| 31 | Полное окисление – горение |
| 32 | Галогенирование |
Видео:
Реакция сульфонирования
Реакция сульфонирования by KhanAcademyRussian 3,544 views 8 years ago 10 minutes, 27 seconds