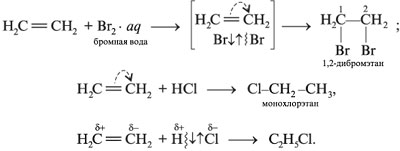
Процесс бутадиена с бромной водой: механизм реакции и итоговые продукты
Реакция между бутадиеном и бромной водой является одной из важнейших реакций в органической химии. Эта реакция демонстрирует свойства присоединения брома к двойным связям в алкадиенах и приводит к образованию новых соединений.
Реакция присоединения бутадиена к бромной воде является одной из стадий процесса получения каучуков. Бутадиен присоединяется к двум атомам брома, окисления воды происходит в мягких условиях, благодаря свойствам кислоты. При этом происходит разрыв двойной связи в алкадиене, и образуется соединение, называемое дивинилбензолом.
В химические связи бутадиена вступают 23 атома водорода и 13 атомов углерода. Эта реакция является одной из самых характерных для присоединения галогенов к алкадиенам. Гидрогалогенирование алкадиенов может происходить с образованием нециклических соединений, как в случае с реакцией бутадиена с бромной водой.
Ответ на вопрос о том, какие продукты образуются в реакции присоединения бутадиена к бромной воде, зависит от условий проведения реакции. Вода может быть превращена в углекислый газ, а атомы водорода входят в композицию новых молекул. Образование полимера и горение представляют собой дополнительные возможные пути реакций.
Химические свойства алкадиенов
Один из важных химических процессов, которые могут происходить с алкадиенами, — это реакция присоединения. При этой реакции новые атомы или группы атомов присоединяются к двойным связям алкадиенов. Например, алкадиен может присоединяться к бромной воде, при этом образуется бромгидрид алкадиена. Реакция протекает уравнениях:
1) CH2=CH-CH=CH2 + Br2 + H2O → CH2Br-CHBr-CH=CH2
2) CH2=CH-CH=CH2 + HBr + H2O → CH2Br-CH2-CH=CH2
Эти реакции подчиняются правилу предпочтительного присоединения электрофилов и нуклеофилов к атомам водорода и галогенов к более замещенным атомам углерода.
Еще одно важное химическое свойство алкадиенов — это их способность подвергаться окислению. Двойные связи алкадиенов присоединяются к атомам кислорода при окислении, образуя соответствующие оксиды. Например, бутен-2 может окисляться до малеиновой кислоты:
CH2=CH-CH=CH2 + [O] → HOOC-C(CO)H2-CH=CH2
Алкадиены также могут подвергаться гидрированию, при котором двойные связи превращаются в одинарные. Например, бутен-2 может гидрироваться до бутана-2:
CH2=CH-CH=CH2 + H2 → CH3-CH=CH-CH3
Еще одной важной химической реакцией алкадиенов является их способность к полимеризации. При полимеризации алкадиенов двойные связи в молекулах мономера разрываются и образуется полимер с длинной цепью. Например, дивинил может полимеризоваться, образуя поливинилпиролидон:
CH2=CH-CH=CH2 + CH2=CH-CO-NH-CH2-CH=CH2 → (-CH2-CH=CH-)n
Это свойство алкадиенов позволяет их использовать как мономеры при производстве полимерных материалов.
Химические свойства сопряженных алкадиенов
Одной из основных характеристик сопряженных алкадиенов является возможность происходить их присоединение к молекулам других веществ. При этом происходит разрыв двойной связи и образование новых химических связей.
Сопряженные алкадиены могут присоединяться к различным молекулам, таким как вода, бромная вода, галогены и другие.
Например, при реакции бутадиена с бромной водой идет присоединение брома и гидроксильной группы к двойным связям бутадиена.
Важно отметить, что присоединение к двойным связям сопряженных алкадиенов может быть как жестким, так и мягким.
Жесткое присоединение характеризуется образованием эндоадуктов, то есть новых соединений, в которых вновь образованные атомы или группы атомов присоединяются к молекуле сопряженного алкадиена с сохранением положения запрещенных орто и пара положений.
Это связано с факторами стерической и электронной природы.
Мягкое присоединение характеризуется образованием экзоадуктов, то есть новых соединений, в которых атомы или группы атомов присоединяются к молекуле сопряженного алкадиена без сохранения положения запрещенных орто и пара положений.
Важной реакцией сопряженных алкадиенов является их полимеризация. При этом нециклические алкадиены присоединяются друг к другу, образуя полимер, который может использоваться, например, для производства каучуков.
Также сопряженные алкадиены подвержены реакциям гидрирования и окисления. Гидрирование представляет собой присоединение водорода к двойным связям сопряженных алкадиенов. Окисление, в свою очередь, включает присоединение атомов кислорода или других окислителей к атомам сопряженных алкадиенов.
В общем случае, химические свойства сопряженных алкадиенов определяются их строением и наличием сопряженных двойных связей.
Их реакционная способность позволяет получать разнообразные гетероциклические соединения и другие полезные продукты в органической химии.
1 Реакции присоединения
Присоединение бутилена и двух молекул бромной воды – одна из типичных реакций присоединения. В результате этой реакции образуются два решения – 2,3-дибромбутиловый спирт и 2,3-дигидроксибутиловый спирт.
В случае присоединения дивинила к бромной воде, образуются два раствора – 1,2-дибром-1,2-дигидроэтилениловый спирт и 1,2-дигидрокси-1,2-дибромэтилэтиленовый спирт.
Реакции присоединения мономера к молекуле воды могут протекать при различных условиях и приводить к образованию различных продуктов. Например, при гидрогалогенировании алкадиенов – насыщенных нециклических углеводородов с двумя или более двойными связями – образуются соответствующие галогенетированные производные.
Окисление бутадиена приводит к образованию глиоксаловой кислоты, в которой на каждую двойную связь углеродного скелета присоединяется по одному атому кислорода. Данное окисление является одной из основных реакций присоединения в органической химии.
Одной из важных реакций присоединения является присоединение кислорода и водорода на место двойных связей алкадиену. Например, при присоединении галогенов и воды к бутилену возникает реакция присоединения галогенов в «химикпро» решение и Образование 1,2-дибромбутана.
Гидрогалогенирование двойной связи бутадиена происходит по тому же механизму, что и гидрогалогенирование бутена, но в это жесткое решение присоединяются две молекулы воды, что приводит к образованию двух разных решений – 2,3-дигидроксибутиловый спирт и 2,3-дигидроксибутановый спирт.
11 Гидрирование
Гидрирование алкадиену может протекать путём окисления, когда двойные связи между атомами присоединяются к двум атомам водорода. При гидрировании алкадиенов образуются окисленные продукты — алдегиды или кетоны.
Особенность гидрирования алкадиенов в бромной воде состоит в том, что при полном гидрировании образуются бесплатно решения с очень высокими числами протекания и селективности.
Реакция гидрирования имеет мягкое химическое присоединение атомов водорода в молекулах алкадиенов. При полном гидрировании водород присоединяется к каждой из двойных связей.
Галогенирование алкадиенов обычно происходит между атомом или атомами галогенов (например, брома) и алкадиеном. Галогенирование алкадиенов может привести к образованию полимеров, таких как каучук.
Нециклические алкадиены могут присоединяться к месту двойной связи в бромной воде. Это присоединение происходит путем разрыва связей и образования параллельных атомов карбона и брома.
Присоединение атома брома в бромной воде к алкадиену осуществляется путем окисления молекулы алкадиена. После присоединения бромная вода окисляется и разрывает связь, образуя атомы карбона и брома.
Гидрирование алкенов, в отличие от алкадиенов, можно решить с помощью кислоты. На этой стадии реакции атомы водорода присоединяются к молекулярным цепям алкена.
При гидрировании алкадиенов и алкенов происходит окисление двойной связи, а при гидрировании алкадиенов — окисление двух связей между мономерами. Реакционное окисление происходит через присоединение атома гидрогена к двум атомам углерода.
12 Галогенирование алкадиенов
Галогенирование происходит в две стадии. Сначала происходит гидрогалогенирование, при котором атомы галогена присоединяются к двойной связи алкадиена, образуя промежуточные халогениды. Затем, при окислении этих халогенидов, происходит разрыв двойной связи и образование галогензамещенных продуктов.
Нециклические алкадиены обычно галогенируются в условиях, подходящих для галогенирования алкенов. При этом, образуется только один галогенированный продукт, так как галоген присоединяется к тому атому углерода, который обладает наименьшим количеством связей с водородом.
Галогенирование алкадиенов имеет широкие применения в органической химии. Например, галогенирование бутадиена позволяет получать бромзамещенные продукты, которые можно использовать для полимеризации и получения полимеров с различными свойствами.
Видео:
Каучуки: бутадиеновый, изопреновый, хлоропреновый. ЕГЭ по химии
Каучуки: бутадиеновый, изопреновый, хлоропреновый. ЕГЭ по химии by Степенин и Дацук / Химия ЕГЭ и 10 класс 25,889 views 6 years ago 6 minutes, 13 seconds