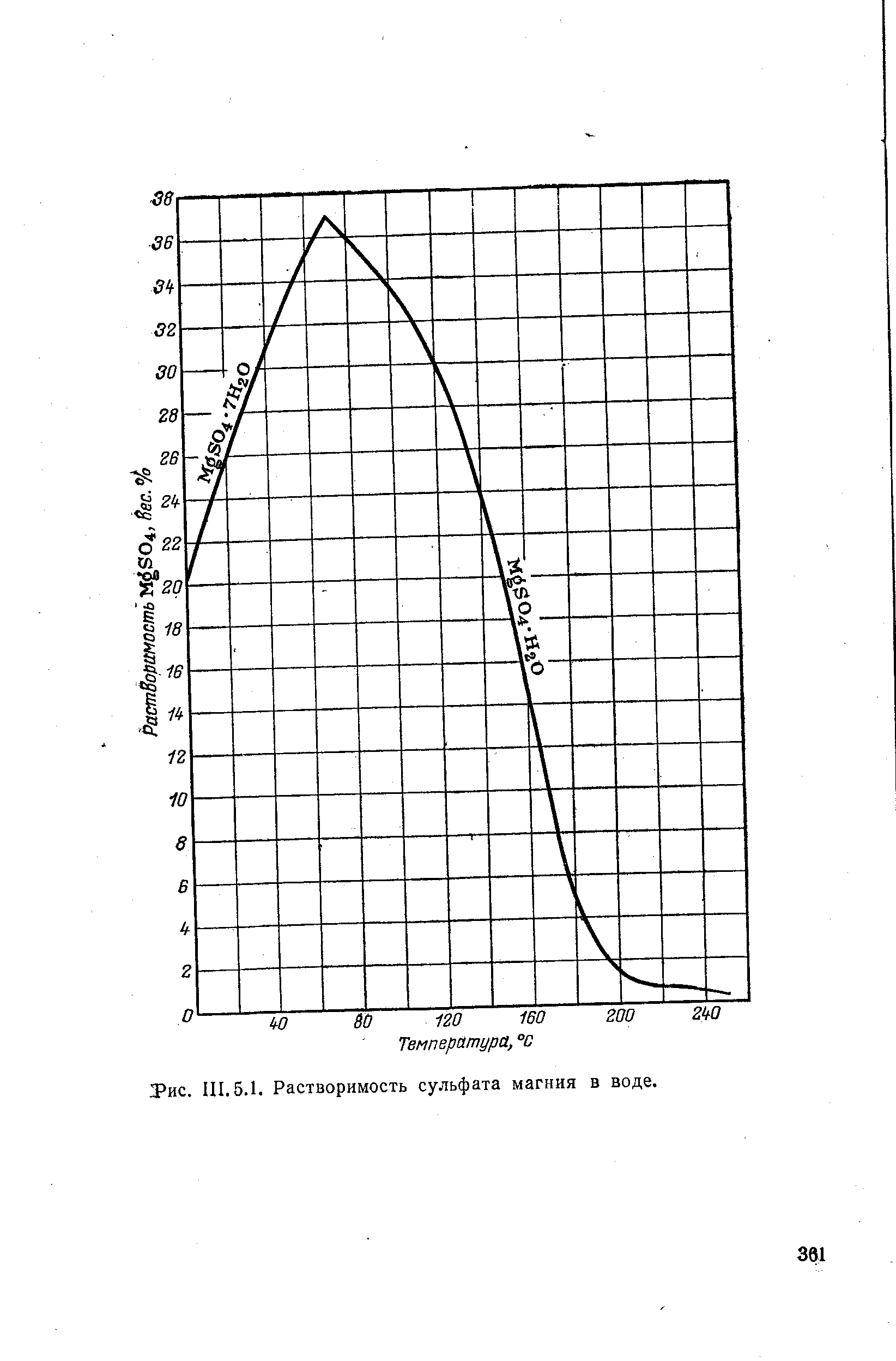
- Влияние растворимости сульфата магния в воде и его особенности.
- Сульфат магния: способы получения и химические свойства
- Получение сульфата магния
- Химические свойства сульфата магния
- Способ получения
- Получение сульфата магния из солей
- Получение сульфата магния по другим способам
- Растворимость сульфата магния в воде
- Качественная реакция
- Получение сульфата магния
- Свойства сульфата магния
- Химические свойства
- Видео:
- СУЛЬФАТ МАГНИЯ. ПОЛЕЗНОЕ УДОБРЕНИЕ для сада и огорода.
Влияние растворимости сульфата магния в воде и его особенности.
Сульфат магния, также известный под названием сернокислого магния (MgSO4), является одной из наиболее распространенных солей, которая образуется в результате химической реакции между серной кислотой и магнием. Эта соль широко используется в промышленности, а также в качестве средства для получения различных металлов.
Сульфат магния образует растворы, которые обладают высокой растворимостью в воде. При комнатной температуре масса сульфата магния, растворимого в 100 г воды, составляет около 26 г. Эта растворимость увеличивается при нагревании, так как происходит образование кристаллогидратов — безводных и гидратированных форм сульфата магния, которые вступают в химические реакции с водой.
Сульфат магния в виде порошка представляет собой бесцветные кристаллы. Это вещество обладает звуковыми и лекарственными свойствами, поскольку служит основным компонентом многих лекарственных препаратов, таких как слабительное. Соли магния также используются в сельском хозяйстве и садоводстве в качестве удобрений для растений.
Реакция сульфата магния с водой происходит следующим образом: магний реагирует с водой, образуя гидратированный магний хлорид. В ходе этой реакции выделяется тепло, и в результате получается раствор сульфата магния.
Кристаллы сульфата магния можно получить путем испарения водных растворов или охлаждения нагретых растворов. При этом обычно образуются прозрачные бесцветные кристаллы, которые кристаллизуются в виде кустарников.
Сульфат магния обладает различными физическими и химическими свойствами, и его растворимость в воде играет важную роль при применении данного вещества в различных отраслях промышленности и медицине.
Сульфат магния: способы получения и химические свойства
Получение сульфата магния
Сульфат магния можно получить различными способами. Одним из них является реакция между серной кислотой (H2SO4) и магнием (Mg). В результате этой реакции образуется MgSO4 и выделяется водород (H2). Получение сульфата магния также возможно при реакции между гидроксидом магния (Mg(OH)2) и сернокислым натрием (Na2SO4).
Химические свойства сульфата магния
Сульфат магния обладает рядом химических свойств. Во-первых, он хорошо растворим в воде, образуя водные растворы с различными содержаниями соли. Температура растворения сульфата магния зависит от плотности раствора и может быть изменена. В комнатной температуре сульфат магния вступает в реакцию с другими металлами, образуя соответствующие соли.
Во-вторых, сульфат магния образует кристаллогидраты, водные растворы которых проявляют свойства слабительного. Происходит это из-за взаимодействия сульфата магния с водой в организме, что вызывает усиленную перистальтику кишечника и улучшает процесс пищеварения.
Физические свойства сульфата магния также стоит отметить. В чистом виде соль представляет собой бесцветные кристаллы, имеющие пластинчатую структуру. Процесс нагревания безводного сульфата магния сопровождается выделением звуковых эффектов и происходит при температуре около 1124°C. Качественная характеристика сульфата магния — это его способность спонтанно поддерживать горение в воздухе при взаимодействии с окислителями, такими как сернистый ангидрид (SO2) или хлорид (Cl).
Способ получения
Получение сульфата магния из солей
Сульфат магния можно получить из различных солей магния, таких как хлорид магния (MgCl2) или порошок магния (Mg). Для этого проводится реакция между солью магния и сульфатом натрия (Na2SO4), в результате которой образуется сульфат магния и хлорид натрия (NaCl). Реакцию можно представить следующей формулой:
MgCl2 + Na2SO4 → MgSO4 + 2NaCl
В данном случае, сульфат магния выступает в качестве продукта реакции в виде бесцветных кристаллов.
Получение сульфата магния по другим способам
Кроме реакции между солями магния и сульфатом натрия, существуют и другие способы получения сульфата магния. Например, его можно получить путем химической реакции между металлическим магнием и газообразным сернистым ангидридом (SO2). Данная реакция происходит при повышенных температурах и даёт сульфат магния в виде порошка.
Сульфат магния также можно получить путем реакции между солями других металлов (например, бария) и сульфатом магния. В этом случае образуются растворимые кристаллы сульфата магния.
Растворимость сульфата магния в воде
Сульфат магния обладает высокой растворимостью в воде. При комнатной температуре его массовая доля в водных растворах может достигать до 26%. Однако, при нагревании растворимость сульфата магния увеличивается.
Сульфат магния также обладает свойствами слабительного.
Качественная реакция
Сульфат магния является бесцветным кристаллогидратом, содержащим несколько молекул воды в своей структуре. Наиболее распространенные кристаллогидраты сульфата магния — гексагидрат (MgSO4 · 6H2O) и гидрат (MgSO4 · H2O). Безводный сульфат магния также известен как эпсомит.
Сульфат магния хорошо растворим в воде. Содержание магния в растворе может быть определено с помощью качественной реакции с барием. При взаимодействии сульфата магния с хлоридом бария (BaCl2) в водном растворе образуется осадок барийсульфата (BaSO4), который имеет характерные бесцветные кристаллы с высокой плотностью.
Качественная реакция позволяет определить наличие сульфата магния (MgSO4) в растворе. При вступлении сульфата магния с солью бария происходит реакция, в результате которой образуется барийсульфат (BaSO4). Реакция происходит при комнатной температуре в виде небольшого осадка в виде белого порошка или хлопьев.
Получение сульфата магния
Сульфат магния может быть получен различными способами. Один из способов — взаимодействие металлического магния с серной кислотой (H2SO4). Реакция происходит при нагревании и сопровождается образованием сернистого газа (SO2) и образованием сульфата магния.
Свойства сульфата магния
Сульфат магния обладает рядом физических и химических свойств. Он обладает белым или бесцветным цветом в виде кристаллов или порошка. Сульфат магния имеет высокую растворимость в воде — около 25 г на 100 мл воды при комнатной температуре. При нагревании сульфат магния теряет свои молекулы воды и кристаллизуется в форме безводного порошка.
В промышленности сульфат магния широко применяется в качестве удобрения для растений. Он обеспечивает доступ магния для растений и способствует их росту и развитию. Кроме того, сульфат магния используется в производстве бумаги, промышленности красителей, лекарственных препаратов и других химических продуктов.
| Название реакции | Уравнение реакции |
|---|---|
| Взаимодействие сульфата магния с хлоридом бария | MgSO4 (aq) + BaCl2(aq) → BaSO4(s) + MgCl2(aq) |
Химические свойства
Сульфат магния, также известный под названием сернокислый магний (MgSO4), обладает различными химическими свойствами. Эта соль, как и многие другие соли магния, хорошо растворяется в воде.
При взаимодействии магния и серной кислоты образуется соль магния, а именно сернокислый магний: Mg + H2SO4 → MgSO4 + H2.
Сернокислый магний может применяться в промышленности как соль магния. Он также используется в медицине, как слабительное средство.
Сульфат магния в природе встречается в виде кристаллов или порошка. Кристаллы сульфата магния обычно бесцветны и имеют высокую плотность. Безводный вид сульфата магния при нагревании кристаллов образуется при температуре выше 250 градусов Цельсия. Температура, при которой кристаллы сульфата магния начинают кристаллизоваться из раствора, называется температурой кристаллизации.
Растворимость сульфата магния в воде зависит от температуры. При комнатной температуре сульфат магния растворим в воде в нескольких кристаллогидратах. При нагревании раствора содержание сульфата магния в растворе увеличивается, а при охлаждении происходит кристаллизация.
Сульфат магния также реагирует с некоторыми металлами, образуя соли магния и выделяя водород. Например, реакция магния и сернокислого натрия (Na2SO4) выглядит следующим образом: MgSO4 + 2Na → Mg + Na2SO4.
Водные растворы сульфата магния имеют качественную химическую реакцию — они реагируют со способностью к образованию ионов магния и сульфата в растворе.
Физические свойства сульфата магния включают образование кристаллов, его белый цвет в безводном виде, а также его способность к кристаллизации и кристаллогидратам. Этот минерал обычно используется в химической лаборатории в виде порошка или кристаллизованных солей магния.
Видео:
СУЛЬФАТ МАГНИЯ. ПОЛЕЗНОЕ УДОБРЕНИЕ для сада и огорода.
СУЛЬФАТ МАГНИЯ. ПОЛЕЗНОЕ УДОБРЕНИЕ для сада и огорода. by GALA. S 41,435 views 2 years ago 6 minutes, 4 seconds