Методы и примеры разведения серной кислоты водой: таблица и объяснение
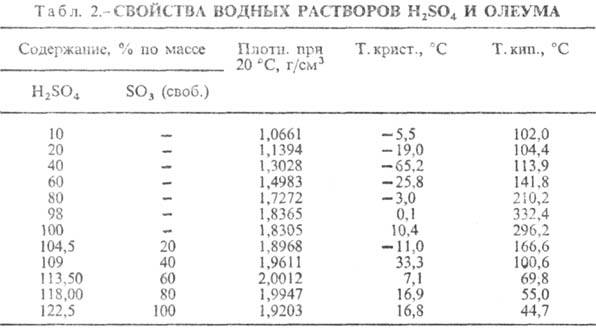
Серная кислота (H2SO4) является одной из наиболее распространенных и важных кислот в химической промышленности. Исходные концентрации серной кислоты могут быть слишком высокими для ряда приложений, поэтому они разбавляются водой до желаемой концентрации.
Смешивание серной кислоты с водой производится в специальных емкостях, таких как эмалированные емкости или стеклотарах. Точные количества кислоты и воды определяются в зависимости от требуемой концентрации разбавленной кислоты. Правило состоит в том, чтобы всегда добавлять кислоту к воде, а не наоборот, поскольку обратное смешивание может вызвать брызги и опасность для здоровья.
Серная кислота в реакции с водой выделяет большое количество тепла и образует пары сернистого ангидрида (SO2) и кислорода (O2). При смешивании кислоты с водой, внимательность и осторожность особенно важны.
Растворы кислот
Для разбавления концентрированной серной кислоты часто используют воду. Разбавление серной кислоты водой должно производиться с осторожностью и следуя определенной последовательности. Приливая воду к концентрированной серной кислоте, следует помнить, что реакция между этими веществами сопровождается выделением большого количества тепла и газа.
При смешивании воды с серной кислотой образуется раствор серной кислоты, а также образуется еще одна кислота – сернистая кислота (H2SO3). Растворение серной кислоты в воде – это реакция сильной кислоты со слабой.
Разбавление серной кислоты водой можно проводить несколькими способами в зависимости от условий. При разбавлении водой наиболее эффективно следует избегать взаимодействия воды с большим количеством кислоты. При разбавлении водой большого количества серной кислоты реакция с водой происходит очень быстро, с выделением большого количества тепла. При столкновении капель серной кислоты с водой возникает кратковременное выделение попутно возникающего пара. Однако, если образование пара будет носить непрерывный характер, возникнет образование аэрозоля.
Для разбавления концентрированной серной кислоты водой используются небольшие количества воды, поэтому разбавление проводят постепенно, добавляя небольшое множество воды к концентрированной серной кислоте. При этом нужно помнить, что при разбавлении концентрированной серной кислоты водой образуется сернистая кислота.
Еще одной сильной кислотой, используемой в лабораториях, является азотная кислота (HNO3). Раствор азотной кислоты очень активен и может реагировать с различными веществами, такими как вода или углекислый газ. Поэтому при работе с раствором азотной кислоты необходимо соблюдать предосторожности.
Азотная кислота растворяется в воде, выделяя красные дымы, состоящие из оксида азота (NO2). Эти дымы можно увидеть, если подвести к ним лист бумаги. Реакция между азотной кислотой и водой является эндотермической реакцией, то есть сопровождается поглощением тепла.
Для получения раствора азотной кислоты обычно сначала готовят раствор серной кислоты. Затем в этот раствор с помощью хлористого натрия добавляют немного азотной кислоты. Реакция между серной кислотой и хлористым натрием приводит к образованию хлористого водорода. Полученная смесь реагентов подается на кислотный крест, при этом между серной кислотой и хлористым натрием происходит связывание серного газа с водородом и образуется азотная кислота.
Работать с растворами кислот следует с особыми мерами предосторожности. Если при использовании кислоты нарушены правила безопасности, то возможно образование сернистой кислоты или дымка нарушит систему дыхания. Поэтому при работе с кислотой следует использовать эмалированный стеклянный сосуд или чугунный резервуар.
Серная кислота
Свойства и использование
Серная кислота (H2SO4) – это одна из наиболее концентрированных кислот, которая имеет безцветное жидкое состояние. Концентрированная серная кислота является сильным окислителем и реагирует с многими веществами. Благодаря своей химической активности и высокой реакционной способности, эта кислота находит широкое применение в различных областях.
В промышленности серная кислота используется для производства удобрений, пластмасс, растворителей, красителей и других химических соединений. Она также часто используется в процессе очистки металлов и различных изделий.
В лабораториях серная кислота используется для определения концентрации веществ, растворов и разбавления растворов для расчетов. Исходя из содержания данной кислоты исходных растворов, определяется концентрация, процентное содержание химических веществ в растворе.
Опасности и предосторожности
Концентрированная серная кислота является очень опасным веществом и требует соблюдения особых мер предосторожности при работе с ней. При взаимодействии кислоты с водой или органическими веществами может происходить выделение тепла и газообразных продуктов. Хлористый и сернистый газы могут быть образованы при смешивании серной кислоты с хлористыми и сернистыми кислотами. Отравление паром серной кислоты может привести к ожогам кожи, слизистых оболочек и дыхательных путей.
Также следует быть предельно осторожными при разбавлении серной кислоты водой. Смешивание кислоты с водой всегда происходит через добавление кислоты в воду, а не наоборот, чтобы избежать попадания кислоты в руки. Приливая малыми порциями концентрированную кислоту к большому количеству воды под контролируемым режимом, можно точно и безопасно разбавить кислоту до нужной концентрации и избежать возможных опасностей.
В лаборатории работа с серной кислотой проводится в эмалированном стекле или пластиковой посуде. При процедуре разбавления серной кислоты водой следует соблюдать следующие правила:
- Надевать защитный костюм, перчатки и специальные очки.
- Соблюдать предосторожности при хранении кислоты: хранить в закрытой и надежно упакованной емкости в отдельном месте.
- Проводить все манипуляции с кислотой в хорошо проветриваемом помещении или под вытяжным шкафом, чтобы избежать вдыхания паров.
- Не оставлять кислоту без присмотра, так как она может реагировать с другими веществами и привести к неожиданным последствиям.
| Условия | Концентрация серной кислоты, % | Количество кислоты, мл | Количество воды, мл |
|---|---|---|---|
| 1+9 | 10 | 10 | 90 |
| 1+4 | 20 | 20 | 80 |
Приведенная выше таблица демонстрирует пример разбавления концентрированной серной кислоты с использованием различных пропорций исходных веществ. Эти пропорции могут быть изменены в зависимости от требуемой концентрации и количества раствора, не забывая следовать правилам безопасности.
Разбавление и смешивание серной кислоты
Разбавление серной кислоты производится путем добавления воды к исходному раствору. Серная кислота подается в реакционную емкость, обычно эмалированный сосуд, а затем к ней постепенно добавляется вода. Данный процесс позволяет уменьшить концентрацию кислоты и получить раствор с требуемой концентрацией.
Разбавление серной кислоты производят в нескольких этапах, пользуясь правилом «от легкого к сложному». Вначале к серной кислоте добавляют небольшое количество воды, после чего смесь тщательно перемешивают до полного растворения кислоты. Затем процесс повторяют, добавляя воду постепенно, пока не достигнута требуемая концентрация раствора.
Серную кислоту также можно разбавлять с помощью сернистого газа (SO2). Для этого воздух, содержащий SO2, подается через газоочистный аппарат и смешивается с концентрированной серной кислотой. Разбавление серной кислоты с помощью сернистого газа позволяет получить раствор с более низкой концентрацией.
Смешивание серной кислоты с другими кислотами также является важной операцией. Например, при производстве олеума, серную кислоту смешивают с концентрированной азотной кислотой (HNO3), что приводит к образованию различных сложных реакционных смесей.
Следует отметить, что смешивание сконцентрированных кислот может приводить к реакции окисления, сопровождающейся выделением тепла и газов. Поэтому при смешивании особо активных кислот, таких как серная кислота и хлористый газ (HCl), следует быть особенно предельно осторожными.
Важно отметить, что при смешивании кислот следует строго соблюдать правило добавления кислоты к воде, а не наоборот. Если добавлять воду к кислоте, возникают опасные пузырьки, которые могут вызвать опасные выбросы и извержения кислоты.
При разбавлении и смешивании серной кислоты с другими кислотами необходимо учитывать их концентрации, проводить расчеты и следить за точностью измерений. Несоблюдение этих правил может привести к нежелательным химическим реакциям и неожиданным последствиям.
Видео:
Правило разбавления концентрированной серной кислоты водой
Правило разбавления концентрированной серной кислоты водой by MIK 1,703 views 2 years ago 20 seconds