Как происходит реакция угарного газа с водой?
Угарный газ (углерод оксид), обозначаемый формулой CO, является одним из основных продуктов сгорания угля и других углеродосодержащих веществ. Этот газ нередко используется в промышленности, где проявляет свои уникальные химические свойства.
Угарный газ реагирует с водой при нагревании или в условиях высокого давления, образуя углеродную кислоту. Такая реакция происходит по следующей схеме: CO + H2O → H2CO3. Углеродная кислота, в свою очередь, является слабым кислотным веществом.
Угарный газ также может реагировать с кислородом, образуя оксид углерода (CO2). Данная реакция часто используется для получения углекислого газа (двуокиси углерода) при газификации угля или других углеродсодержащих материалов. Тройная связь в молекуле угарного газа достаточно сильная, поэтому для окисления угарного газа до CO2 требуется применение высоких температур и переходных металлов в качестве катализатора.
Угарный газ, являясь ядовитым веществом, также проявляет восстановительные свойства. Он способен восстанавливать кислород из оксидов различных металлов, превращая их в соответствующие металлы. Например, угарный газ при нагревании с хлором дает продукты реакции COCl2, COCl2 и CO.
Вода, в свою очередь, может быть восстановителем в реакциях с угарным газом. В результате таких реакций вода может окисляться до молекулярного кислорода (O2) при наличии угарного газа и высоких температурах.
Оксид углерода II
Оксид углерода II образуется при неполном сгорании угля, древесины, нефти и других углеродсодержащих веществ. В промышленности он получается в результате газификации угля или восстановительного выплавления металлов.
Оксид углерода II обладает рядом химических свойств. Он является ядовитым газом, обладающим отравляющими свойствами. При взаимодействии с кислородом осуществляется реакция окисления, в результате которой образуется углекислый газ. Этот газ также проявляет кислотные свойства в реакции с неметаллами и щелочами.
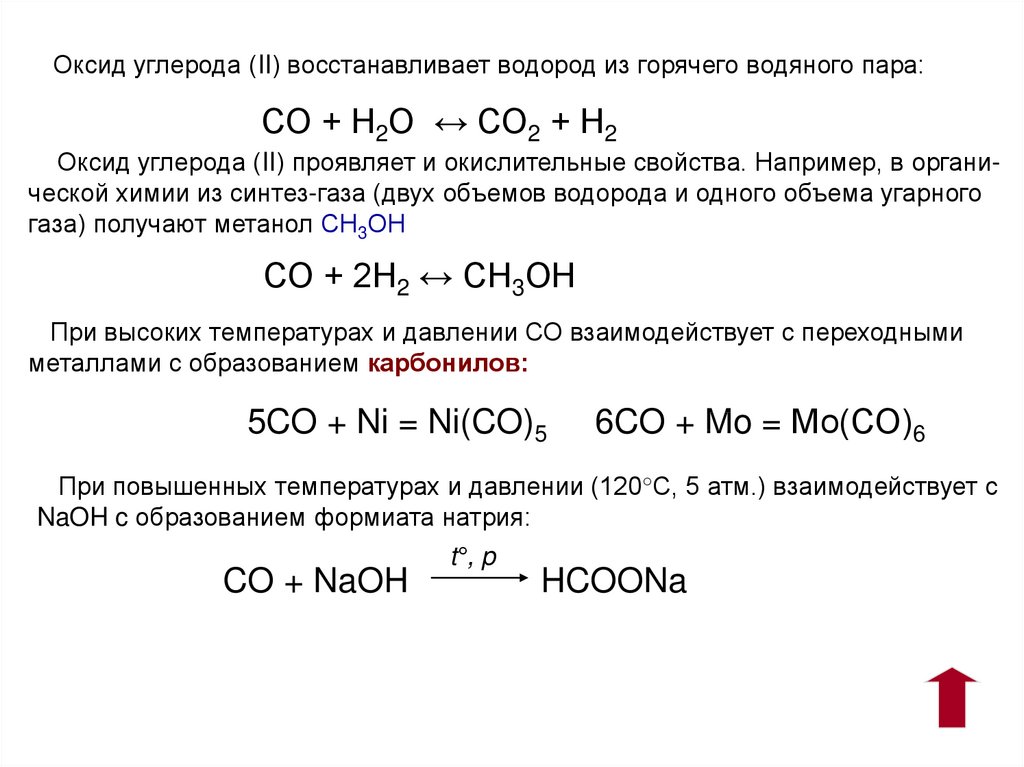
Угарный газ обладает способностью реагировать с водой и образовывать углекислый газ и водород. Реакция оксида углерода II с водой происходит при обычных условиях давления и температуры.
| Условия реакции | Реакционная формула |
|---|---|
| Оксид углерода II + Вода | Углекислый газ + Водород |
Оксид углерода II также может восстанавливать вещества, например, оксиды металлов или переходные металлы, при нагревании.
Общая реакция оксида углерода II с кислородом можно представить так:
Оксид углерода II + Кислород → Углекислый газ
Оксид углерода II также образуется при облучении угарного газа в присутствии кислорода. При этой реакции происходит окисление угарного газа до оксида углерода II:
Угарный газ + Кислород → Оксид углерода II
Получение оксида углерода II возможно также путем химической реакции во время газификации угля при высоких температурах и давлении. При этом происходит реакция окисления угля и образование углерода и угарного газа:
Уголь + Кислород → Оксид углерода II
Таким образом, оксид углерода II обладает разнообразными химическими свойствами, которые проявляются в различных реакциях с другими веществами. Его получение возможно разными способами, например, путем газификации угля или восстановления оксидов металлов. Оксид углерода II является ядовитым газом, который образуется при неполном сгорании углеродсодержащих веществ и используется в промышленности.
Оксид углерода II
Водорастворимый оксид углерода II образуется также при пропускании диоксида серы через воду:
CO2 + H2O → H2CO3
Оксид углерода II имеет молекулярную формулу CO2 и состоит из одной атомарной группы углерода, связанной с двумя атомами кислорода двойной связью. Эти связи являются тройной связями, что делает молекулу CO2 стабильной и инертной соединением.
CO2 является газообразным веществом при обычных температурах и давлениях, без цвета и запаха. Он растворяется в воде и образует угольную кислоту (H2CO3), которая хорошо проявляет свойства слабой кислоты. Пропускание угарного газа через растворы щелочей приводит к получению оксида углерода II:
CO2 + 2NaOH → Na2CO3 + H2O
Оксид углерода II может взаимодействовать с металлами при нагревании и образовывать соединения в виде оксида металла и углекислого газа. Также CO2 реагирует с кислотами, образуя соли через вытеснение двух атомов кислорода:
CO2 + 2HCl → COCl2 + H2O
Оксид углерода II также может быть получен при облучении раскаленного угля:
C + O2 → CO2
CO2 является одним из основных продуктов сгорания угля и других органических веществ в атмосфере.
Углерод
Углерод способен образовывать тройные химические связи, что делает его основным элементом в многочисленных органических соединениях. Уголь и графит — основные аллотропические формы углерода, которые можно получить при нагревании угля. Раскаленный уголь или хлор с оксидом углерода можно использовать для получения графита.
Угарный газ, или оксид углерода, образуется при неполном горении угля или при газификации угля в промышленности. Этот продукт можно использовать в химических реакциях, восстанавливающих соединения и окисляющих кислород в воде или кислых оксидах.
Угарный газ часто взаимодействует с кислотами, образуя их соли и проявляя свойства восстановительного агента. Например, при пропускании угарного газа через серную кислоту можно получить угарный газ плюс серную кислоту. Также, при реакции угарного газа с кислородом можно получить диоксид углерода, который является кислотным оксидом.
Углерод также проявляет свои химические свойства при взаимодействии с металлами. Например, при нагревании угля с добавлением металлов можно получить множество соединений, таких как карбиды металлов.
Взаимодействие углерода с водой и кислотами происходит при определенных условиях — например, при высоких температурах или пропускании газа через реакционную среду. Углерод может участвовать в различных химических реакциях и влиять на их ход и результат.
Угарный газ плюс вода реакция
Добавление угарного газа к воде приводит к образованию кислотного оксида. Подобная реакция происходит при низких температурах и характеризуется окислением угарного газа кислородом из воды. В результате образуется кислотный оксид, который в свою очередь может образовывать различные соединения с кислотами.
Угарный газ может также действовать как восстановитель, образуя соединения с неметаллами при высоких температурах. Например, при нагревании метана с угарным газом образуется оксид углерода, который является продуктом реакции.
Группа оксидов, в которую входит угарный газ, обладает свойствами оксидов тройной связи, что позволяет им образовывать стабильные соединения с кислородом. Такие соединения могут быть использованы для получения различных веществ, например, серной кислоты.
Химические реакции угарного газа с водой и другими соединениями играют важную роль в общей химии. Изучение этих реакций помогает понять структуру молекул и связи между ними, а также способы получения различных веществ.
Оксид углерода II
Оксид углерода II химически реагирует с водой при нагревании, образуя углекислый газ и метанол:
CO(g) + H2O(l) → CO2(g) + CH3OH(l)
Угарный газ также реагирует с хлором, образуя фосген (COCl2). Этот химический процесс используется в промышленности для получения хлора.
Свойства оксида углерода II также связаны с его восстановительными свойствами. Например, оксид углерода II может восстанавливать некоторые металлы, например натрий, из их оксидов.
Взаимодействие угарного газа с серной кислотой приводит к образованию сульфоугольной кислоты:
CO(g) + H2SO4(aq) → H2CO3(aq) + SO2(g)
Оксид углерода II обладает тройной связью между атомами углерода. Его структура состоит из группы CO, где кислород образует двойную связь с углеродом, а один из его электронов образует одинарную связь с другим углеродом.
Оксиды углерода играют важную роль в промышленности. Например, оксид углерода II часто используется для получения углеродных солей, таких как угольная кислота, с помощью пропускания его через водные растворы оксидов металлов.
Таким образом, оксид углерода II имеет множество химических и физических свойств, которые делают его важным соединением в химии и промышленности. Его получение может производиться путем газификации угля или других органических материалов при высоких температурах, а также в результате неполного сгорания угля. Реакция угарного газа с водой и другими веществами может дать полезные продукты и позволяет использовать его в различных процессах.
Строение окида углерода II
Один из таких продуктов – вода – образуется в результате реакции оксида углерода II с кислородом в присутствии каталитических веществ или при высоких температурах. Другой продукт – углекислый газ – образуется при окислении углерода в оксиде углерода IV кислородом или другими окислителями.
Строение окида углерода II, известного также как оксид углерода, CO, химические свойства которого получили широкое применение в различных областях науки и техники. Он является одним из основных компонентов горючих газов в природных и технических газах. Он также является ядовитым газом с запахом слабой горелки, который может накопиться в недостаточно вентилируемых местах и представлять опасность.
| Физические свойства оксида углерода II | |
|---|---|
| Цвет газа | Безцветный |
| Цвет пламени | Синий |
| Температура кипения, ℃ | -191.5 |
| Температура плавления, ℃ | -205.1 |
| Плотность газа, кг/м³ (при 0 °C и 1 атм.) | 1.250 |
| Давление насыщенного пара, мм рт. ст. | 10, 100, 200, 300, 350 |
Оксид углерода II может образовываться не только при получении воды, но и при нагревании железных руд с коксом, а также при окислении углеродом металлов и переходными оксидами. Он может быть использован для получения углепластика и из него можно получить много видов тройных связей и множество кислых оксидов в виде различных оксидов углерода.
Получение оксида углерода II
1. Пропускание угарного газа через раскаленный винтовой нагреватель позволяет получить оксид углерода II:
2CO + O2 → 2CO2
CO2 + C → 2CO
2. Образование оксида углерода II также возможно при взаимодействии углера с оксидами некоторых галогенов, например, с хлором:
C + Cl2 → CO2 + CO
CO + Cl2 → COCl2
Общая реакция получения оксида углерода II:
C + O2 → CO2
2CO2 + C → 2CO
Оксид углерода II образуется также при облучении газовой смеси угарного газа и воды. В этом случае углерод из угарного газа восстанавливает оксид углерода II:
CO + H2O → CO2 + H2
Оксид углерода II часто используется в химических реакциях. В счет его кислых свойств он может взаимодействовать с щелочами и образовывать соль оксоаньона. Кроме того, оксид углерода II можно получить при газификации угля и других углеродсодержащих материалов высокой температурой и водяным паром:
C + H2O → CO + H2
Оксид углерода II также образуется при окислении метана (CH4):
2CH4 + 2O2 → 2CO + 4H2O
Следует отметить, что при соотношении окисления угарного газа II кислородам CO2 образуется оксид углерода IV (CO2).
Как видно из вышеуказанных реакций, образование оксида углерода II происходит через восстановление связей между атомами углерода, а также разрыв связей углерода с кислородом при взаимодействии оксидов и кислот.
Химические свойства окида углерода II
Угарный газ может взаимодействовать с водой и образовывать углеродную кислоту (H2CO3). Реакция воды с угарным газом происходит при пропускании газа через воду и идет с образованием углекислого газа (CO2) и образующейся кислоты:
| Угарный газ | Вода | Углекислый газ | Угарная кислота |
|---|---|---|---|
| CO | H2O | CO2 | H2CO3 |
Угарный газ также может образовывать реакцию с хлором, при которой образуется хлороформ (CHCl3):
CO + 3Cl2 → 2COCl2 + CCl4
Наиболее интересными химическими свойствами оксида углерода II являются его восстановительные свойства. Он может восстанавливать некоторые оксиды к натрию и метан ор. Взаимодействие оксида углерода II с окислами дает тройную реакцию, в результате которой образуются кислород и соответствующий оксид металла:
4CO + O2 → 2CO2 + C
Эта реакция широко используется в промышленности для получения кислорода из угарного газа.
Оксид углерода II также проявляет реакцию с серной кислотой, в результате которой образуется сероводород (H2S) и угольный диоксид (CO2):
CO + H2SO4 → CO2 + H2S
Эти химические свойства окида углерода II определяют его роль как восстановитель и окислитель в различных реакциях в промышленных и лабораторных условиях.
Видео:
СКОЛЬКО МОЖНО ПРОЖИТЬ БЕЗ КИСЛОРОДА
СКОЛЬКО МОЖНО ПРОЖИТЬ БЕЗ КИСЛОРОДА by GopherVid 2,602,419 views 2 years ago 16 minutes