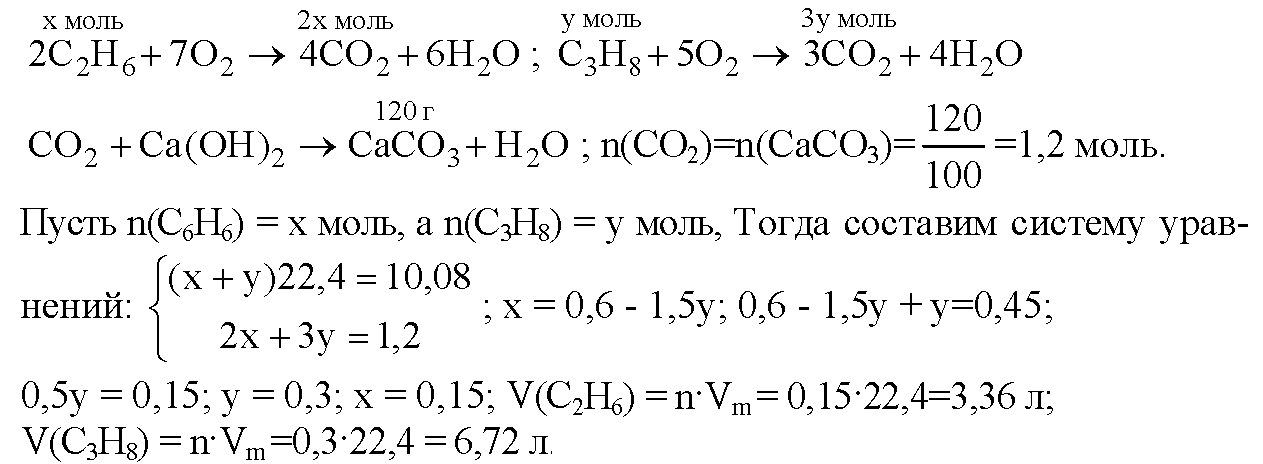- Химическое уравнение реакции ионного взаимодействия между углекислым газом и известковой водой
- Практическая работа 6 Получение оксида углерода IV и изучение его свойств Распознавание карбонатов
- Материалы и оборудование:
- Ход работы:
- Распознавание карбонатов:
- Получение оксида углерода IV и изучение его свойств
- Свойства оксида углерода IV:
- Использование индикатора в данной работе:
- Распознавание карбонатов
- Напишите молекулярное и ионное уравнение с водой
- Молекулярное уравнение:
- Ионное уравнение:
- CaCO3 + CO2 + H2O уравнение реакции
- Получение известковой воды
- Уравнение реакции
- Свойства известковой воды
- Углекислый газ, известковая вода и ионное уравнение
- Видео:
- Эксперимент «Известковая вода» из набора «Углекислый газ»
Химическое уравнение реакции ионного взаимодействия между углекислым газом и известковой водой
Углекислый газ – это пищевой газ, который содержится во многих продуктах, например, в газированных напитках. Но, кроме того, углекислый газ можно получить и путем реакции с известковой водой. Рассмотрим ионное уравнение реакции между углекислым газом и известковой водой.
Известковую воду получают, растворяя гашенный известь в воде. Если к полученному раствору добавить несколько капель фенолфталеина, то раствор приобретет качественной свойство: он станет прозрачного, а фенолфталеин, индикатор, будет окрашен в розовый цвет. Следует отметить, что известковая вода является лакмусом и может употребляться для определения кислотности растворов.
Когда в пробирку добавляют известковую воду и пропустите через нее углекислый газ, то в результате реакции образуется отложение белого цвета, которое наблюдаете на стенках пробирки. Это осадок представляет собой мела (углерода) и карбонат-ионы (CO32-). Молекулярное уравнение этой реакции выглядит следующим образом:
CO2 + Ca(OH)2 → CaCO3 + H2O
В ионном уравнении эта реакция записывается так:
CO2(g) + 2OH—(aq) → CO32-(aq) + H2O(l)
Также возможно растворение полученного осадка в кислотной среде с образованием соответствующей соли. Например, растворение осадка CaCO3 в соляной кислоте приводит к образованию Na2CO3 и NaCl:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g)
В результате этой реакции выделяется газ углекислый газ (СO2) и образуется раствор CaCl2 в воде. Таким образом, реакция между углекислым газом и известковой водой является примером качественной реакции с выделением газа и образованием соли.
Практическая работа 6 Получение оксида углерода IV и изучение его свойств Распознавание карбонатов
Материалы и оборудование:
- Известковая вода (Ca(OH)2)
- Уксусная кислота (CH3COOH)
- Растворимая соль натрия (NaCl)
- Вода (H2O)
- Раствор сульфата меди (II) (CuSO4)
Ход работы:
- В стеклянную колбу налейте известковую воду (Ca(OH)2) и добавьте несколько капель уксусной кислоты (CH3COOH).
- Наблюдайте, как в результате реакции образуется белый осадок и выделяется углекислый газ (CO2), который можно увидеть благодаря образованию прозрачного газового пузыря на поверхности раствора.
- Определите наличие углекислого газа, проведя ряд химических тестов:
Распознавание карбонатов:
- Добавьте в полученный раствор раствор сульфата меди (II) (CuSO4) и наблюдайте, как образуется осадок медного карбоната (CuCO3) в виде мела (белого осадка).
- Добавьте несколько капель раствора сульфата меди (II) (CuSO4) в другую порцию известковой воды, в которой отсутствует углекислый газ (CO2). Наблюдайте, как не образуется осадок медного карбоната (CuCO3), что свидетельствует об отсутствии карбонат-ионов (CO32-) в растворе.
Экспериментально полученный углекислый газ (CO2) используется в промышленности для улучшения качества пищевых продуктов и в других процессах. Карбонаты, которые содержат карбонат-ионы (CO32-), также широко используются в различных отраслях промышленности.
Получение оксида углерода IV и изучение его свойств
CO2 + Ca(OH)2 → CaCO3 + H2O
Для выполнения этой практической работы поместите известковую воду (раствор гидроксида кальция) в колбу с газоотводной трубкой. Затем начните подавать углекислый газ (CO2) в колбу с помощью газоотводной трубки. При этом произойдет реакция между CO2 и Ca(OH)2, и полученный молочный осадок будет оседать на дне колбы. Вода в колбе обесцветится из-за реакции между гидроксидом кальция и углекислым газом. Если добавить немного барита на дно колбы, то будет видно, как сначала осадок помутнеет, а затем станет молочным.
Данная реакция характерна для всех карбонатов кальция. Реакция между углекислым газом и гидроксидом кальция является примером осаждения соединения. Углекислый газ (CO2) из воздуха реагирует с гидроксидом кальция (Ca(OH)2), что приводит к образованию молочного осадка. Молочный осадок образуется из-за выделения карбоната кальция (CaCO3) и воды.
Свойства оксида углерода IV:
- Оксид углерода IV, также известный как диоксид углерода (CO2), является бесцветным и без запаха газом в стандартных условиях.
- CO2 обладает химической формулой CO2 и молекулярной массой около 44 г/моль.
- Оксид углерода IV является неполярным молекулой и обладает линейной геометрией.
- CO2 не поддерживает горение и не является горючим веществом.
- Оксид углерода IV является растворимым в воде, при контакте с которой образует угольную кислоту.
- CO2 используется в промышленности для формирования газовой среды в реакционных процессах и для охлаждения.
- Углекислый газ также является вызывающим веществом и используется в продуктах химической обработки, таких как содовые напитки и пиво.
Использование индикатора в данной работе:
Для определения завершения реакции и образования оксида углерода IV можно использовать индикаторы, такие как фенолфталеин или лакмусовая бумага. Например, при воздействии на реакционную смесь фенолфталеина, он изменит свой цвет из безцветного в розовый при достижении щелочной среды (при получении углекислого газа). Лакмусовая бумага также может быть использована для определения щелочной среды — она будет окрашена в синий цвет при достижении щелочной реакции.
Таким образом, получение оксида углерода IV из углекислого газа и известковой воды является интересной практической работой, которая позволяет изучить свойства данного вещества и провести химический эксперимент.
Распознавание карбонатов
Карбонаты представляют собой растворимые в воде соли, которые образуют осадок при воздействии с кислотой или другими специфическими веществами. Для распознавания карбонатов можно провести химическую реакцию с известковой водой и углекислым газом.
Для этого необходимо взять пробирку с водой и добавить небольшое количество известковой воды (Ca(OH)2) в раствор. При добавлении Ca(OH)2 в воду происходит реакция нейтрализации, при которой образуется осадок белого гидроксида кальция (Ca(OH)2).
Далее, к полученному раствору добавляют углекислый газ (CO2) путем пропускания воздуха через раствор. Углекислый газ связан с водой и образует карбоновую кислоту (H2CO3) в растворе.
Наблюдаете вышеописанную реакцию с добавлением раствора с Ca(OH)2 можно с помощью добавления фенолфталеина и лакмуса. При добавлении фенолфталеина в раствор появляется красный цвет, а при добавлении лакмуса — голубой. Эти цветовые изменения являются индикаторами наличия карбонатов в растворе.
Работа с карбонатами также связана с изучением ионного уравнения, в котором представлены молекулярные и ионные формулы веществ, участвующих в реакции. Например, уравнение реакции между известковой водой и углекислым газом может быть представлено так:
| Исходные вещества | Продукты реакции |
|---|---|
| Ca(OH)2 + CO2 | CaCO3 + H2O |
Таким образом, распознавание карбонатов основано на реакции между известковой водой и углекислым газом, а также на наблюдении цветовых изменений при добавлении фенолфталеина и лакмуса к раствору. Этот метод часто используется в химической и пищевой промышленности для получения и исследования карбонатов.
Напишите молекулярное и ионное уравнение с водой
Молекулярное уравнение:
CaCO3 + H2O + CO2 → Ca(OH)2 + CO2
Ионное уравнение:
CaCO3 + 2H2O + CO2 → Ca(OH)2 + CO2
Реакция начинается с помещения углекислого газа в растворимую известковую воду (CaCO3). В результате химической реакции образуется нерастворимый осадок молочного гидроксида (Ca(OH)2) и выделяется углекислый газ (CO2).
Углекислый газ играет важную роль в пищевой промышленности, а также в получении известковой воды. При реакции с водой он образует углекислую кислоту (H2CO3), которая далее реагирует с кальцием и образует молочный гидроксид (Ca(OH)2).
Реакцию можно наблюдать с помощью окрашивания лакмусовой бумажки. Исходная растворимая известковая вода имеет голубой цвет, но после реакции с углекислым газом лакмусовая бумажка становится красной. Это является индикатором нейтрализации.
Молекулярные и ионные уравнения позволяют легче понять химические реакции, происходящие с водой и другими веществами.
CaCO3 + CO2 + H2O уравнение реакции
Получение известковой воды
Известковая вода получается путем растворения карбоната кальция (CaCO3) в воде, присутствующей в атмосфере, что приводит к образованию ионов кальция (Ca2+) и карбонат-ионов (CO32-).
Уравнение реакции
Уравнение реакции между CaCO3, CO2 и H2O можно записать следующим образом:
CaCO3 + CO2 + H2O → Ca2+ + 2HCO3-
В результате нейтрализации известковой воды с углекислым газом получаются ионы кальция и два иона гидрокарбоната.
Свойства известковой воды
Известковая вода обладает свойством обесцвечиваться в результате добавления к ней фенолфталеина, что связано с образованием нерастворимого осадка — карбоната кальция (CaCO3).
Также известковая вода проявляет щелочные свойства, что выражается в возникновении щелочного окрашивания лакмуса при контакте с этим веществом.
Изучение свойств и реакций известковой воды имеет большое значение в химии и промышленности, особенно в процессах нейтрализации и получения карбонат-ионов, которые широко используются в различных отраслях.
Углекислый газ, известковая вода и ионное уравнение
Когда углекислый газ (CO2) взаимодействует с водой (H2O), образуется слабая кислота – угольная кислота (H2CO3). Эта реакция связана с химическими свойствами углекислого газа и его взаимодействием с водой.
Окрашивание фенолфталеина в растворе натрия (NaOH) и его обесцвечивание в результате реакции с углекислым газом также объясняется ионным уравнением.
Ионное уравнение реакции между углекислым газом (CO2) и известковой водой (Ca(OH)2):
Ca(OH)2 + CO2 → CaCO3 + H2O
Результатом этой реакции является образование молочного раствора карбоната кальция (CaCO3) и воды (H2O). При добавлении фенолфталеина в раствор известковой воды (Ca(OH)2), он окрашивается в голубой цвет из-за присутствия гидроксид-ионов (OH-) в растворе. Однако, при взаимодействии углекислого газа (CO2) с известковой водой (Ca(OH)2), гидроксидные ионы (OH-) реагируют с углекислым газом и образуют карбонаты (CO32-), вызывающие помутнение раствора и обесцвечивание фенолфталеина.
Таким образом, реакция углекислого газа с известковой водой является результатом нейтрализации щелочи (натрия гидроксида) углекислым газом и представляет собой ионное уравнение, которое иллюстрирует полный процесс реакции.
Видео:
Эксперимент «Известковая вода» из набора «Углекислый газ»
Эксперимент «Известковая вода» из набора «Углекислый газ» by MEL Chemistry на русском 3,527 views 6 years ago 1 minute, 59 seconds