- Феномен кипения воды: изучение внутренней энергии системы пар-вода
- Внутренняя энергия системы вода пар при кипении
- Кипение и удельная теплота парообразования
- Что такое кипение
- Различия между испарением и кипением
- Процессы кипения и конденсации на графиках
- Температура кипения и как ее найти на графике
- Температуры кипения некоторых веществ
- Почему температура жидкости при кипении не изменяется
- Как давление влияет на температуру кипения
- Что такое удельная теплота парообразования
- Что происходит с энергией во время кипения и конденсации
- Видео:
- Урок 187. Испарение и конденсация. Насыщенный пар и его свойства
Феномен кипения воды: изучение внутренней энергии системы пар-вода
Вода – одно из наиболее распространенных и удивительных веществ на Земле. У каждого из нас есть представление о ее свойствах и состояниях, но мало кто задумывается о том, каким образом происходит переход воды из жидкого состояния в состояние пара при кипении.
Формула воды (H2O) известна всем. Именно благодаря ей происходит кипение: водные молекулы образуют пар, что сопровождается поглощением энергии. Каждая конкретная молекула воды с определенной температурой начинает испаряться, и только когда большинство молекул образовало пар, вода начинает кипеть. Кипение – это процесс, в результате которого межмолекулярные силы притяжения вещества практически исчезают и его давление уравнивается с давлением внешней среды.
Цельсий. Скажи, а что происходит со внутренней энергией воды при кипении? Оказывается, она не увеличивается с ростом температуры, а испарением! Когда водная молекула преодолевает межмолекулярные связи и переходит в состояние пара, она получает потенциальную энергию – теплоту, которая ранее была связана с энергией притяжения молекул жидкости. Нагревание жидкости влечет за собой увеличение среднеквадратичной скорости движения молекул, и это влияет на кипение. Температура при которой начинается процесс кипения, называется температурой кипения данного вещества при данном давлении.
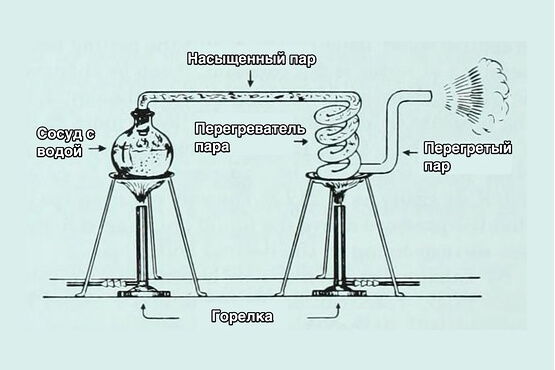
Чтобы разобраться, что происходит внутри воды во время кипения, рассмотрим рисунок. Именно на нем всё видно своими глазами! Внутренняя энергия вещества различается при разной температуре. Изображение вещества при относительно низкой температуре отличается ледяным цветом. С ростом температуры, внутренняя энергия увеличивается, и вещество преображается в жидкое состояние, уже изображенное зеленым цветом. Однако, самая интересная и отличающаяся особенность происходит именно при кипении. Внутренняя энергия теперь изображена красным цветом. Это можно объяснить тем, что при кипении состояние вещества изменяется, образуются новые связи и области более высокой энергии. Такое отличие позволяет нагреть вещество путем постепенного повышения его температуры и, следовательно, энергии.
Внутренняя энергия системы вода пар при кипении
Одной из основных физических характеристик вещества, влияющей на процесс кипения, является температура. При повышении температуры воды, внутренняя энергия системы также увеличивается. Во время кипения, когда вода переходит в парообразное состояние, часть предоставленной энергии тратится на изменение агрегатного состояния молекул вещества, а оставшаяся энергия обеспечивает увеличение температуры пара.
Графики, отображающие зависимость внутренней энергии системы от температуры при кипении воды, различаются в зависимости от количества воды и удельной теплоемкости каждой конкретной системы. Левая наклонная линия на графике представляет увеличение внутренней энергии воды до температуры кипения. После этого, внутренняя энергия системы остается постоянной в течение процесса кипения, так как энергия тратится на изменение состояния молекул воды.
Правая наклонная линия на графике показывает увеличение внутренней энергии пара во время кипения. Так как температура пара выше комнатной, его внутренняя энергия также выше. В процессе кипения внутренняя энергия пара остается постоянной, так как энергия тратится на противодействие атмосферному давлению и конденсацию пара обратно в воду.
Таким образом, внутренняя энергия системы вода пар при кипении зависит от температуры и количества вещества. Внутренняя энергия увеличивается при испарении и изменении состояния воды в парообразное состояние, а также при нагревании пара. Для более точной оценки внутренней энергии необходимо учитывать конкретные значения температуры, количества воды и удельной теплоемкости системы.
Кипение и удельная теплота парообразования
На графике парообразования вода-пар отображается зависимость между температурой воды и количеством теплоты, необходимым для ее изменения от жидкости в кипящую воду. Красная линия на графике представляет равновесие между жидкостью и паром во время кипения.
Во время кипения жидкости молекулы не только движутся, но и выполняют работу внутренней энергии. Эта работа осуществляется при переходе между двумя состояниями вещества — жидкостью и паром. При этом удельная теплота парообразования — это количество энергии, которую физики предварительно высчитывают, чтобы увеличить давление на жидкость и преобразовать ее в пар.
Таким образом, во время кипения внутренняя энергия системы вода-пар увеличивается за счет работы между молекулами жидкости и их перемещением в парообразное состояние. Удельная теплота парообразования температурно зависит от конденсации воды и количества работы, необходимой для изменения ее состояния.
Именно при кипении вода претерпевает фазовый переход и превращается в пар. Это происходит при достижении определенной температуры и давления. Состояние равновесия между жидкостью и паром обеспечивается при кипении, и в этом состоянии пар обладает удельной теплотой парообразования.
На рисунке показаны графики удельной теплоты парообразования воды при различных температурах. В каждой точке линии графика отображается соответствующее значение удельной теплоты парообразования для данной температуры, которая изменяется от некоторых значений до конечных. Чем выше температура, тем больше удельная теплота парообразования воды.
Что такое кипение
Внутренняя энергия системы вещества правильно будет тем, что отражает сумму кинетической энергии молекул и их потенциальной энергии в результате притяжения друг к другу. При снижении внутренней энергии системы плотность жидкости увеличивается, а при ее увеличении – уменьшается.
Кипение происходит, когда внутренняя энергия достигает такого значения, что ее температура становится равной (или выше) температуры кипения при данном давлении. В этот момент начинается оживленное движение молекул, которые приобретают достаточно энергии для преодоления притяжения друг к другу и образования пара.
При кипении жидкость тратит теплоту на преодоление притяжения между молекулами, именно поэтому она не нагревается выше температуры кипения.
Этот процесс парообразования происходит на противоположной стороне кипящей жидкости относительно ее поверхности. Молекулы пара имеют более высокую энергию, чем кипящая жидкость, поэтому внутренняя энергия пара будет выше, чем внутренняя энергия жидкости.
На графике зависимости внутренней энергии от температуры внутренняя энергия жидкости находится слева, а внутренняя энергия пара — справа. Во время кипения, при постоянной температуре, график имеет общий участок.
Различия между испарением и кипением
- Теплота, необходимая для испарения и кипения, различна. При испарении воды теплота перевода составляет около 600 кал/г, а при кипении — примерно 540 кал/г.
- Графики теплоты перевода в зависимости от температуры для испарения и кипения также различаются. На графике испарения красная линия наклонная, что указывает на увеличение энергии, необходимой для испарения воды при повышении температуры. В то же время, на графике кипения голубая линия горизонтальная, что означает стабильную теплоту перевода при постоянной температуре кипения.
- При кипении вся вода в кипящей жидкости превращается в пар, в то время как при испарении только часть жидкости переходит в парообразное состояние.
- Кипение происходит при определенной температуре (для чистой воды при атмосферном давлении это 100°C), в то время как испарение может происходить при любой температуре.
- Испарение зависит от давления, которое влияет на скорость испарения, в то время как кипение происходит при конкретном давлении.
- Кипение сопровождается движением пара, тогда как при испарении пар не образуется в таких количествах, чтобы вызвать заметное движение.
- Кипение сопровождается работой, так как происходит переход от жидкости в газообразное состояние. Однако работа при испарении часто не учитывается или не представлена на графиках.
- Кипящая вода имеет определенное давление, которое зависит от ее температуры. Однако испарение не приводит к закипанию, так как при испарении частицы пара взаимодействуют только с верхними слоями жидкости.
Итак, испарение и кипение — это два различных процесса, которые имеют свои особенности и зависят от разных факторов, таких как температура и давление. Понимание различий между этими процессами является важным для понимания тепловых процессов и физических свойств воды.
Процессы кипения и конденсации на графиках
Процессы кипения и конденсации вода пара могут быть проиллюстрированы на графиках, которые наглядно показывают зависимость давления и температуры от времени.
На графиках, представленных ниже, мы можем увидеть, как изменяется давление и температура в различные моменты времени при кипении и конденсации жидкости.
На левой части графика, отмеченной «Кипение», мы видим, что при повышении температуры кипящей жидкости давление также увеличивается. Это объясняется тем, что при кипении молекулы жидкости образующую пузырьки пара и вода испаряется.
По мере повышения температуры, все больше молекул жидкости приобретают достаточную энергию для испарения. На графике это продемонстрировано увеличением давления с ростом температуры.
С другой стороны, на правой части графика, помеченной «Конденсация», мы можем наблюдать, как при снижении температуры кипящей жидкости давление уменьшается. Это объясняется тем, что молекулы пара теряют свою энергию и превращаются в жидкость.
По мере снижения температуры, все больше молекул пара теряют свою энергию и возвращаются в состояние жидкости. На графике это проиллюстрировано уменьшением давления с уменьшением температуры.
Таким образом, на этих графиках мы можем наблюдать, как давление и температура связаны между собой во время кипения и конденсации воды. Когда жидкость закипает, она поглощает теплоту и выполняет работу воздуха, который окружает пузырьки. Поэтому внутренняя энергия системы вода пар при кипении изменяется.
Температура кипения и как ее найти на графике
На графике изменения внутренней энергии системы вода-пар при кипении можно увидеть, как температура воды вначале увеличивается. Когда достигается температура кипения, процесс парообразования начинается, и температура воды больше не изменяется.
В процессе кипения энергия, полученная от работы по поглощению теплоты, распределяется между молекулами жидкости. Тепловая энергия используется для преодоления взаимного притяжения молекул, и они начинают двигаться быстрее. При достижении температуры кипения, энергия используется для преодоления этих сил и испарения молекулами жидкости.
Температура кипения различных жидкостей зависит от их внутренней энергии и количества теплоты, которое необходимо поглотить для их преобразования в парообразное состояние. Также температура кипения связана с давлением, при котором происходит кипение.
На графике можно заметить линии, представляющие температуру кипения различных веществ. Вначале линия поднимается слева от комнатной температуры, показывая, что температура жидкости увеличивается. Затем, при температуре кипения, линия становится горизонтальной, что указывает на то, что происходит парообразование и температура не изменяется. Против линии между этими двумя точками показывает, что при понижении температуры некоторых веществ происходит обратный процесс – конденсация и переход из парообразного состояния в жидкость.
Температуру кипения можно найти на графике, исследуя изменение внутренней энергии системы во время кипения. Когда внутренняя энергия системы достигает значения, соответствующего температуре кипения, происходит парообразование.
Итак, температура кипения и процесс кипения веществ связаны с внутренней энергией системы, тепловой энергией и движением молекул. На графике можно найти температуру кипения, а также увидеть изменения внутренней энергии при кипении воды или других жидкостей. Этот процесс играет важную роль в физике и имеет множество применений в различных областях науки и техники.
Температуры кипения некоторых веществ
В физике такое явление, как кипение, связано с процессами изменения фазы вещества. Во время кипения вода, например, испаряется, и в результате образуется пар. Для перевода жидкости в пар необходимо увеличить энергию молекул, что выполняется за счет их нагревания.
Каждая конкретная жидкость имеет свою температуру кипения при определенном давлении. На рисунках и графиках можно найти зависимость температуры кипения от давления для различных веществ. В общем случае, с увеличением давления температура кипения тоже возрастает. Это особенно видно на наклонной части графика, где происходит кипение и жидкость переходит в пар.
Некоторые вещества имеют очень низкую температуру кипения. Например, вода кипит при 100 градусах Цельсия при нормальном атмосферном давлении. Другие вещества, наоборот, имеют очень высокие температуры кипения, например, золото кипит при 2856 градусах Цельсия.
Температура кипения каждого вещества зависит от его свойств, особенностей молекулярной структуры и количества молекул вещества. Например, в воде большое количество молекул, которые тесно связаны друг с другом из-за сил притяжения. Это обуславливает большую внутреннюю энергию вещества и более высокую температуру кипения.
Также температура кипения может изменяться в зависимости от внешних факторов, таких как давление. Повышение давления обычно повышает температуру кипения, а понижение — снижает. Это связано с изменением внутренней энергии молекул и их свободного движения при различном давлении.
Изучение температур кипения различных веществ позволяет получить информацию о их физических свойствах и использовать ее в различных отраслях науки и техники. Например, знание температуры кипения может быть полезно при разработке новых материалов, в процессе выделения чистых веществ из смесей и в других областях.
Почему температура жидкости при кипении не изменяется
Когда жидкость переходит в парообразное состояние при кипении, ее температура остается постоянной, несмотря на поступление теплоты. Это может показаться странным, так как обычно предполагается, что нагревание вещества приводит к повышению его температуры. Однако, при кипении происходит процесс перехода жидкости в пар, который требует большого количества энергии.
Что происходит с молекулами воды, когда она кипит? На рисунке ниже показаны две графики: первая показывает изменение температуры воды при нагревании, а вторая — изменение температуры воды и пара при кипении.
| График 1: Температура жидкости при нагревании | График 2: Температура жидкости и пара при кипении |
Как видно из графика 1, температура воды увеличивается с увеличением количества теплоты, которую она получает. Это происходит до тех пор, пока температура воды не достигнет точки кипения (обычно 100 градусов по Цельсию при нормальном атмосферном давлении).
На графике 2 видно, что при достижении точки кипения, температура жидкости перестает расти и остается постоянной. Вместо того, чтобы повышаться, поступающая вода вливается прямо в пар на поверхности жидкости. В этом процессе происходит массовое испарение жидкости, при котором молекулы воды образуют пар, покидая жидкость.
Энергия, переданная воде для превращения ее в пар, называется теплотой парообразования. Эта энергия нужна для преодоления сил межмолекулярного притяжения в жидкости и превращения молекул в парообразное состояние. Процесс испарения требует значительного количества энергии, поэтому при кипении вода поглощает теплоту без изменения своей температуры.
Следует отметить, что образовавшийся пар имеет ту же температуру, что и вода до кипения. Таким образом, температура пара также остается постоянной.
Иными словами, при кипении происходит тепловая обработка вещества, в результате которой вода получает энергию, не вызывающую изменения ее температуры. С точки зрения внутренней энергии системы, наклонная линия на графике 2 представляет собой увеличение энергии воды всей системы в процессе кипения. Таким образом, тепловая энергия переходит от молекул вода в молекулы пара.
Как давление влияет на температуру кипения
Когда количество энергии, представленной в виде теплоты, достаточно большое, чтобы преодолеть силы притяжения между молекулами вещества, происходит парообразование. Однако, если вода находится под давлением, молекулы испаряются сильнее, чтобы преодолеть дополнительное сопротивление, создаваемое воздействием внешнего давления. Поэтому температура кипения вещества будет отличаться при разных давлениях.
Чтобы лучше разобраться, почему давление влияет на температуру кипения, рассмотрим график, представленный на графиках внутренней энергии и линии изотермы жидкостей:
1. На левой части графика мы видим зависимость между внутренней энергией и температурой при постоянном давлении. Здесь изображен процесс нагревания вещества до точки кипения. По мере нагревания, внутренняя энергия растет и температура также увеличивается.
2. В точке кипения происходит испарение – молекулы начинают переходить из жидкостного состояния в газообразное. При этом внутренняя энергия уже не изменяется, но она превращается в потенциальную энергию парообразования.
3. Когда вода находится под давлением, линия изотермы смещается вверх, то есть при одной и той же температуре давление увеличивается. Таким образом, чтобы вода начала кипеть при повышенном давлении, нужно увеличить ее внутреннюю энергию. Следовательно, температура кипения увеличивается.
4. Обратно, если давление снижается, то и температура кипения уменьшается. Это связано с тем, что молекулам воды будет легче преодолеть силы притяжения друг к другу и испариться.
Таким образом, вода будет кипеть при разных температурах в зависимости от давления, при котором происходит кипение. Исследование влияния давления на точку кипения помогает лучше понять свойства веществ и их фазовые переходы.
Что такое удельная теплота парообразования
В процессе парообразования воды при ее кипении происходит поглощение тепловой энергии. Вначале, при понижении давления, вода нагревается и находится в жидком состоянии. На графике температуры в зависимости от количества теплоты, линия будет наклонная и соответствовать комнатной температуре.
Однако, при достижении определенного значения давления (равного давлению насыщенного пара при данной температуре), начинает происходить процесс кипения воды. Вода превращается в парообразное состояние и находится на горе в зависимости от количества теплоты.
Парообразование — это процесс, в котором жидкость превращается в газ (пар) при поглощении теплоты. Поэтому, удельная теплота парообразования определяет, сколько энергии необходимо потратить на парообразование единицы вещества при конкретной температуре.
Различия между удельной теплотой парообразования и удельной теплотой конденсации воды заключаются именно в том, что у парообразования теплота поглощается, а в случае конденсации теплота высвобождается.
Таким образом, удельная теплота парообразования воды представлена в виде линии на графике температуры и количества теплоты. Эта линия может быть наклонной или горизонтальной в зависимости от температуры.
Что происходит с энергией во время кипения и конденсации
Во время кипения и конденсации происходят важные изменения во внутренней энергии системы вода-пар. При нагревании жидкости до температуры кипения, на поверхности жидкости начинают образовываться пузырьки пара, так как теплота преобразуется в энергию испарения. При этом, внутренняя энергия системы не изменяется, но происходит увеличение количества движущихся молекул.
Когда температура достигает точки кипения, жидкость начинает испаряться быстрее, а внутренняя энергия системы начинает увеличиваться. Это связано с тем, что для испарения жидкости требуется поглощение теплоты. При этом, температура жидкости остается постоянной, так как все поступающие вещества используются для преобразования из жидкого состояния в пар.
При конденсации пара, происходит обратный процесс: внутренняя энергия системы уменьшается, а теплота переходит из газообразного состояния в жидкое. Это означает, что пара отдаёт свою энергию для превращения обратно в жидкость.
Изменение температуры во время кипения и конденсации можно представить с помощью графиков на рисунках. Кипение происходит при постоянной температуре, пока есть жидкость. Когда весь пар конденсируется обратно в жидкость, температура стабилизируется на точке кипения.
Теплота, связанная с изменением внутренней энергии системы, представлена следующей формулой:
Q = mL,
где Q — теплота, m — масса вещества, L — теплота испарения.
Таким образом, при кипении и конденсации внутренняя энергия системы вода-пар изменяется, а теплота переходит между различными состояниями вещества. Эти процессы могут быть проиллюстрированы графиками, показывающими зависимость температуры от времени или от давления.
При повышении температуры вода может перейти в паровое состояние, а при снижении температуры — из парового состояния в жидкостное. Таким образом, изменение температуры связано с изменением внутренней энергии системы вода-пар.
Изучение процессов кипения и конденсации важно не только для понимания физических свойств воды, но и для применения в различных сферах, например, для выработки электроэнергии или при промышленных процессах.
Видео:
Урок 187. Испарение и конденсация. Насыщенный пар и его свойства
Урок 187. Испарение и конденсация. Насыщенный пар и его свойства by Павел ВИКТОР 188,799 views Streamed 8 years ago 38 minutes