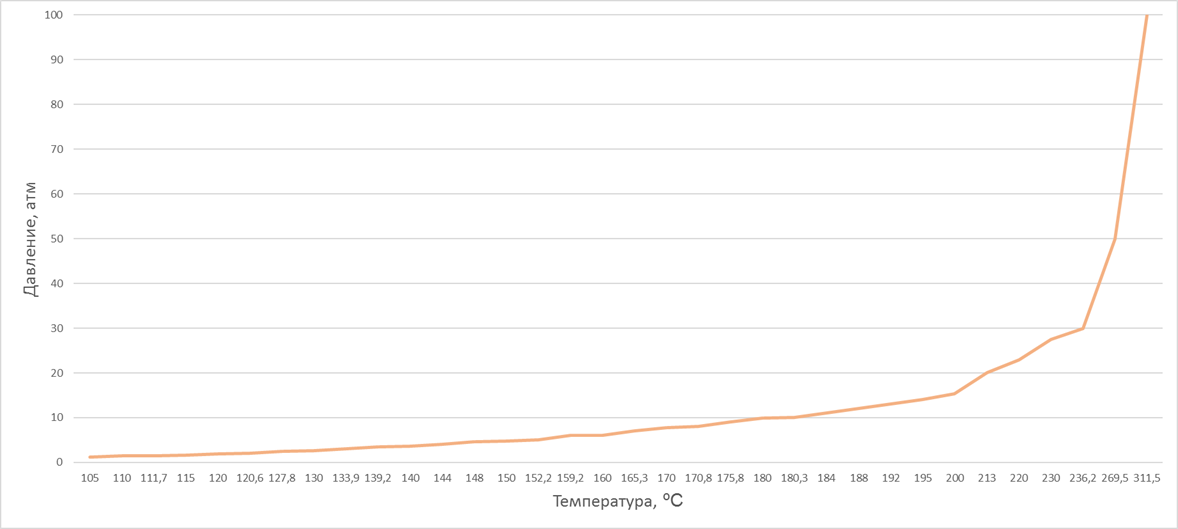
- Каково давление при температуре воды 115 градусов?
- Температура кипения воды в зависимости от давления 4 фактора таблица для расчёта
- Как будет меняться температура кипения воды 4 фактора
- Влияние атмосферного давления
- Температура кипения в горах
- Температура кипения воды в шахте
- Применение герметической крышки
- Кипячение воды в вакууме
- Кипение солёной воды
- Температура кипения воды в чайнике
- Таблица температуры кипения воды при различных условиях
- Удельная теплоемкость
- Видео:
- Урок 124 (осн). Зависимость температуры кипения жидкости от давления
Каково давление при температуре воды 115 градусов?
Вода при атмосферном давлении кипит при температуре 100 °C. Это агрегатное состояние воды, при котором жидкость переходит в пар. Но что происходит с водой при более высоких температурах, например, при 115 °C? На этом экстремальном уровне температуры вода находится в состоянии, которое не вполне понято и изучено.
При низком атмосферном давлении и повышенной температуре вода может принять форму пара. А вот при более высоком давлении и более низкой температуре вода может находиться в состоянии, близком к кипению. Это связано с тем, что при повышении давления на данной температуре происходит уменьшение объема пара, что повышает его плотность и предотвращает полное кипение воды.
Таким образом, вода при 115 градусах находится в особом состоянии, которое является промежуточным между жидкостью и паром. В этом состоянии вода содержит множество мельчайших пузырьков, выпуская их при дальнейшем увеличении давления или снижении температуры. Для проверки данной зависимости существует формула, которая позволяет определить давление на любой температуре воды.
Температура кипения воды в зависимости от давления 4 фактора таблица для расчёта
Объясняется это тем, что при повышении давления молекулы воды более плотно упаковываются внутри жидкости, и для их перехода в парообразное состояние требуется более высокая энергия. Следовательно, температура кипения воды будет выше при повышении давления и ниже при снижении.
Вода, кипящая под давлением, может достигать температуры выше 100 градусов Цельсия. Например, при давлении 115 пси (паундов на квадратный дюйм) температура кипения воды составит около 310 градусов Цельсия. Это объясняется изменением скорости парообразования, что приводит к повышению температуры.
Температура кипения воды также может быть изменена в зависимости от состава воды и давления. Например, добавление солей или других компонентов может повысить или понизить температуру кипения. Это часто используется при приготовлении пищи, например, при использовании соленой воды для варки макаронных изделий или яиц.
Другой фактор, влияющий на температуру кипения воды, — емкость или объем сосуда. При увеличении объема сосуда температура кипения воды снижается, так как молекулы воды имеют больше пространства для движения и более свободно взаимодействуют с воздушными молекулами.
Зависимость температуры кипения воды от давления хорошо изучена и определена в таблицах, основанных на исследованиях и экспериментах. Эти таблицы позволяют определить температуру кипения воды в зависимости от заданного давления. Такая информация полезна в инженерных расчетах, например, при проектировании систем охлаждения или герметической упаковки продуктов.
Использование этих таблиц и знание взаимосвязи между температурой кипения и давлением важно для ряда отраслей, таких как атмосферное и хозяйственное хозяйство, где контроль над температурой и давлением имеет большое значение.
Как будет меняться температура кипения воды 4 фактора
Температура кипения воды зависит от нескольких факторов, которые можно разделить на следующие категории:
- Влияние атмосферного давления: Обычно вода кипит при температуре 100 градусов Цельсия на уровне моря. С увеличением высоты над уровнем моря атмосферное давление уменьшается, что приводит к понижению температуры кипения. Например, в горах, где атмосферное давление ниже, вода может начать кипеть при температурах ниже 100 градусов.
- Применение дополнительных веществ: Добавление солей или других веществ в воду может повысить ее температуру кипения. Как правило, соленая вода кипит при температуре выше 100 градусов Цельсия. Это объясняется изменением энергии, необходимой для превращения жидкости в газовое состояние в присутствии солей.
- Изменение теплоемкости воды: Теплоемкость вещества определяет, сколько тепла необходимо для его нагрева. Вода имеет высокую теплоемкость, поэтому она может нагреваться на много градусов, прежде чем начнет кипеть. С другой стороны, вещества с низкой теплоемкостью, например, металлы, могут начать кипеть при намного более низких температурах.
- Влияние закрытой системы: Если вода нагревается в герметической системе, где нагреваемое вещество не может стекать или испаряться, точка кипения может быть выше 100 градусов Цельсия. Это происходит из-за увеличения давления в герметической системе, которое подвижно в таблице. Например, вода в шахте могла бы кипеть при температуре 115 градусов.
Зависимость температуры кипения воды от этих факторов предоставлена в следующей таблице:
| Фактор | Влияние на температуру кипения |
|---|---|
| Атмосферное давление | Уменьшение высоты над уровнем моря приводит к снижению температуры кипения |
| Добавление солей | Повышение температуры кипения |
| Теплоемкость воды | Высокая теплоемкость воды позволяет ей нагреваться до более высоких температур перед кипением |
| Герметическая система | Увеличение давления в закрытой системе приводит к повышению температуры кипения |
Разное применение воды и ее состояния и каком теплом оно находится в справочнике сайта dpvaru.
Влияние атмосферного давления
Атмосферное давление оказывает значительное влияние на многие процессы, связанные с водой. Вода кипит при температуре 100 градусов по Цельсию при нормальном атмосферном давлении (1013,25 мбарабс), однако этот показатель может меняться в зависимости от давления.
При повышенном атмосферном давлении, например, 115 градусов Цельсия оказывается недостаточно для выкипания воды в чайнике. Это связано с тем, что вода не может перейти в паровую фазу из-за давления, которое создает чайник. Поэтому, вода остается в жидком состоянии, несмотря на высокую температуру.
Важно отметить, что при кипячении воды под давлением в мультиварке или герметичной посуде, температура воды может превышать 100 градусов и доходить до 115 градусов Цельсия, что позволяет более быстро приготовить пищу. Действующее давление и температура можно рассчитать с помощью формулы Клапейрона.
На космической станции, где отсутствует атмосферное давление, вода будет выкипать уже при низкой температуре около 37 градусов Цельсия. Это связано с низким давлением, при котором вода переходит из жидкого состояния в паровое без перехода через стадию кипения.
Атмосферное давление также влияет на температуру, при которой убиваются микробы. При высоком давлении поддерживается более высокая температура кипения, что способствует более эффективному уничтожению бактерий в продуктах. Это часто используется при консервировании сырых продуктов.
Таким образом, атмосферное давление является одним из основных факторов, влияющих на кипение и кипячение воды. Оно определяет температуру, при которой вода переходит из жидкого состояния в газообразное, и контролирует много других процессов, связанных с водой.
В таблице ниже приведены значения температуры кипения воды при различных атмосферных давлениях:
- 0 мбарабс (вакуум) – 32 °F (0 °C)
- 1000 мбарабс – 212 °F (100 °C)
- 2000 мбарабс – 226 °F (108 °C)
- 3000 мбарабс – 238 °F (114 °C)
- 4000 мбарабс – 248 °F (120 °C)
- 5000 мбарабс – 258 °F (126 °C)
Теплоемкость воды также зависит от атмосферного давления. При повышенном давлении теплоемкость воды снижается, что позволяет быстрее нагревать продукты под высоким давлением.
Исследования показывают, что в условиях горной местности, где атмосферное давление ниже, вода кипит уже при температуре ниже 100 градусов Цельсия, что может затруднять приготовление пищи.
Вода, содержащая в себе растворенный хлор, имеет более низкую температуру кипения, чем чистая вода. Это связано с тем, что хлор обладает низкой теплоемкостью и менее прочными прочностью по сравнению с водой.
Таким образом, атмосферное давление играет важную роль в различных процессах, связанных с водой. Оно влияет на температуру кипения, теплоемкость и другие параметры, которые определяют свойства воды при разных условиях.
Температура кипения в горах
Как известно, температура кипения воды зависит от давления. Обычно вода начинает кипеть при температуре 100 градусов Цельсия под атмосферным давлением. Однако, в горах этот процесс может происходить при более низких температурах.
Возникает вопрос: как это возможно? Все дело в том, что на высоте над уровнем моря атмосферное давление снижается, поэтому просто изменяется среднее значение давления, при котором кипение начинается. Если меньше давление, то и температура кипения будет ниже.
Подробно рассмотрим процесс кипения под действием уменьшенного давления в герметической кастрюле в горах. Тепло, подводимое к воде, вызывает преобразование ее водяного газа при температуре ниже 100 градусов Цельсия. При этом уровень в герметичной кастрюле не меняется, так как поглощенное количество теплоты компенсируется уменьшением числа молекул воды.
Как результат, вода начинает кипеть при температуре ниже 100 градусов Цельсия. Это объясняет, почему в горах пища готовится на меньшей температуре, и время приготовления увеличивается. С другой стороны, бактерии, которые обезвреживаются при кипении вода, могут оставаться в живых при более низкой температуре кипения.
Следует отметить, что в горах необходимо учитывать влияние и других факторов, таких как размер герметичной кастрюли и ее теплоемкость. Большие размеры и высокая теплоемкость кастрюли могут вызвать более медленное кипение, так как больше тепла будет необходимо для нагревания кастрюли до начала процесса кипения.
Также стоит отметить, что температура кипения в горах может изменяться в зависимости от высоты над уровнем моря. К примеру, в городе Ла-Пас, в Боливии, расположенном на высоте 3600 метров над уровнем моря, вода начинает кипеть уже при температуре около 85 градусов Цельсия.
Температура кипения воды в шахте
В обычных условиях, при атмосферном давлении, температура кипения воды составляет примерно 100°C. Однако, согласно закону изменения давления с глубиной, с понижением давления в шахте температура кипения воды также уменьшается. Это объясняется физическими свойствами воды и ее теплоемкостью.
Вода в шахте находится в охлаждающемся пространстве, где давление ниже атмосферного. При этом, единицы тепла, необходимые для преобразования воды в пар, больше, чем при атмосферном давлении. Таким образом, чтобы закипеть, вода в шахте должна достичь температуры ниже 100°C.
Процесс изменения температуры кипения воды в глубокой шахте может быть проверен на практике. Для этого можно использовать бульон или другой охлаждающийся источник, чтобы нагреть его в вакууме. При пониженном давлении, температура кипения жидкости увеличится, что позволит пронаблюдать изменение состава и объема воды с течением времени.
Важным фактором при рассмотрении температуры кипения воды в шахте является также применение специальной одежды и оборудования для работы на глубине. Города, строительство которых связано с разработкой шахт и горных работ, часто располагаются на больших глубинах. В таких условиях, существует необходимость учитывать изменение температуры кипения воды и принимать меры для обеспечения безопасности работников.
| Температура (°C) | Давление (атм) |
|---|---|
| 100 | 1 |
| 95 | 0.9 |
| 90 | 0.8 |
| 85 | 0.7 |
| 80 | 0.6 |
| 75 | 0.5 |
Таблица представляет собой примерный показатель изменения температуры кипения воды при разных давлениях. Отметим, что данные значения могут варьироваться в разных условиях и для разных составов воды.
Применение герметической крышки
Вода обычно кипит при температуре 100 °C (212 °F) при атмосферном давлении. Но если добавить соль в кипящую воду, то температура кипения повышается. Например, на 4 градуса Цельсия при добавлении 115 граммов соли на каждый литр воды. Поэтому, приготавливая солёную пищу, называющуюся psia dpva, рецепт которой рассмотрим ниже, необходимо применять герметическую крышку, чтобы поддержать необходимый режим кипения.
Расчета для этого можно проводить с использованием специального технического справочника по измерению давления воды при разных температурах. Ниже приведена таблица, где масса соли указана в граммах, а температура воды измеряется в градусах Цельсия:
Масса соли, г | Температура кипения, °C
0 | 100
58 | 101
116 | 102
174 | 103
232 | 104
290 | 105
348 | 106
… | …
В таблице показано, что с увеличением количества соли в воде температура кипения также увеличивается. Это объясняется тем, что соль образует раствор, который повышает кипящую точку воды.
При готовке блюда «psia dpva» рекомендуется использовать герметическую крышку и измерять температуру, чтобы добиться необходимого количества соли в воде. Для этого можно использовать ртутный термометр, который измеряет температуру воды. Все измерения проводятся на уровне моря.
Один из способов определить, что вода кипит при 115 градусах Цельсия (239 °F), — это использовать герметическую крышку. Когда вода начнет выкипать через отверстие на крышке, это означает, что достигнута нужная температура и можно закончить приготовление блюда.
На практике применение герметической крышки позволяет существенно сократить время приготовления блюда «psia dpva». Также это помогает сохранить полезные вещества в пище, так как при низком давлении происходит меньшее количество их потерь.
Итак, использование герметической крышки при приготовлении блюда «psia dpva» — это важная составляющая процесса готовки. Она позволяет достичь нужного количества соли при определенной температуре и сократить время приготовления, сохраняя полезные вещества в пище.
Кипячение воды в вакууме
Вода кипит при определенной температуре в зависимости от давления. У воды есть удельная температура кипения при нормальном атмосферном давлении, которая составляет 100 градусов Цельсия. Однако, исследования показали, что при уменьшении давления, кипячение воды происходит при более низких температурах.
Когда вода нагревается, ее молекулы начинают двигаться быстрее. Под действием тепла, связи между молекулами ослабевают и они могут ускользнуть друг от друга. При достаточной температуре и давлении, эта свободность движения приводит к появлению пузырьков пара, что и является процессом кипения.
В условиях вакуума, когда давление меньше атмосферного, вода начинает кипеть при более низких температурах. Это связано с уменьшением давления на поверхности воды, что позволяет молекулам легче переходить в газообразное состояние. Подобное явление наблюдается, например, в горных районах, где давление воздуха меньше, и вода кипит при ниже 100 градусах.
Кроме того, в вакууме процесс кипения воды становится стремительным и более интенсивным. Небольшая разность давления между газообразными пузырьками и окружающей средой создает подъем, что приводит к более быстрому образованию пара. Подобные особенности кипячения в вакууме были отмечены в химическом справочнике, где предоставлена таблица с измерениями температур кипения воды при различных давлениях.
Изменение давления существенно влияет на условия кипения воды. Например, если вода подвергается сильному снижению давления, как при создании вакуума, то даже при комнатной температуре она начинает испаряться и кипеть, становясь газообразной. Такое состояние воды позволяет использовать ее для различных технических целей, например, для создания герметической среды в герметичных сосудах или ускоренной стерилизации предметов.
| Давление, мм рт.ст. | Температура кипения воды, °C |
|---|---|
| 10 | 92.2 |
| 5 | 83.2 |
| 1 | 47.8 |
| 0.5 | 30.1 |
Поэтому, при нагревании воды в вакуумных условиях, важно учитывать фактор размера и герметичности посуды, в которой происходит процесс кипения. Малейшие отверстия или неплотности могут увеличить давление и привести к резкому изменению условий кипения.
Кипение солёной воды
Когда мы говорим о температуре кипения воды, как правило, имеем в виду температуру, при которой среднемолекулярные силы притяжения между молекулами жидкости преодолеваются и вода начинает переходить в парообразное состояние. Однако, когда вода содержит растворенные вещества, процесс кипения может изменяться.
Когда вода нагревается до определенной температуры, начинающей называться точкой кипения, ее паровые молекулы становятся достаточно энергичными, чтобы преодолеть силы притяжения и перейти в паровую фазу. Однако, в растворенных веществах, таких как соль или другие ионы, часто возникает явление, называемое элевацией температуры кипения. Это означает, что точка кипения воды повышается при наличии растворенных веществ.
Одной из причин, почему растворенные вещества повышают точку кипения воды, является их влияние на кинетическую энергию молекул. Растворенные вещества уменьшают скорость испарения молекул, поэтому энергия, которую молекулы получат, прежде чем они начнут испаряться, будет больше. Это повышение температуры кипения является эффектом, называемым элевацией кипения.
Для представления зависимости температуры кипения от концентрации растворенных веществ в воде существует формула Клапейрона-Клаузиуса:
dpva/dT = Lv / Rv / T²
- dpva — изменение давления пара от температуры;
- Lv — молярная теплота испарения;
- Rv — универсальная газовая постоянная для паров;
- T — абсолютная температура на шкале Кельвина.
Но что происходит с кипением солёной воды? Фактически, при наличии растворенной соли точка кипения воды повышается. При добавлении соли, ее ионы растворяются в воде и оказывают свое влияние на структуру и взаимодействия молекул воды. Результатом является повышение точки кипения солёной воды.
Таблица ниже предоставляет рекомендации по изменению точки кипения воды с добавлением различных солей:
| Соль | Концентрация | Температура кипения (°C) |
|---|---|---|
| Хлорид натрия (NaCl) | 0.1 M | 100.2 |
| Хлорид натрия (NaCl) | 0.5 M | 101.4 |
| Хлорид натрия (NaCl) | 1.0 M | 102.0 |
Емкости, такие как бактерии, часто используют кипячение для дезинфекции воды. Кипение воды, имеющей повышенную точку кипения, может быть особенно полезным, поскольку это позволяет достичь более высокой температуры для дезинфекции.
Когда говорят о кипении смесей вода-раствор, нельзя не упомянуть горные озера и альпинистов. Горные озера, находящиеся на большой высоте, имеют более низкую атмосферную температуру и, соответственно, ниже атмосферное давление. Поэтому точка кипения воды в горных озерах будет ниже, чем на уровне моря. Альпинисты исследуют этот эффект при подъеме на высоту, и, сталкиваясь с изменением точки кипения воды, принимают меры для соответствующего приготовления пищи и питья.
Таким образом, кипение солёной воды имеет свои особенности, вызванные элевацией кипения, влиянием растворенных веществ на молекулярные взаимодействия, а также изменением атмосферного давления в зависимости от высоты. Поэтому при варке пищи или проведении дезинфекции в воде стоит учитывать эти факторы и принимать соответствующие меры для достижения необходимой температуры и дезинфекционного эффекта.
Температура кипения воды в чайнике
Влияние давления на температуру кипения воды достаточно велико. На глубине 115 метров (375 футов) вода начинает закипать при температуре около 113 градусов Цельсия (235.4°F). В шахте, где присутствуют высокое давление, температура кипения воды может достигать значений более 115 градусов Цельсия (239°F).
Состав воды также влияют на ее температуру кипения. Например, соленая вода имеет более высокую температуру кипения. В таблице справочника можно увидеть, что при добавлении соли к воде, ее температура кипения увеличивается. Соль, находящаяся в морской воде, также влияет на ее температуру кипения, делая ее выше, чем у пресной воды.
Также, вакуум или высокая высота могут снижать температуру кипения воды. В многих районах с высокой высотой наблюдается низкая температура кипения воды, поэтому суть продуктов там закипает при менее высоких температурах.
Одно из интересных наблюдений связанных с кипячением — это быстрое кипячение воды при добавлении соли или сахара в кипящую воду. Энергия, которая была энергией движения молекул воды, теперь используется для разрушения соли или сахара и создания новых молекул. В результате этого процесса образуются микроскопические пузырьки, что и приводит к быстрому и стремительному кипению.
Таблица температуры кипения воды при различных условиях
| Условия | Температура кипения, градусы Цельсия | Температура кипения, градусы Фаренгейта |
|---|---|---|
| Обычное давление на уровне моря | 100 | 212 |
| На глубине 115 метров (375 футов) | 113 | 235.4 |
| В шахте с высоким давлением | 115+ | 239+ |
| С солью (зависит от концентрации) | выше 100 | выше 212 |
| Сахар в кипящей воде | выше 100 | выше 212 |
| Вакуум или высокая высота | ниже 100 | ниже 212 |
Удельная теплоемкость
Удельная теплоемкость жидкостей и твердых тел обычно выше, чем у газов, поэтому вода с высокой удельной теплоемкостью широко используется в промышленности и быту.
Удельная теплоемкость воды зависит от ее температуры. На стадии нагревания ее значение немного увеличивается. Например, при нагревании воды с 0°C до 100°C удельная теплоемкость составляет примерно 4,184 Дж/(г·°C).
Удельная теплоемкость воды также изменяется при изменении агрегатного состояния. Например, при кипении вода превращается в пару, и удельная теплоемкость уменьшается.
Удельная теплоемкость воды является важным фактором в различных областях, включая пищевую промышленность, космическое исследование и химические процессы.
Удельная теплоемкость также играет значительную роль в нашей повседневной жизни. Например, она позволяет нам определить, как долго продукты будут готовиться при нагревании или какую одежду лучше надеть в различные времена года.
Удельная теплоемкость вещества может быть определена экспериментально или вычислена с использованием специальных уравнений и формул. Известно, что наибольшая удельная теплоемкость наблюдается у тяжелых металлов и солей, а наименьшая – у воздуха.
Однако при пониженном давлении (например, в городе на высоте) температура кипения воды будет ниже. Согласно физическому уравнению, известному как уравнение Клапейрона, температура кипения воды находящейся на поверхности Луны, где давление близко к нулю, составляет примерно 374°C.
Кипение воды сопровождается появлением пузырьков пара, которые с высокой скоростью движутся вверх. Это связано с кинетической энергией молекул, которая при нагревании увеличивается. При достижении критической температуры и давления, пар полностью заполняет пространство, образовавшееся в результате испарения жидкости.
Это явление вызывает звуковые волны, которые слышны в виде характерного шипения или свиста при кипении воды. Также известно, что при кипении барометром можно измерить давление пара, которое зависит от его температуры.
Видео:
Урок 124 (осн). Зависимость температуры кипения жидкости от давления
Урок 124 (осн). Зависимость температуры кипения жидкости от давления автор: Павел ВИКТОР 50 066 переглядів 3 роки тому 50 хвилин