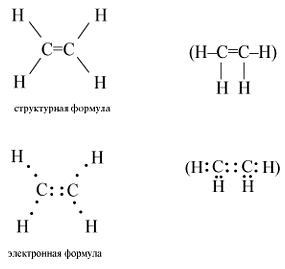
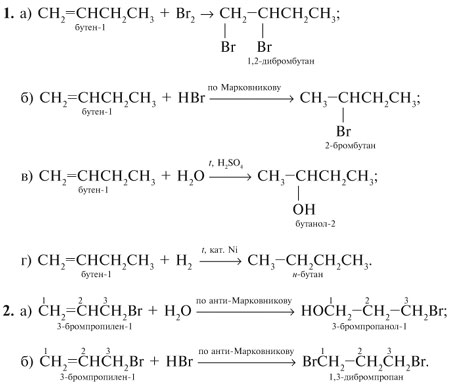
- Процесс гидратации: взаимодействие этилена с водой
- Взаимодействие этилена с водой является реакцией гидратации
- Этилен и этен: получение, свойства и химические реакции
- Этилен (этен) — получение, свойства, химические реакции
- Этилен (этен) — формула, газ и характеристики
- Физические свойства этилена (этена)
- Физические свойства
- Процессы получения
- Применение в промышленности
- Взаимодействие с водой
- Химические свойства этилена (этена)
- Свойства и использование
- Получение этилена (этена). Химические реакции – уравнения получения этилена (этена)
- Применение и использование этилена (этена)
- Видео:
- Органическая химия с нуля
Процесс гидратации: взаимодействие этилена с водой
Взаимодействие этилена (этена) с водой является одной из основных реакций гидратации. В результате этого процесса образуются этиленгликоль и вода. Реакция гидратации этена обладает рядом характеристик, которые определяются свойствами взаимодействующих веществ. Данная реакция является прямой и проводится при повышенных температурах и в присутствии каталитических систем, таких как сернокислотная и фосфорная кислоты, фосфорные соединения и другие органические и неорганические кислоты. Такие катализаторы применяются для увеличения скорости процесса.
В гидратационной смеси этилена и воды происходит ромачивание двойной углеродной связи в молекуле этена, атом водорода атакует один из атомов углерода, образуя новую одинарную ковалентную связь между атомами углерода и водорода. При этом углеродная связь ослабевает, что позволяет объединять два атома водорода, образуя молекулярный водород. Формула уравнения этой реакции представляется следующим образом:
C2H4 + H2O → C2H4O + H2
Такой метод получения этиленгликоля широко применяется в химической и фармацевтической промышленности. Гидратация этилена осуществляется на контактных аппаратах, в которых создаются оптимальные условия для проведения реакции. Физические и химические характеристики этой реакции зависят от различных факторов, таких как давление, температура, концентрации веществ и катализатора.
Образование этиленгликоля в результате гидратации этилена имеет большое значение для растений. Этот органический соединение является ценным продуктом обмена веществ, который принимает активное участие в жизнедеятельности растений. Кроме того, этиленгликоль используется также в других отраслях производства, например, для получения спиртов, олефинов и других органических соединений.
Взаимодействие этилена с водой является реакцией гидратации
Гидратация этена проводится при высоких температурах и давлении в присутствии катализатора, часто используется серная кислота. Уравнение гидратации этена имеет следующий вид:
C2H4 + H2O → C2H6O
Этен растворяется в воде, и процесс гидратации протекает в несколько стадий. Сначала происходит адсорбция этеновых молекул на поверхности катализатора, затем происходит разрыв двойной связи и образуется алкилсерные группы. На последней стадии происходит реакция с водой и получение этиленгликоля.
Гидратация этилена имеет прямой характер и является быстрой реакцией. Она протекает при повышенных температурах и давлениях, а также требует применения катализатора. Как правило, гидратацию проводят в промышленных условиях в специальных печах или реакторах.
В промышленности гидратация этилена часто используется для получения этиленгликоля, который широко применяется в производстве различных классов химических соединений, таких как полиэфиры, полиэстеры, пластиковые полимеры и многое другое. Кроме того, этиленгликоль используется в качестве охлаждающей жидкости, антифриза и пропана.
Спирты также могут быть получены из этилена путем гидратации. Возможны различные способы получения спиртов, включая метод гидрогенизированного этилена, контактный метод и другие. Спирты, такие каюмэтанол, глицерин, этанол и др., имеют различные свойства и характеристики.
Таким образом, взаимодействие этилена с водой является важным процессом гидратации, который играет важную роль в промышленности и обеспечивает получение различных химических соединений, включая этиленгликоль и спирты.
| Реакция | Уравнение |
|---|---|
| Гидратация этена | C2H4 + H2O → C2H6O |
Этилен и этен: получение, свойства и химические реакции
Взаимодействие этилена с водой является реакцией гидратации. При этом процессе этилен и вода образуют этиленгликоль, который является важным предшественником для производства различных соединений, таких как этиловый спирт и серная кислота. Уравнение этой реакции выглядит следующим образом:
С2Н4 + H2O → С2Н6О2
Гидратацию этилена можно проводить при высоких температурах и давлениях с применением катализатора класса контактных печей. Этот процесс является важным для производства этиленгликоля, который находит применение в химической промышленности.
Этилен также может взаимодействовать с кислородом под действием катализатора в процессе окисления, образуя углекислый газ и воду:
2С2Н4 + 3O2 → 4СО2 + 4H2O
Также этилен может реагировать с серной кислотой, образуя этилсульфат:
C2Н4 + 2H2SO4 → С2Н5SO4H
Этилен также может проводить растворение в серной кислоте, при этом образуются этилсульфоновая кислота и серная кислота:
C2Н4 + H2SO4 → C2Н5HSO4
Этилен взаимодействует с алкинами, образуя характерную двойную связь:
С2Н4 + Х — Х = С2H2 + Х — Х
Одной из важных реакций, в которых участвует этен, является его прямое окисление кислородом:
C2H4 + O2 → C2H2O + H2O
Также этен может реагировать с водородом в присутствии катализатора и формировать этан:
C2H4 + H2 → C2H6
Благодаря своим химическим свойствам, этилен и этен нашли широкое применение в различных отраслях промышленности и сельского хозяйства. Они используются для получения различных соединений, полимеров и других продуктов, которые являются необходимыми для производства различных товаров и материалов.
Таким образом, этилен и этен играют важную роль в химических реакциях, процессах производства и различных областях нашей жизни.
Этилен (этен) — получение, свойства, химические реакции
Для получения этилена применяют различные методы, однако наиболее широко распространенный способ — прямая гидратация этилена. Гидратация — это химическая реакция, при которой алкилен (в данном случае этилен) реагирует с водой, образуя соответствующий спирт (этиловый спирт).
- Одним из способов получения этилена является фосфорная гидратация. Этот метод применяется в промышленности.
- Другой метод получения этилена — прямая гидратация сернокислотой. Он также находит широкое применение в промышленности.
Результатом взаимодействия этилена с водой является образование этиленгликоля (этилендигликоля). Эта реакция может быть представлена следующим уравнением:
C₂H₄ + H₂O → C₂H₆O₂
Свойства этиленгликоля и его соединений рассматриваются в контексте химической промышленности и их применения. Олефины, к которым относится этилен, являются важными сырьевыми материалами для производства пластиков, резин и других органических соединений.
Промышленное получение этилена осуществляется с использованием катализатора, который ускоряет скорость реакции. Схема промышленного процесса включает стадии гидратации и разделения полученной смеси соединений, включая этилен и этиленгликоль.
Этилен (этен) — формула, газ и характеристики
Этилен (этен) широко используется в промышленности для получения различных органических соединений. Одним из основных методов получения этена является гидроформирование, когда пары этилена проходят через катализатор при высоких температурах и давлениях.
Этилен обладает рядом свойств, делающих его ценным в промышленности и сельском хозяйстве:
- Высокая скорость реакции: Этилен способен быстро гидрогенизироваться в присутствии водорода при использовании катализаторов.
- Химическая реакция с водой: В результате гидратации этилен взаимодействует с водой, образуя этиленгликоль.
- Применение в различных сферах: Этилен широко используется в промышленности для получения пластмасс, резиновых изделий, растительных гормонов для растений и других химических соединений.
Согласно схеме получения этилена, гидратация проводится в контактном способе при давлениях и температурах, специальных для проведения реакции.
Этилен обладает следующими физическими характеристиками:
- Формула: C2H4
- Молекулярная масса: 28.05 г/моль
- Кипение: -103.7°C
- Плотность: 0.97 г/см³
- Температура автоокисления: 426°C
Таким образом, этилен (этен) – это важный газ, который находит применение в различных отраслях промышленности и сельском хозяйстве.
Физические свойства этилена (этена)
Физические свойства
- Температура кипения этена составляет -103,7 °C, а его температура плавления -169,2 °C.
- Этилен – бесцветный газ с резким запахом.
- При нормальных условиях давления и температуры этен образует гомогенную смесь с водой и многими органическими растворителями.
- Этилен обладает малой растворимостью в воде.
- Этилен – горючий газ, который может соединяться с кислородом и образовывать высокоэнергетический газовый смесь.
Процессы получения
Этилен можно получить различными способами, например:
- Контактным методом с использованием фосфорной кислоты в качестве катализатора.
- Методом гидрогенизированного разрыва серных связей, при котором сернистый газ пропускают через непредельные алкилсульфаты, образуя серные эфиры. Затем эфиры пропускают через сернокислотную смесь, что приводит к получению диолефинов. Процесс заключается в осуществлении гидратации сернокислотой.
Применение в промышленности
Этилен является важным сырьем для производства различных химических соединений, таких как этиловый спирт, этиленгликоль, этилендиамин и др. Он также используется в процессе получения пластиков, резин, восков, ацеталей и других продуктов.
Взаимодействие с водой
Взаимодействие этилена (этена) с водой является реакцией гидратации. При этом двухкушеточное соединение (этанол) превращается в нетоксичные спирты, которые могут использоваться в сельском хозяйстве и взаимодействовать с растениями.
Химические свойства этилена (этена)
Одним из основных химических свойств этилена является его реакция с водой, известная как гидратация. В результате этой реакции образуется этиленгликоль. Уравнение реакции гидратации этилена выглядит следующим образом:
C2H4 + H2O → C2H5OH
Гидратация этилена является прямой реакцией, которая проводится при повышенных температурах и давлениях в присутствии кислоты или щелочи в качестве катализатора.
Кроме гидратации, этилен может участвовать в ряде других реакций, включая гидрогенизацию (присоединение водорода) и реакции с различными органическими и неорганическими соединениями. Эти реакции могут привести к образованию различных продуктов, например этиленового гликоля или этиленового спирта.
Физические свойства этилена включают низкую теплоту образования связей между атомами углерода, что делает его газообразным при комнатной температуре и давлении. Кроме того, этилен обладает хорошей растворимостью в органических растворителях.
Химический состав этилена позволяет его использовать в различных отраслях промышленности. Он находит применение в производстве пластиков, резиновых изделий, синтетических волокон, а также в процессе получения различных органических соединений.
Согласно схеме представленной ниже, этилен может получаться из этана путем разрыва карбон-углеродных связей при использовании фосфорной или сернокислотной кислот в качестве катализатора:
CH2CH2 → CH2=CH2
Свойства и использование
Этилен имеет широкое применение в химической и промышленной сфере, особенно на этапе синтеза полимеров и в процессах производства пластиков и резиновых материалов. Он может быть гидрогенизирован в присутствии катализаторов, что приводит к образованию этиленового спирта.
Этилен также используется в сельском хозяйстве для обработки растений. Он способствует ускоренному созреванию и сохранению плодов и овощей, а также ингибирует рост нежелательных растений.
Получение этилена (этена). Химические реакции – уравнения получения этилена (этена)
1. Гидратация этана. Одним из методов получения этена является гидратация этана с использованием катализатора. Согласно химической схемы процесса, в результате гидратации этана при повышенных температурах и давлениях, осуществляется разрыв связи атомов водорода и углеродной цепи. Полученный этан гидрогенизируется к получению этилена (этена) следующим образом:
C2H6 + H2O → C2H4 + H2
2. Дегидратация этилового спирта. Дегидратация этилового спирта также является методом получения этена. Она осуществляется при контактных температурах в присутствии катализатора (фосфорная кислота). Фосфорная кислота обладает свойствами катализатора и способствует разрыву связи атомов водорода в молекуле этанола.
3. Реакция гидратации. Взаимодействие этилена с водой является реакцией гидратации, в результате которой образуется этанол:
C2H4 + H2O → C2H5OH
Таким образом, получение этилена (этена) может осуществляться различными методами, включая гидратацию этана, дегидратацию этилового спирта и реакцию гидратации этилена. Химические уравнения данных реакций позволяют определить стадии и характеристики процесса получения этена (этилена) в промышленности.
| Метод | Реакция |
|---|---|
| Гидратация этана | C2H6 + H2O → C2H4 + H2 |
| Дегидратация этилового спирта | C2H5OH → C2H4 + H2O |
| Реакция гидратации этилена | C2H4 + H2O → C2H5OH |
Применение и использование этилена (этена)
C2H4 + H2O → C2H5OH
Процесс получения этанола из этилена является прямой реакцией, которая проводится при повышенной температуре и давлении. Результатом этого процесса являются свойства и характеристики этанола. Он применяется в химической промышленности и сельском хозяйстве.
Этилен (этен) также используется для получения других органических соединений. Например, его гидрогенизированное соединение, полученное в результате взаимодействия с водородом при катализе, применяется для производства алкилсерных спиртов — представителей класса спиртов.
В промышленности этилен используется в процессе производства пропилена, мономера для создания пластиков, а также в процессах получения полиэтилена.
Одна из важных химических реакций, в которой участвует этен, это взаимодействие его с серной кислотой. В результате этого взаимодействия образуется этилсерная кислота:
C2H4 + H2SO4 → C2H5SO3H
Применение и использование этилена (этена) в промышленности и сельском хозяйстве составляет важную часть органической химии. Он находит применение в различных отраслях, включая производство пластиков, химической промышленности и сельском хозяйстве.
Видео:
Органическая химия с нуля
Органическая химия с нуля by Химия ЕГЭ Умскул 3,979 views Streamed 5 days ago 4 hours, 59 minutes