- Взаимодействие металлов с водой: иллюстрации и примеры
- Взаимодействие метала с водой примеры
- Какие металлы реагируют с водой
- Все химические реакции, которые необходимы для успешной сдачи ОГЭ
- Правило 11 Взаимодействие простых веществ металлов и неметаллов с водой
- Взаимодействие металлов с водой
- Взаимодействие неметаллов с водой
- Правило 12 Взаимодействие оксидов с водой
- Правило 12
- Взаимодействие оксидов с водой
- Acetyl
- Видео:
- Взаимодействие металлов с растворами солей. 8 класс.
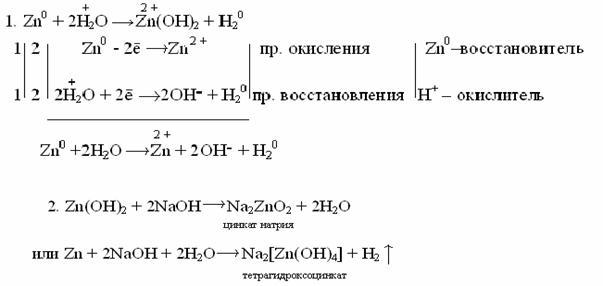
Взаимодействие металлов с водой: иллюстрации и примеры
Взаимодействие металлов с водой является одним из важных химических процессов, которые необходимо запомнить для успешной сдачи ОГЭ по химии. В результате таких реакций образуются водород и гидроксиды металлов — вещества, которые можно встретить как в природе, так и использовать в промышленности.
Щелочные металлы (включая натрий, калий, литий) а таже щелочноземельные металлы (включая магний, кальций) способны реагировать с водой при обычных температурах и условиях. Простые металлы, такие как железо, медь, свинец и цинк, могут взаимодействовать с водой только при повышенной температуре или в присутствии кислорода.
Взаимодействие металлов с водой может быть описано схемой реакции, в которой металл окисляется, а вода восстанавливается. В результате реакции, ионы металла и ионы водорода образуются гидроксид металла и водород.
Примерами таких реакций являются реакция алюминия с водой, в результате которой образуется оксид алюминия и водород, а также реакция железа с водой, которая сопровождается образованием гидроксида железа(III) и водорода.
Взаимодействие метала с водой примеры
Металлы реагируют с водой с образованием гидроксидов и выделением молекулярного водорода. Реакция металла с водой может быть представлена следующей схемой:
| Металл | Реакция с водой |
|---|---|
| Натрий (Na) | 2Na + 2H2O → 2NaOH + H2↑ |
| Калий (K) | 2K + 2H2O → 2KOH + H2↑ |
| Магний (Mg) | Mg + 2H2O → Mg(OH)2 + H2↑ |
| Алюминий (Al) | 2Al + 6H2O → 2Al(OH)3 + 3H2↑ |
Взаимодействие металлов с водой является реакцией окисления и восстановления, так как металлы окисляются, а вода восстанавливается до молекулярного водорода. Правило простых веществ гласит, что для успешной сдачи ОГЭ необходимо запомнить основные реакции взаимодействия металлов с водой, включая реакции оксидов, гидроксидов и ионов металлов, описание которых может быть найдено на сайте организаторов ОГЭ.
Какие именно активные металлы будут реагировать с водой, зависит от условий эксперимента и свойств самой воды. Однако общим правилом можно считать, что металлы в верхней части электрохимического ряда более активны и склонны к взаимодействию с водой.
Взаимодействие металлов с водой — это одна из важных химических реакций, которую нужно запомнить для успешной сдачи ОГЭ по химии.
Какие металлы реагируют с водой
Металлы, которые реагируют с водой, могут быть разделены на две группы: щелочные и щелочноземельные металлы. Щелочные металлы, такие как литий (Li), натрий (Na) и калий (K), являются самыми активными металлами при взаимодействии с водой. В результате реакций образуется щелочное гидроксидное вещество и выделяется водород.
Щелочноземельные металлы, такие как магний (Mg) и кальций (Ca), также реагируют с водой, но их активность ниже, чем у щелочных металлов. Реакция данных металлов с водой сопровождается образованием гидроксидов и выделением водорода.
Однако, не все металлы могут быть активными при взаимодействии с водой. Некоторые металлы, такие как железо (Fe) и алюминий (Al), мало активны и не реагируют с водой при обычных условиях температуры и давления.
Взаимодействие металлов с водой можно описать следующей схемой:
- Металл + Вода → Гидроксид металла + Водород
Различные металлы могут реагировать с водой с разными скоростями и образовывать различные оксиды в процессе восстановления. Например, при взаимодействии натрия с водой образуется гидроксид натрия и выделяется водород. Реакция выглядит следующим образом:
2Na + 2H₂O → 2NaOH + H₂↑
В результате реакции образуются гидроксид ионы щелочного металла и гидроксид водорода.
Как можно запомнить, какие металлы реагируют с водой? Для успешной сдачи ОГЭ по химии важно знать основные примеры металлов, которые реагируют с водой и образуют гидроксиды. Вот некоторые примеры:
- Литий (Li) + Вода → Гидроксид лития + Водород
- Натрий (Na) + Вода → Гидроксид натрия + Водород
- Калий (K) + Вода → Гидроксид калия + Водород
- Магний (Mg) + Вода → Гидроксид магния + Водород
- Кальций (Ca) + Вода → Гидроксид кальция + Водород
Таким образом, знание реакций металлов с водой является важным для понимания основ химии и может быть использовано при решении задач на ОГЭ. Для получения более полной информации о взаимодействии металлов с водой, вы можете обратиться к учебным материалам или химическим сноскам на официальном сайте ОГЭ.
Все химические реакции, которые необходимы для успешной сдачи ОГЭ
Для успешной сдачи ОГЭ необходимо знать и уметь описывать различные химические реакции, включающие взаимодействие металлов с водой, неметаллов с водородом и щелочных металлов с щелочью.
Взаимодействие металлов с водой может быть представлено следующей схемой реакции:
Металл + Вода → гидроксид металла + водород
В зависимости от активности металла данная реакция может протекать при различных условиях. Например, активные металлы, такие как натрий и калий, реагируют с водой уже при комнатной температуре, образуя гидроксид металла и высвобождая водород.
Еще один пример такой реакции – взаимодействие щелочных металлов (например, натрия и калия) с щелочью (например, гидроксидом натрия или калия). В результате такой реакции образуется гидроксид металла и высвобождается водород:
Щелочный металл + Щелочь → гидроксид металла + водород
Однако, малоактивные металлы не реагируют с водой или другими веществами, поэтому для успешной сдачи ОГЭ важно запомнить, какие металлы являются активными и какие – малоактивными. Для этого можно воспользоваться правилом о расположении элемента в распределении оксидных свойств:
Активные металлы расположены слева от акцепторов электронов, малоактивные – справа.
Кроме того, для успешной сдачи ОГЭ необходимо знать реакции взаимодействия неметаллов с водородом. Такие реакции сопровождаются образованием гидроксидов и ионов водорода. Например, взаимодействие сероводорода с кислородом:
Сероводород + Кислород → Вода + Сернистая кислота + Водород
Успешная сдача ОГЭ также требует знания химических реакций окисления и восстановления. Например, реакции окисления ацетилена и сероводорода:
Ацетилен + Кислород → Углекислый газ + Вода
Сероводород + Кислород → Вода + Сернистая кислота
Запомни эти реакции и ты сможешь успешно сдать ОГЭ по химии! Если необходимо более подробное описание реакций и примеры, то на сайте ОГЭ 12 вы можете найти дополнительные материалы и справочные сноски.
Правило 11 Взаимодействие простых веществ металлов и неметаллов с водой
Взаимодействие металлов с водой
По правилу 11, активные металлы образуют гидроксиды и ионы водорода при взаимодействии с водой. Реакция металла с водой происходит только при определенных условиях, включая употребление натрия, лития, калия или другого металла щелочного ряда, расположенного выше в таблице элементов. Эти металлы являются малоактивными и образуют щелочные гидроксиды.
Например, натрий реагирует с водой по следующей схеме:
2Na + 2H2O -> 2NaOH + H2↑
Реакция лития с водой происходит аналогично:
2Li + 2H2O -> 2LiOH + H2↑
Однако, для взаимодействия более активных металлов с водой, таких как калий, необходимы условия, которые позволят провести реакцию при повышенной температуре или восстановлении оксидной формы металла по схеме:
2K + 2H2O -> 2KOH + H2↑
Таким образом, взаимодействие металлов с водой может быть реализовано лишь для малоактивных металлов. Активные металлы, такие как литий, натрий и калий, реагируют с водой даже под обычными условиями.
Взаимодействие неметаллов с водой
В отличие от металлов, неметаллы реагируют с водой с образованием кислот. Эти реакции являются эндотермическими и требуют подачи энергии. Например, взаимодействие серы с водой происходит по следующей схеме:
S + 2H2O -> H2SO4 + H2↑
Таким образом, взаимодействие неметаллов с водой приводит к образованию кислоты и выделению молекул водорода.
Правило 12 Взаимодействие оксидов с водой
Правило 12
Правило 12 описывает, какие условия необходимы для успешной реакции металлов с водой и какие реакции могут быть возможны.
Взаимодействие оксидов с водой
Оксиды металлов могут взаимодействовать с водой, образуя гидроксиды. Эта реакция может проходить при обычной температуре и даже при пониженной температуре. В схеме реакции взаимодействия оксида с водой образуется водород и гидроксид металла, который может быть щелочным или щелочноземельным.
Примеры реакций взаимодействия оксидов металлов с водой:
- Оксид неметалла + вода → образование кислоты
- Оксид металла + вода → образование основания (гидроксида) металла и выделение водорода
Взаимодействие оксидов с водой является химической реакцией, которая может быть сопровождена восстановлением элемента и образованием гидроксида металла и водорода.
Список оксидов металлов, взаимодействие которых с водой может быть успешной реакцией, расположен на сайте Федерального института педагогических измерений (ФИПИ) и называется «Правило 12». В этом списке приведены оксиды всех металлов, включительно с щелочными и щелочноземельными металлами.
Оксиды некоторых металлов могут быть активными и взаимодействовать с водой даже при низкой температуре. Такие оксиды называются активными оксидами. Они способны вступать в реакции с веществами, тем самым их образуя.
Взаимодействие оксидов металлов с водой включает не только реакцию с образованием гидроксида металла, но и реакцию окисления водорода, который образуется в результате этой реакции.
В таблице ниже представлены примеры реакций взаимодействия оксидов металлов с водой:
| Оксид | Реакция с водой |
|---|---|
| Оксид неметалла | образование кислоты |
| Оксид металла | образование гидроксида металла и выделение водорода |
Взаимодействие оксидов металлов с водой является одной из химических реакций, которые могут протекать в простых веществах, включая металлы и неметаллы.
Взаимодействие оксидов металлов с водой имеет практическое значение и находит применение в различных отраслях химии и промышленности. Оно может быть использовано, например, для получения гидроксидов металлов, используемых в производстве щелочей и соединений этих металлов.
Важно отметить, что взаимодействие оксидов с водой может происходить и без образования гидроксидов металлов, но при этом выделяется водородный газ.
Также взаимодействие оксидов металлов с водой может быть отражено на сноски 11 и 12 в описании химических свойств и реакциях металлов на сайте ФИПИ в разделе «Химия» для подготовки к ЕГЭ(ОГЭ) и может быть содержательной частью задания.
Acetyl
Видео:
Взаимодействие металлов с растворами солей. 8 класс.
Взаимодействие металлов с растворами солей. 8 класс. by МЕКТЕП OnLine ХИМИЯ 22,817 views 3 years ago 12 minutes, 51 seconds