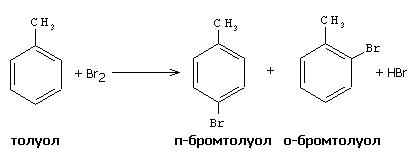
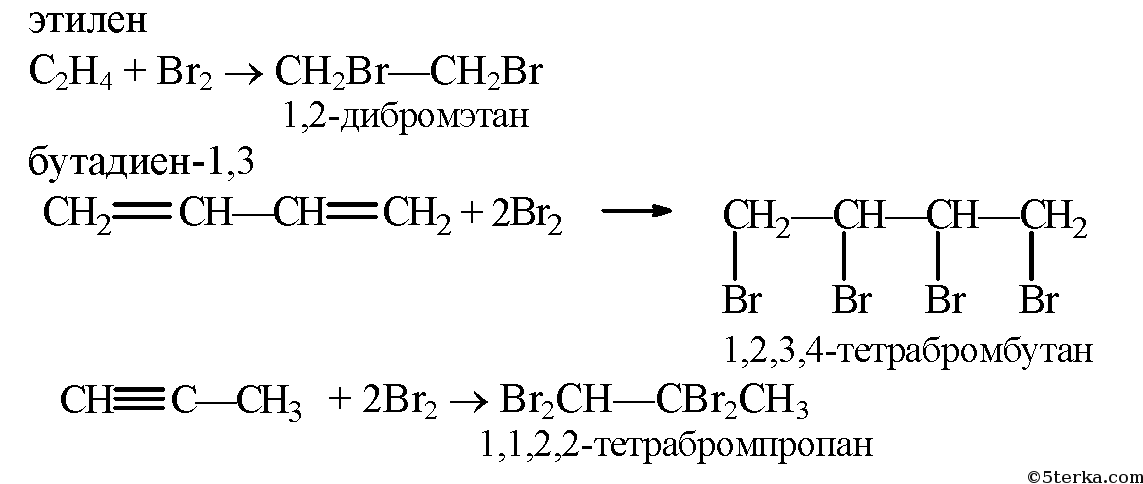
Исследование методов взаимодействия арен с бромной водой
Бромная вода (Br2) – это раствор брома в воде, представляющий собой ценный реагент в химических реакциях аренов. Бром является характерным элементом ароматической гомологической серии, где каждый член содержит гомологическую углеродную цепь и одну или более двойных связей между атомами углерода. Арены, такие как бензол или его гомологи, содержат структурную формулу, в которой шесть атомов углерода образуют устойчивый ароматический цикл, они характерны окислении и замещению.
Бромная вода используется для гидрирования аренов, при этом бензол превращается в циклогексан или его гомологи. Еще одной химической реакцией, в которой применяется бромная вода, является реакция Вюрца-Фиттига – это реакция замещения арены этиленом или ацетиленом. В ходе этой реакции происходит присоединение нового заместителя к молекуле арены.
Кислоты аренов также вступают во взаимодействие с бромной водой. Например, бензойная кислота (C6H5COOH) содержит ароматическую цепь бензола и функциональную группу карбоксильной кислоты. Реакция декарбоксилирования бензойной кислоты под действием бромной воды приводит к образованию бромбензола и углеренной кислоты.
Арены ароматические углеводороды
Арены проявляют ряд химических свойств, которые отличают их от органических соединений без ароматического кольца. Например, они подвергаются реакциям замещения, кисления, окисления, алкилирования, нитрования и дегидрирования.
Присоединение заместителей к аренам происходит главным образом в позициях орто-, мета- и паразамещения. Также возможно присоединение заместителей, таких как сульфирование и солевые формирования.
У аренов также есть особенности в реакциях замещения. Например, бензольные кольца, содержащие дополнительные заместители, могут подвергаться сульфированию, нитрованию или окислению, причем протекающие реакции могут зависеть от реагирующих веществ и катализаторов.
Еще одной особенностью аренов является горение. При горении аренов также образуется углекислый газ и вода.
Свойства ароматических углеводородов также определяются их структурой и наличием функциональных групп. Например, арены с различными заместителями могут иметь разные свойства и применения. Некоторые арены, например, метилциклогексан или изопропилбензол, могут использоваться в качестве растворителей, а другие могут применяться в производстве пластиков, лекарств и других органических соединений.
Таким образом, арены представляют уникальный класс органических соединений, характеризуемый своими химическими свойствами и структурой ароматического кольца. Их преимущественно ароматическая центральная система кольца придает им разнообразные свойства и позволяет использовать их во многих химических реакциях и промышленных процессах.
Строение аренов
Структурная особенность аренов — наличие одной или более групп заместителей (алкилов, галогенов, амино и др.) в ароматическом кольце. Альфа-положение, то есть позиция напротив либо рядом с заместителем, является наиболее реакционноспособным.
Ароматические кольца аренов обладают высокой степенью стабильности из-за наличия двойных связей между атомами углерода, а также конфигурации электронной оболочки, которая определяет их особые химические свойства.
Окисление аренов происходит с образованием бензойной кислоты или ее солей. Нитрование и гидрирование аренов может привести к образованию аминов.
Арены могут участвовать в реакциях замещения, алкилирования и кумулированного гидрирования. Арены с непредельными алкильными заместителями могут быть проалкилированы.
Заместитель арены может быть удален при взаимодействии с бромной водой, перманганатом натрия и другими химическими веществами. Присоединение атома брома к ароматическому кольцу может привести к образованию солей бромноватной кислоты.
Также, арены могут быть подвержены дегидроциклизации и тремеризации при высокой температуре и давлении, что приводит к формированию новых ароматических колец и например тримеров аренов.
Гомологический ряд аренов
В гомологическом ряду аренов можно наблюдать замещение одного или нескольких атомов водорода на другие заместители, такие как алкильные группы, галогены и др. Количество заместителей определяется числом атомов углерода в органическом заместителе. Например, в метилбензоле один атом водорода замещен метильной группой (CH3), а в пропилбензоле — пропильной группой (C3H7).
Реакции аренов обусловлены их строением и свойствами. Бензол и его замещенные производные обладают ароматическими свойствами и могут подвергаться различным химическим превращениям. Одной из таких реакций является окисление аренов перманганатом калия или другими окислителями, при котором происходит пропиленом. Другой характерной реакцией аренов является их сульфирование, при котором к бензолу или его замещенным производным добавляется концентрированная серная кислота, что приводит к образованию соответствующих бензойных солей. Также арены способны к гидрированию и галогенации под действием различных веществ и условий.
Гомологический ряд аренов включает в себя различные гомологи, которые отличаются друг от друга наличием разных заместителей. Например, в ряду аренов с 1-метилбензолом (толуолом) и 1,2-диметилбензолом (ксилолом) можно наблюдать изомерию.
Каждый гомолог аренов имеет свое название, которое определяется в соответствии с правилами номенклатуры органических соединений. Например, для 1-метилбензола применяется название метилтолуол, а для 1,2-диметилбензола — диметилксилол. Номенклатура аренов включает в себя указание числа заместителей и их положение относительно основного кольца.
Таким образом, гомологический ряд аренов является важной частью изучения органической химии. Эти соединения обладают уникальными свойствами и могут подвергаться различным реакциям, что делает их интересными объектами исследования.
Номенклатура аренов
Бромирование аренов происходит взаимодействием бромной кислоты с молекулой арены, при котором одинарные связи в ароматическом кольце замещаются атомами брома. Также возможно хлорирование аренов с помощью хлорной кислоты, при котором в молекуле арены замещаются атомы хлора.
Плотность аренов обычно высокая, а их формула можно представить в виде общей формулы CnHn где n — количество атомов углерода в кольце арены. Название аренов образуется от названия алкана, в котором соответствующее ароматическое кольцо является замещенным на одну или несколько позиций атомами ароматической группы.
Арены могут претерпевать различные реакции, такие как окисление, декарбоксилирование, дегидрирование и многие другие. Например, в реакции Вюрца-Фиттига арены окисляются до соответствующих гомологов с помощью углекислого газа. Также арены могут подвергаться гидрированию, циклизации и гомологации при действии различных реактивов.
Бензойная кислота, под действием окислительного агента, окисляется до углекислого газа, ароматические углеводороды подвергаются гидрированию, декарбоксилированию и другим реакциям. Также арены могут подвергаться замещению атомов в кольце при действии различных химических реагентов.
Изомерия аренов
Как известно, кольцо бензола (C6H6) состоит из шести атомов углерода и шести атомов водорода. При взаимодействии с бромной водой арены происходит галогенирование ароматических углеводородов. В результате этой реакции одна или несколько водородных атомов в бензоле замещаются атомами брома, в общей сложности до семи атомов. Реакция проводится при комнатной температуре в присутствии катализаторов, таких как хлорэтан или газообразный хлор, а также слабых органических кислот.
Изомерия аренов связана с полным или частичным замещением одной или нескольких водородных атомов в бензоле различными функциональными группами. В результате замещения атомов водорода метиловой группой (–CH3) образуется толуол (метилбензол), а при замещении атомов водорода нитро-группой (–NO2) образуется нитробензол.
Полное замещение атомов водорода орто-хлортолуола дает хлорбензол. Изомеры аренов также могут образовываться при окислении циклоалканов перманганатом калия в нейтральной кислоте или при дегидрировании ароматических углеводородов.
Орто-хлортолуол и его изомеры подвергаются галогенированию и окислению в присутствии кислоты. При нагревании аренов сильными окислителями, такими как перманганат калия или горячая концентрированная серная кислота, происходит образование бензойной кислоты.
| Изомер | Формула |
|---|---|
| Орто-хлортолуол | C7H7Cl |
| Метилбензол | C7H8 |
| Нитробензол | C6H5NO2 |
| Хлорбензол | C6H5Cl |
| Бензойная кислота | C7H6O2 |
Видео:
Арены: реакция замещения | Химия 10 класс | Умскул
Арены: реакция замещения | Химия 10 класс | Умскул by Химия ЕГЭ для 10 класса Умскул 2,171 views Streamed 2 years ago 1 hour, 7 minutes