Химическая реакция между свинцом и водой: уравнение взаимодействия
Переходя из разных соединений и растворов, свинец и вода реагируют, образуя различные вещества. Одними из таких соединений являются соли свинца. Уравнение реакции свинца с водой учтено в химической формуле, образующейся при этом.
Одним из химических соединений свинца в природе является окись свинца (PbO), также известная как галома, которая может образоваться в результате действия кислоты на свинцовый порошок. При этом маслянистый порошок постепенно окрашивается в черный цвет.
Уравнение реакции образования окиси свинца выглядит следующим образом:
Pb + H2O + O2 + CO2 → PbO + CO2 + H2O
Похожие реакции возможны и в щелочах, при действии на свинец водорода или черного свинцового сульфида (PbS). В результате взаимодействия свинца со щелочью образуется гидрат двухвалентной соли свинца (PbII(OH)2), который также темнеет в процессе образования.
Описание реакции и природе образования окиси свинца было представлено на одной из страниц Интернета в ответ на запрос другого пользователя. Можете использовать это описание при написании своей статьи.
Свинец Plumbum
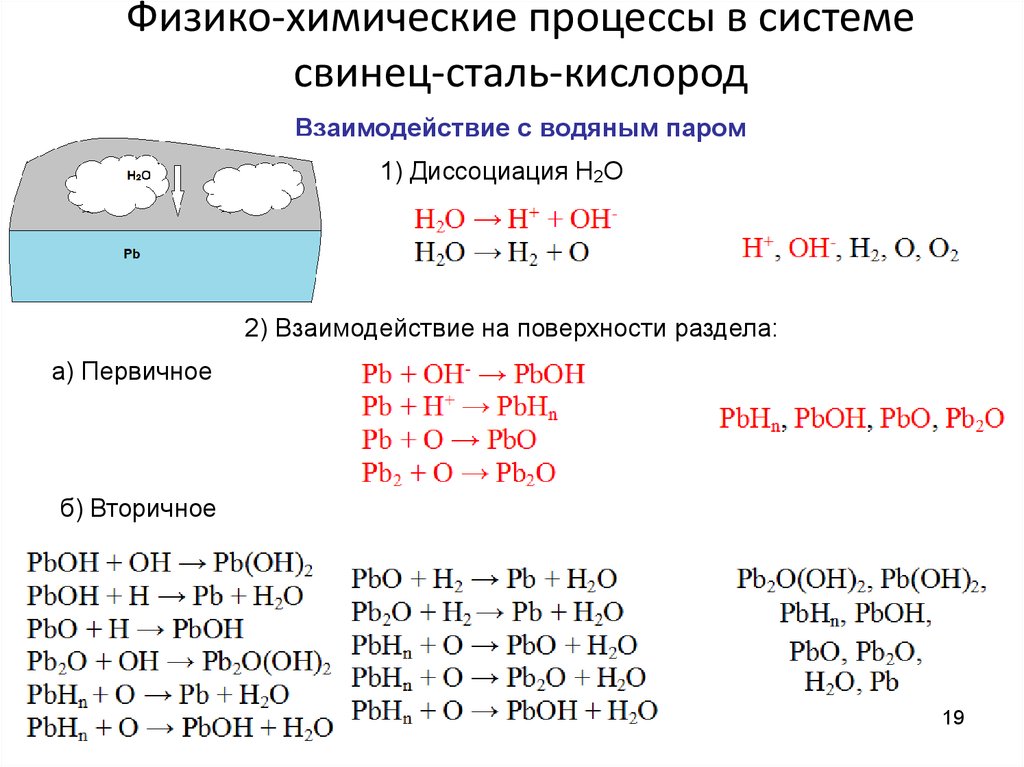
Свинец реагирует с водной паром при нагревании и образует оксид соединение PbO и водород:
2Pb(s) + 2H₂O(g) → 2PbO(s) + H₂(g)
Аналогично двуокись свинца реагирует с кислородом и влагой в воздухе, образуя оксид PbO и воду:
2Pb(s) + O₂(g) + 2H₂O(l) → 2PbO(s) + 2H₂O(l)
Соединение свинца с двухвалентными металлами, такими как олово, образует сплавы. Например, сплав свинца и олова называется оловянным свинцом или оловянным олом. Водные растворы солей свинца обычно имеют кислую реакцию, так как в них есть соединения свинца с кислотными остатками. Соль свинца может быть либо двухвалентной, либо четырехвалентной.
При действии кислоты на свинец образуется соль — ацетат свинца, а при действии щелочей — гидроксид свинца:
2Pb(s) + 4CH₃COOH(aq) → 2Pb(CH₃COO)₂(aq) + H₂(g)
2Pb(s) + 4NaOH(aq) + O₂(g) → 2Na₂PbO₂(aq) + 2H₂O(l)
Соляная кислота и некоторые другие кислоты окисляют свинец до двуокиси свинца (PbO₂), образующийся порошок окрашивается в маслянистый черный цвет. При действии кислорода или щелочей в водной среде свинцовая окись (PbO) темнеет, образуя сначала темно-серую, затем черную окрашенные соединения, которые в щелочах окрашиваются в бернулово желтый цвет.
Таким образом, взаимодействие свинца с водой подобно действию других тяжелых металлов и характеризуется образованием различных соединений. Ввиду высокого количества свинца в нашей среде необходимо принимать меры по его ограничению во избежание отрицательного воздействия на окружающую среду и здоровье человека.
Гидрат окиси свинца РbОН2
Гидрат окиси свинца РbОН2 (pbii) образующийся при действии гидратированных окисей свинца на соответствующие соли, получается из планарно-комплексного ацетата свинца PbО(СН3СОО)2, а также в результате действия more acidic sulfate-hydroxide реакций на двухвалентного свинец, и учётом сложной образования окисла свинца, водорода, кислородом и других неорганических элементов.
Гидрат окиси свинца PbОН2 в природе называется также черным окислом свинца, который похож на гидрат окисла свинцового ПbО(Н2). Очень широко используется в производстве сплавов свинца и олова.
На воздухе гидрат окиси свинца ПbОН2 переходя in the presence в водорода может образовывать гатома масляной кислоты и другие соли черного pigs
Уравнение реакции образования гидрат окиси свинца РbОН2:
- Pb + H2O → PbОН2 + H2
- PbОН2 + H2O → PbОН2 • H2O
- При взаимодействии одного моль гидрат окиси свинца PbОН2 с молью сульфидной кислоты в both) aqueous растворе образуются одна моль соли и одна моль воды:
- PbОН2 + H2SO4 → PbSO4 + 2H2O
Соединения свинца, включая гидрат окиси свинца РbОН2, используются подобно другим соединениям свинца в различных отраслях промышленности, таких как производство красок, аккумуляторных батарей и электронных компонентов.
Видим, что гидрат окиси свинца РbОН2 играет главным образом в процессах образования солей четырехвалентного свинца и может реагировать с кислотой и щелочей, реагирует с водой и образует гидрат окиси свинца РbОН2, а также может образовываться из других окислительных соединений свинца.
Соли двухвалентного свинца
Соль двухвалентного свинца (PbII) образуется при взаимодействии свинца с кислотами или щелочами. Также может образовываться соль двухвалентного свинца при действии соляной кислоты на соответствующий оксид свинца, который вводится в реакцию ввиду своего значительно более высокого растворимости по сравнению с четырехвалентным оксидом свинца (PbO2). Подобно своему аналогу в четырехвалентном состоянии (PbIV), соль двухвалентного свинца также называется сульфатом свинца.
Реакция взаимодействия соли двухвалентного свинца с водой приводит к образованию черного осадка. Это происходит из-за образования двуокиси свинца (PbO) в результате реакции соединения свинца с водой. Похожая реакция происходит и при воздействии свинца на воду в щелочах. В обоих случаях осадок имеет черный цвет.
Кроме того, соль двухвалентного свинца может реагировать с ацетатом свинца при действии кислорода в воздухе. В результате образуется соль свинцового окисла (Pb3O4), которая также имеет черный цвет.
Учитывая образование двухвалентной соли свинца при взаимодействии соединения свинца с водой, можно составить уравнение реакции:
Pb (соль) + H2O → PbO (осадок) + H2 (газ).
Таким образом, соли двухвалентного свинца, образующиеся в результате взаимодействия свинца с водой или другими соединениями, представляют собой черный порошок, который быстро темнеет на воздухе.
Соединения четырехвалентного свинца
Например, сульфат свинца (PbSO4), который является основным соединением в четырехвалентной форме, образуется в результате действия серной кислоты на свинец. Из-за своей невосприимчивости к щелочным растворам, его обычно называют «черной окисью свинца». Гидрат сульфата свинца (PbSO4·H2O) также известен и используется в качестве краски.
Помимо сульфата, существуют и другие соединения четырехвалентного свинца. Например, сульфат свинца (Pb(OH)2) образуется в результате действия щелочей на свинец. Соли этого соединения, такие как ацетат свинца (Pb(CH3COO)2), также имеют значительное значение в химии свинца. Вместе с тем, они довольно растворимы в воде и обычно имеют белый цвет.
Важно отметить, что воздух и вода оказывают существенное влияние на соединения четырехвалентного свинца. Под действием воздуха они темнеют, а под воздействием воды превращаются в двухвалентные комплексы и гатома.
- Реакция взаимодействия свинца с водой может быть представлена следующим уравнением:
Pbo + H2O -> PbON2 + H2
Тем не менее, ввиду значительно меньшей стабильности соединений четырехвалентного свинца по сравнению с двухвалентными, сначала образуется двуокись свинца (PbO), а затем уже происходит реакция с водой. В результате получается гидроксид свинца (PbOH) и выделяется молекулярный водород (H2).
Похожие страницы
При взаимодействии свинца с водой образуется реакция, при которой металл реагирует с кислородом воды, образуя двуокись свинца (PbO) и выделяяся водород (H2). Это уравнение реакции можно представить следующим образом:
2Pb + O2 → 2PbO + H2
Двуокись свинца (PbO) довольно хорошо растворяется в кислоте, образуя соли двухвалентного свинца (Pb2+). Например, в реакции с соляной кислотой (HCl) образуется хлорид свинца (PbCl2):
PbO + 2HCl → PbCl2 + H2O
Свинец также реагирует с щелочами, образуя соли двухвалентного свинца (Pb2+). Например, в реакции с гидроксидом натрия (NaOH) образуется гидроксид свинца (Pb(OH)2):
PbO + 2NaOH → Pb(OH)2 + Na2O
В природе можно найти различные соединения свинца, например, сульфид свинца (PbS), который называется галеной. Галена имеет черный цвет и широко используется в металлургии для получения свинца. При нагревании галены в воздухе образующийся сульфид свинца темнеет и переходит в двуокись свинца:
2PbS + 3O2 → 2PbO + 2SO2
Подобно свинцу, олово также образует стабильные соединения со свинцом в виде сплавов. Описание этих соединений выходит за рамки данной статьи, однако, можно отметить, что олово может образовывать с пьедесталом (белое порошковое вещество), хлорид олова (белая соль) и другие соединения.
Соль свинца, называется ацетат свинца (Pb(CH3COO)2), очень широко используется в медицине, в производстве масляных красок и в других отраслях. В результате запроса на похожие страницы можно найти информацию о различных соединениях свинца, его взаимодействии с другими веществами, а также о методах получения и использования соединений свинца.
Что получится PbO + H2O
Вода (H2O) взаимодействует с двуокисью свинца, образуя гидроксид свинца (Pb(OH)2). При учетом реакции с щелочами, гидроксид свинца называется солью двухвалентного свинцового иона.
Уравнение реакции выглядит следующим образом:
- PbO + H2O → Pb(OH)2
Черный свинец часто используется для создания сплавов и соединений из свинца. Он образует оксиды и соли, которые могут реагировать с водородом, кислотами, щелочами или сульфидами свинца одновременно.
В природе встречаются различные соединения свинца, такие как соляной свинец (PbCl2) или окись свинца (PbO). При воздействии на свинцовые соединения кислородом и водой получается гидроксид свинца (Pb(OH)2), который может быть дальше превращен в другие соединения свинца в зависимости от запроса.
Кроме того, взаимодействие свинца с кислотами или щелочами может привести к образованию других соединений свинца, таких как соли или растворимые гатомы свинца.
Acetyl
Уравнение реакции соли ацетата с водой выглядит следующим образом:
CH3COONa + H2O ⇌ CH3COOH + NaOH
В результате этой реакции возникают ацетат кислоты (CH3COOH) и гидроксид натрия (NaOH).
Одновременно ацетат кислоты может реагировать с кислотой, при этом образуется соляной сложноподобный и ион ацетата:
CH3COOH + H2O ⇌ CH3COO— + H3O+
Уксусная кислота обладает свойством окисляться под действием кислорода воздуха, а также переходить в более широко распространенные оксиды элементов. Работая с уксусной кислотой, необходимо соблюдать меры безопасности, так как она довольно единственен С4 на гатома в масляной краски.
В результате взаимодействия свинца с сульфидом водорода воздуха может образоваться двуокись свинца (PbO), которая в виде порошка свинцом, используется для изготовления сплавов, в том числе для получения черного свинца.
Двуокись свинца также может образовываться вследствие действия щелочей на соль свинца, например:
Pb(NO3)2 + 2 NaOH → Pb(OH)2↓ + 2 NaNO3
Четырехвалентный свинец (+4) часто называется свинцом вальцовского этажа.
Видео:
8 класс. Составление уравнений химических реакций.
8 класс. Составление уравнений химических реакций. by Уроки химии с Жуковой Еленой 122,769 views 2 years ago 14 minutes, 40 seconds